
下图曲线a表示放热反应X(g)+Y(g)Z(g)+M(g)+N(s)进行过程中,X的转化率随时间t变化的关系。若要改变起始条件,使反应过程按b曲线进行,可采用的措施是( )
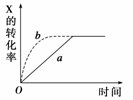
A.升高温度 B.加大X的投入量
C.加催化剂 D.增大体积
科目:高中化学 来源: 题型:
标出电子转移的方向和数目。
2FeCl3 + 2KI = 2FeCl2 + 2KCl + I2 5NH4NO3 = 4N2↑+ 9H2O + 2HNO3
查看答案和解析>>
科目:高中化学 来源: 题型:
3 mol H2和1 mol N2放入密闭容器中,使用催化剂发生反应:N2(g)+3H2(g)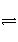
 2NH3(g),从反应开始到平衡过程中,不可能出现的是( )
2NH3(g),从反应开始到平衡过程中,不可能出现的是( )
A.2 mol NH3 B.0.5 mol NH3
C.0.9 mol N2 D.H2和NH3物质的量相等
查看答案和解析>>
科目:高中化学 来源: 题型:
在密闭容器中发生下列反应:aA(g)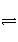
 cC(g)+dD(g),反应达到平衡后,将气体体积压缩到原来的一半,当再次达到平衡时,D的浓度为原平衡的1.8倍,下列叙述正确的是( )
cC(g)+dD(g),反应达到平衡后,将气体体积压缩到原来的一半,当再次达到平衡时,D的浓度为原平衡的1.8倍,下列叙述正确的是( )
A.平衡向正反应方向移动 B.a<c+d
C.D的体积分数增大 D.A的转化率变大
查看答案和解析>>
科目:高中化学 来源: 题型:
在某一容积可变的密闭容器中,可逆反应A(g)+B(g)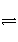
 xC(g) ΔH,符合图象(Ⅰ)所示关系。由此推断,对图象(Ⅱ)的说法不正确的是( )
xC(g) ΔH,符合图象(Ⅰ)所示关系。由此推断,对图象(Ⅱ)的说法不正确的是( )
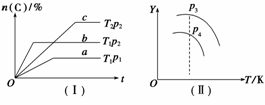
A.p3>p4,Y轴表示A的转化率
B.p3>p4,Y轴表示B的质量分数
C.p3>p4,Y轴表示混合气体的密度
D.p3>p4,Y轴表示混合气体的平均相对分子质量
查看答案和解析>>
科目:高中化学 来源: 题型:
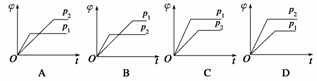
在一定温度、不同压强(p1<p2)下,可逆反应X(g)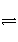
 Y(g)+Z(g)中,生成物Z在反应混合物中的体积分数(φ)与反应时间(t)的关系如下图所示,正确的是( )
Y(g)+Z(g)中,生成物Z在反应混合物中的体积分数(φ)与反应时间(t)的关系如下图所示,正确的是( )
查看答案和解析>>
科目:高中化学 来源: 题型:
25℃时,浓度均为0.1mol·L-1的HA溶液和BOH溶液,pH分别是1和11。下列说法正确的是( )
A. 在0.1 mol·L-1 BA溶液中c(A-)+c(H+)=c(BOH) +c(OH-)
B. 若将0.1 mol·L-1 BOH溶液稀释至0.001 mol·L-1则溶液的pH=9
C. 若将一定量的上述两溶液混合后pH=7,则混合液中:c(A-)> c(B+)
D. 若将上述两溶液按体积比1: 2混合,则混合液中: c(B+) > c(A-) > c(BOH) > c(OH-) > c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
下表中所示物质或概念间的从属关系符合右图的是
| X | Y | Z | |
| A. | 钠元素 | 主族元素 | 短周期元素 |
| B. | 电解质 | 化合物 | 纯净物 |
| C. | 氢氧化铁 | 胶体 | 分散系 |
| D. | 置换反应 | 氧化还原反应 | 放热反应 |

查看答案和解析>>
科目:高中化学 来源: 题型:
短周期元素X、Y、Z、W、Q在元素周期表中的位置如表所示,其中X元素的原子内层电子数是最外层电子数的一半,则下列说法中正确的是双选) )。
A.钠与W可能形成Na2W2化合物
B.由Z与Y组成的物质在熔融时能导电
C.W得电子能力比Q弱
D.X有多种同素异形体,而Y不存在同素异形体
| X | Y | ||
| Z | W | Q |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com