
800℃时,向容积为2L的密闭容器中充入一定量的CO和H2O,发生反应
CO(g)+H2O(g) CO2(g)+H2(g),反应过程中测定的部分数据见下表(表中t1>t2):
CO2(g)+H2(g),反应过程中测定的部分数据见下表(表中t1>t2):
| 反应时间/min | n(CO)/mol | n(H2O)/ mol |
| 0 | 1.20 | 0.60 |
| t1 | 0.80 | |
| t2 | 0.20 |
下列说法正确的是
A.反应在t1min内的平均速率为v(H2)= mol/(L·min)
mol/(L·min)
B.保持其他条件不变,起始时向容器中充入0.60molCO和1.20molH2O,到达平衡时n(CO2)=0.40 mol
C.保持其他条件不变,向平衡体系中再通入0.20molH2O,与原平衡相比,达到新平衡时CO转化率增大,H2O的体积分数增大
D.温度升至1000℃,上述反应平衡常数为1.6,则正反应为放热反应
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
下列关于电解质溶液的叙述不正确的是( )
A.常温下,pH=7的CH3COONa与CH3COOH的混合溶液中离子浓度大小顺序为
c(Na+)=c(CH3COO-)>c(H+)= c(OH-)
B.将pH=10的氨水稀释后,溶液中所有离子的浓度均降低
C.中和pH与体积均相同的盐酸和醋酸溶液,消耗NaOH的物质的量前者小于后者
D.常温下,同浓度的Na2CO3溶液与NaHCO3溶液相比,Na2CO3溶液的pH较大
查看答案和解析>>
科目:高中化学 来源: 题型:
将铁粉、铜粉、FeCl3溶液和CuCl2溶液混合于某容器中充分反应,(假设容器不参加反应)。若过滤后滤渣能被磁铁吸引,则下列有关叙述正确的是 ( )
A.溶液中肯定不存在的离子只有Fe3+
B.Fe3+和Cu2+均能被铁粉还原
C.Fe2+与SCN-能形成红色的物质
D.滤渣中肯定不含有铜
查看答案和解析>>
科目:高中化学 来源: 题型:
实验室制备乙酸丁酯,反应温度要控制在115℃~125℃之间,其他有关数据如下表:
| 物质 | 乙酸 | 1−丁醇 | 乙酸丁酯 | 98%浓硫酸 |
| 沸点 | 117.9℃ | 117.2℃ | 126.3℃ | 338.0℃ |
| 溶解性 | 溶于水和有机溶剂 | 溶于水和有机溶剂 | 微溶于水,溶于有机溶剂 | 与水混溶 |
关于实验室制备乙酸丁酯的叙述错误的是
A.不能边反应边蒸出乙酸丁酯的原因:乙酸丁酯的沸点高
B.不用水浴加热是因为:乙酸丁酯的沸点高于100℃
C.从反应后混合物分离出粗品的方法:用Na2CO3溶液洗涤后分液
D.由粗品制精品需要进行的一步操作:加吸水剂蒸馏
查看答案和解析>>
科目:高中化学 来源: 题型:
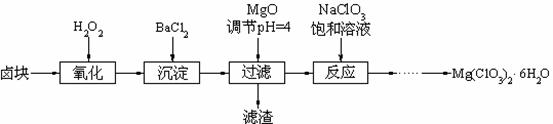
氯酸镁[Mg(ClO3)2]常用作催熟剂、除草剂等,实验室制备少量Mg(ClO3)2·6H2O的流程如下:
已知:
①卤块主要成分为MgCl2·6H2O,含有MgSO4、
FeCl2等杂质。
 ②几种化合物的溶解度(S)随温度(T)变化曲线
②几种化合物的溶解度(S)随温度(T)变化曲线
如右图。
40.加MgO后过滤所得滤渣的主要成分为 。
41.加入BaCl2的目的是除去SO42-,如何检验SO42-已沉淀完全? 。
42.加入NaClO3饱和溶液会发生如下反应:
MgCl2+2NaClO3 Mg(ClO3)2+2NaCl↓,
Mg(ClO3)2+2NaCl↓,
请利用该反应,结合右图,制取Mg(ClO3)2·6H2O的实验步骤依次为:
①取样,加入NaClO3饱和溶液充分反应,② ;③ ;④ ;⑤过滤、洗涤,获得Mg(ClO3)2·6H2O晶体。
产品中Mg(ClO3)2·6H2O含量的测定:
步骤1:准确称量3.50g产品溶解定容成100mL溶液。
步骤2:取10mL于锥形瓶中,加入10mL稀硫酸和20mL1.000mol/L的FeSO4溶液,微热。
步骤3:冷却至室温,用0.100mol/LK2Cr2O7溶液滴定至终点,此过程中反应的离子方程式为:Cr2O72-+6Fe2++14H+ 2Cr3++6Fe3++7H2O。
2Cr3++6Fe3++7H2O。
步骤4:将步骤2、3重复两次,平均消耗K2Cr2O7溶液15.00mL。
43.上述产品测定中需要检查是否漏液的仪器有 。
步骤3中若滴定前不用标准液润洗滴定管,会导致最终结果偏 。(填“大”或“小”)。
44.产品中Mg(ClO3) 2·6H2O的质量分数为 。(计算结果保留两位小数)
查看答案和解析>>
科目:高中化学 来源: 题型:
下列事实所对应的方程式不正确的是
A.盛放氢氧化钠溶液的试剂瓶不能用玻璃塞:SiO2 + 2NaOH === Na2SiO3 + H2O
B.高温下铁与水蒸气反应生成保护膜:2Fe + 6H2O(g)  2Fe (OH)3 + 3H2
2Fe (OH)3 + 3H2
|
D.实验室制取氨气:2NH4Cl + Ca(OH)2 === CaCl2 + 2NH3↑+ 2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)锡为第ⅣA族元素,锡的单质和化合物与某些物质的化学性质有许多相似之处。已知锡元素具有如下性质:
 ;
;




 。
。
试回答:
①锡溶于盐酸,再向反应后的溶液中通入氯气,有关反应类似于铁的相应变化,试写出有关反应的化学方程式:_____________________________________________________,_______________________________________。
②将①中溶液蒸干后继续灼烧所得固体,变化过程类似于FeCl3溶液相应的变化,则最后得到的固体物质是__________(填化学式)。
③若可用SnCl2溶液与过量的碱溶液反应的方法制Sn(OH)2,该碱可选用________。
(2)某无色稀溶液X中,可能含有下表所列离子中的某几种。
| 阴离子 |
|
| 阳离子 |
|
现取该溶液适量,向其中加入某试剂Y,产生沉淀的物质的量(n)与加入试剂Y体积(V)的关系如图所示。

①若Y是盐酸,则溶液中含有的金属阳离子是_________,ab段发生反应的离子方程式为_______________,图中oa段参加反应的阴离子的物质的量之比为___________________。
②若Y是NaOH溶液,则bc段反应的离子方程式为____________________。
若不考虑离子的水解,忽略H+和OH-的影响,且溶液中只存在四种离子,则它们的离子个数比为_____________________________________________(按阳离子在前,阴离子在后,高价在前,低价在后的顺序排列)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com