

| A. | c为正极、d为负极 | |
| B. | 电路中电子的流动方向:b-d-CuCl2溶液-c-a | |
| C. | 电解过程中,d电极质量增加 | |
| D. | 电解过程中,氯离子浓度不变 |
分析 该电解池中,根据电流方向知,a是电源正极、b是负极,c是阳极、d是阴极,阳极上电极反应为2Cl-2e-=Cl2↑、阴极上电极反应为Cu2++2e-=Cu,据此分析解答.
解答 解:A.根据电流方向知,a是正极、b是负极,c是阳极、d是阴极,故A错误;
B.根据电流方向知,电子的流动方向:b-d,c-a,电子不经过溶液,故B错误;
C.电解过程中,d电极电极反应式为Cu2++2e-=Cu,所以d电极质量增加,故C正确;
D.电解过程中阳极电极反应式为2Cl-2e-=Cl2↑,所以氯离子浓度降低,故D错误;
故选C.
点评 本题考查了电解原理,根据电流分析确定电极名称,再结合阴阳极上电极反应式分析解答,题目难度不大.


 春雨教育同步作文系列答案
春雨教育同步作文系列答案科目:高中化学 来源: 题型:解答题

| Fe3+ | Co2+ | Co3+ | Al2+ | |
| pH(开始沉淀) | 1.9 | 7.15 | -0.23 | 3.4 |
| pH(完全沉淀) | 3.2 | 9.15 | 1.09 | 4.7 |
| 温度范围/℃ | 固体质量/g |
| 150~210 | 4.41 |
| 290~320 | 2.41 |
| 890~920 | 2.25 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 +2Br2→
+2Br2→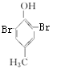 +2HBr
+2HBr
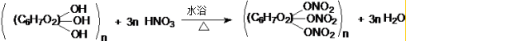 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 加成、水解、加成、消去 | B. | 取代、水解、取代、消去 | ||
| C. | 加成、取代、取代、消去 | D. | 取代、取代、加成、氧化 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
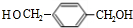 .
. +O2$→_{△}^{Cu}$
+O2$→_{△}^{Cu}$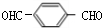 +2H2O.
+2H2O.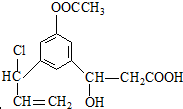 发生反应为①②③④⑤⑥
发生反应为①②③④⑤⑥查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 碳酸钙受热分解 | |
| B. | 灼热的木炭与CO2的反应 | |
| C. | 铝粉与四氧化三铁反应 | |
| D. | Ba(OH)2•8H2O晶体与NH4Cl晶体的反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 将乙酸和乙醇混合加热制乙酸乙酯 | |
| B. | 乙醇、浓硫酸加热到140℃制乙烯 | |
| C. | CH3CH2Br中滴加AgNO3溶液观察是否有浅黄色沉淀,判断卤代烃的类型 | |
| D. | 用CuSO4溶液和过量NaOH溶液混合,然后加入几滴乙醛,加热煮沸观察红色沉淀 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①⑤ | B. | ③④⑤ | C. | ①②⑤ | D. | ②③④ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com