
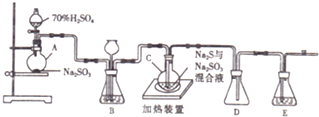
·ÖĪö ×°ÖĆAÖŠÖʱø¶žŃõ»ÆĮņ£¬CÖŠ¶žŃõ»ÆĮņ”¢Įņ»ÆÄĘÓėŃĒĮņĖįÄĘ·“Ӧɜ³ÉNa2S2O3£¬E×°ÖĆ½ųŠŠĪ²Ęų“¦Ąķ£¬·ĄÖ¹ĪŪČ¾æÕĘų£¬æÉŅŌŹ¢·ÅĒāŃõ»ÆÄĘ·“Ó¦£¬DĪŖ°²Č«Ę棬·ĄÖ¹µ¹Īü£¬×°ÖĆBæÉÓĆĄ“¹Ū²ģSO2µÄÉś³ÉĖŁĀŹ£¬Ņ²æÉŅŌøł¾Ż³¤¾±Ā©¶·ÖŠŅŗĆę±ä»ÆÅŠ¶Ļ×°ÖĆŹĒ·ń·¢Éś¶ĀČūµČ×÷ÓĆ£®
£Ø1£©ĮņĖįÓėŃĒĮņĖįÄĘ·“Ӧɜ³ÉĮņĖįÄĘ”¢¶žŃõ»ÆĮņÓėĖ®£»DÖŠ×ó²ąĪŖ¶Ģµ¼¹Ü£¬ĪŖ°²Č«Ę棬·ĄÖ¹µ¹Īü£»
£Ø2£©×°ÖĆEĘšµ½ĪüŹÕĪ²ĘųÖŠSO2”¢H2SµÄ×÷ÓĆ£»ČōCÖŠ·¢Éś¶ĀČū£¬×°ÖĆÄŚĘųŃ¹Ōö“ó£¬BÖŠŅŗĢå»į±»Ń¹Čė³¤¾±Ā©¶·ÖŠ£»
£Ø3£©æŲÖʵĪ¼ÓĮņĖįµÄĖŁ¶Č£¬æÉŅŌæŲÖĘÉś³É¶žŃõ»ÆĮņĖŁĀŹ£»·“Ó¦Na2SO3+S$\frac{\underline{\;\;”÷\;\;}}{\;}$Na2S2O3Ļą¶Ō½ĻĀż£¬ĖłŅŌÉÕĘæCµÄ·“Ó¦ÖÕµćµÄĻÖĻóĪŖČÜŅŗ±ä³ĪĒ壻
¹żĮæµÄ¶žŃõ»ÆĮņŹ¹ČÜŅŗ³ŹĖįŠŌ£¬Na2S2O3ŌŚĖįŠŌĢõ¼žĻĀ²»ĪČ¶Ø£»
£Ø4£©øł¾ŻĢāÄæĖłøų3øö·“Ó¦£¬æÉµĆ³ö¶ŌÓ¦¹ŲĻµ£ŗ2Na2S”«2H2S”«3S”«3 Na2SO3£¬2molNa2S·“Ó¦Ź±Ķ¬Ź±Éś³É2molNa2SO3£¬»¹ŠčŅŖ1molNa2SO3£»
£Ø5£©¼ÓČėŃĪĖį£¬Na2S2O3·“Ӧɜ³ÉS³Įµķ£¬ĖłŅŌ¾²ÖĆŗóČ”ÉĻ²ćĒåŅŗ£¬µĪ¼ÓBaCl2ČÜŅŗ£¬¼ģŃéČÜŅŗÖŠŹĒ·ńŗ¬ÓŠĮņĖįøłĄė×Ó£®
½ā“š ½ā£ŗ×°ÖĆAÖŠÖʱø¶žŃõ»ÆĮņ£¬CÖŠ¶žŃõ»ÆĮņ”¢Įņ»ÆÄĘÓėŃĒĮņĖįÄĘ·“Ӧɜ³ÉNa2S2O3£¬E×°ÖĆ½ųŠŠĪ²Ęų“¦Ąķ£¬·ĄÖ¹ĪŪČ¾æÕĘų£¬æÉŅŌŹ¢·ÅĒāŃõ»ÆÄĘ·“Ó¦£¬DĪŖ°²Č«Ę棬·ĄÖ¹µ¹Īü£¬×°ÖĆBæÉÓĆĄ“¹Ū²ģSO2µÄÉś³ÉĖŁĀŹ£¬Ņ²æÉŅŌøł¾Ż³¤¾±Ā©¶·ÖŠŅŗĆę±ä»ÆÅŠ¶Ļ×°ÖĆŹĒ·ń·¢Éś¶ĀČūµČ×÷ÓĆ£®
£Ø1£©ĮņĖįÓėŃĒĮņĖįÄĘ·“Ӧɜ³ÉĮņĖįÄĘ”¢¶žŃõ»ÆĮņÓėĖ®£¬·“Ó¦·½³ĢŹ½ĪŖ£ŗNa2SO3+H2SO4ØTNa2SO4+SO2”ü+H2O£¬DÖŠ×ó²ąĪŖ¶Ģµ¼¹Ü£¬×÷°²Č«Ę棬·ĄÖ¹µ¹Īü£¬
¹Ź“š°øĪŖ£ŗNa2SO3+H2SO4ØTNa2SO4+SO2”ü+H2O£»×÷°²Č«Ę棬·ĄÖ¹µ¹Īü£»
£Ø2£©×°ÖĆEĘšµ½ĪüŹÕĪ²ĘųÖŠSO2”¢H2SµÄ×÷ÓĆ£¬æÉŃ”ÓĆNaOHČÜŅŗ£¬ČōCÖŠ·¢Éś¶ĀČū£¬×°ÖĆÄŚĘųŃ¹Ōö“ó£¬BÖŠŅŗĢå»į±»Ń¹Čė³¤¾±Ā©¶·ÖŠ£¬ĻÖĻóŹĒ£ŗ׶ŠĪĘæÄŚŅŗĆęĻĀ½µ£¬³¤¾±Ā©¶·ÖŠŅŗĆęÉĻÉż£¬
¹Ź“š°øĪŖ£ŗNaOHČÜŅŗ£»×¶ŠĪĘæÄŚŅŗĆęĻĀ½µ£¬³¤¾±Ā©¶·ÖŠŅŗĆęÉĻÉż£»
£Ø3£©¶žŃõ»ÆĮņĪŖ70%ĮņĖįŗĶŃĒĮņĖįÄĘ·“Ó¦ÖĘČ”µÄ£¬ĖłŅŌĪŖĮĖŹ¹¶žŃõ»ÆĮņ»ŗĀż½ųČėÉÕĘæC£¬²ÉÓĆµÄ²Ł×÷ŹĒæŲÖʵĪ¼ÓĮņĖįµÄĖŁ¶Č£¬
·“Ó¦Na2SO3+S$\frac{\underline{\;\;”÷\;\;}}{\;}$Na2S2O3Ļą¶Ō½ĻĀż£¬ĖłŅŌÉÕĘæCµÄ·“Ó¦ÖÕµćµÄĻÖĻóĪŖČÜŅŗÓÉ»ė×Ē±ä³ĪĒ壬
¹żĮæµÄ¶žŃõ»ÆĮņŹ¹ČÜŅŗ³ŹĖįŠŌ£¬Na2S2O3ŌŚĖįŠŌĢõ¼žĻĀ²»ĪČ¶Ø»į·Ö½ā£¬CÖŠ·“Ó¦Ķź³É·“Ó¦Į¢¼“¹Ų±ÕĀ©¶·ŠżČū£¬Ķ£Ö¹¼ÓČČ£¬
¹Ź“š°øĪŖ£ŗæŲÖʵĪ¼ÓĮņĖįµÄĖŁ¶Č£»ČÜŅŗÓÉ»ė×Ē±ä³ĪĒ壻¹żĮæµÄ¶žŃõ»ÆĮņŹ¹ČÜŅŗ³ŹĖįŠŌ£¬Na2S2O3ŌŚĖįŠŌĢõ¼žĻĀ²»ĪČ¶Ø»į·Ö½ā£»
£Ø4£©øł¾ŻĢāÄæĖłøų3øö·“Ó¦£¬æÉµĆ³ö¶ŌÓ¦¹ŲĻµ£ŗ2Na2S”«2H2S”«3S”«3 Na2SO3£¬2molNa2S·“Ó¦Ź±Ķ¬Ź±Éś³É2molNa2SO3£¬»¹ŠčŅŖ1molNa2SO3£¬ĖłŅŌÉÕĘæCÖŠNa2SŗĶNa2SO3ĪļÖŹµÄĮæÖ®±ČĪŖ2£ŗ1£¬
¹Ź“š°øĪŖ£ŗ2£ŗ1£»
£Ø5£©¼ģ²ā²śĘ·ÖŠŹĒ·ń“ęŌŚNa2SO4µÄŹµŃé·½°øĪŖ£ŗȔɣĮæ²śĘ·ČÜÓŚ×ćĮæĻ”ŃĪĖį”¢¾²ÖĆ”¢Č”ÉĻ²ćĒåŅŗ£Ø»ņ¹żĀĖ£¬Č”ĀĖŅŗ£©”¢µĪ¼ÓBaCl2ČÜŅŗ£¬Čō³öĻÖ³ĮµķŌņĖµĆ÷ŗ¬ÓŠNa2SO4ŌÓÖŹ£¬
¹Ź“š°øĪŖ£ŗȔɣĮæ²śĘ·ČÜÓŚ×ćĮæĻ”ŃĪĖį”¢¾²ÖĆ”¢Č”ÉĻ²ćĒåŅŗ£Ø»ņ¹żĀĖ£¬Č”ĀĖŅŗ£©”¢µĪ¼ÓBaCl2ČÜŅŗ£¬Čō³öĻÖ³ĮµķŌņĖµĆ÷ŗ¬ÓŠNa2SO4ŌÓÖŹ£®
µćĘĄ ±¾Ģāæ¼²éŹµŃé·½°øµÄ·ÖĪöÓėĘĄ¼Ū£¬Éę¼°¶žŃõ»ÆĮņµÄÖʱø”¢Ąė×Ó¼ģŃ锢¶Ō²Ł×÷µÄ·ÖĪöĘĄ¼ŪµČ£¬²ąÖŲŹµŃé·ÖĪöÄÜĮ¦¼°ÖŖŹ¶×ŪŗĻÓ¦ÓĆÄÜĮ¦µÄ漲飬£Ø4£©ĪŖŅדķµć£¬æÉŅŌĄūÓĆ×Ü·“Ó¦µÄ·ÖĪö£¬ĢāÄæÄѶČÖŠµČ£®


 ѧʌø“Ļ°Ņ»±¾ĶØѧĻ°×ܶÆŌ±ĘŚÄ©¼ÓŹī¼ŁŃÓ±ßČĖĆń³ö°ęÉēĻµĮŠ“š°ø
ѧʌø“Ļ°Ņ»±¾ĶØѧĻ°×ܶÆŌ±ĘŚÄ©¼ÓŹī¼ŁŃÓ±ßČĖĆń³ö°ęÉēĻµĮŠ“š°ø Ć¢¹ū½ĢøØŹī¼ŁĢģµŲÖŲĒģ³ö°ęÉēĻµĮŠ“š°ø
Ć¢¹ū½ĢøØŹī¼ŁĢģµŲÖŲĒģ³ö°ęÉēĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
| T/”ę | 700 | 800 | 850 | 1 000 | 1 200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
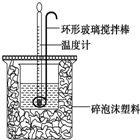 ĄūÓĆČēĶ¼ĖłŹ¾×°ÖĆ²ā¶ØÖŠŗĶČȵďµŃé²½ÖčČēĻĀ£ŗ
ĄūÓĆČēĶ¼ĖłŹ¾×°ÖĆ²ā¶ØÖŠŗĶČȵďµŃé²½ÖčČēĻĀ£ŗ| ŹµŃé ŠņŗÅ | ĘšŹ¼ĪĀ¶Čt1/”ę | ÖÕÖ¹ĪĀ¶Čt2/”ę | |
| ŃĪĖį | ĒāŃõ»ÆÄĘČÜŅŗ | »ģŗĻČÜŅŗ | |
| 1 | 20.0 | 20.1 | 23.2 |
| 2 | 20.2 | 20.4 | 23.4 |
| 3 | 20.5 | 20.6 | 23.6 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ¼ĘĖćĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Ąė×Ó°ė¾¶£ŗY£¾Z£¾W£¾R£¾X | |
| B£® | Ēā»ÆĪļĪČ¶ØŠŌ£ŗX£¾W£¾R | |
| C£® | Y”¢Z”¢WµÄ×īøß¼ŪŃõ»ÆĪļ¶ŌÓ¦µÄĖ®»ÆĪļĮ½Į½¾łæÉ»„Ļą·“Ó¦ | |
| D£® | YÓėZ²»ÄÜ“ęŌŚÓŚĶ¬Ņ»Ąė×Ó»ÆŗĻĪļÖŠ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | AÓėBŠĪ³ÉµÄ»ÆŗĻĪļÖŠÖ»ŗ¬Ąė×Ó¼ü | |
| B£® | AµÄĘųĢ¬Ēā»ÆĪļµÄ·ŠµćŅ»¶ØøßÓŚDµÄĘųĢ¬Ēā»ÆĪļµÄ·Šµć | |
| C£® | ČōAÓėCµÄŌ×ÓŠņŹżĻą²ī5£¬Ōņ¶žÕߊĪ³É»ÆŗĻĪļµÄ»ÆѧŹ½Ņ»¶ØĪŖC2A3 | |
| D£® | ĻąĶ¬Ģõ¼žĻĀ£¬BµÄ×īøß¼ŪŃõ»ÆĪļµÄĖ®»ÆĪļµÄ¼īŠŌ±ČCµÄ×īøß¼ŪŃõ»ÆĪļµÄĖ®»ÆĪļµÄ¼īŠŌĒæ |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com