
【题目】锂电池是一代新型高能电池,它以质量轻、能量高而受到普遍重视,目前已成功研制多种锂电池。某种锂电池的总反应为Li+MnO2===LiMnO2,下列说法正确的是( )
A. Li是正极,电极反应为Li-e-===Li+
B. Li是负极,电极反应为Li-2e-===Li2+
C. MnO2是负极,电极反应为MnO2+e-===MnO![]()
D. Li是负极,电极反应为Li-e-===Li+
科目:高中化学 来源: 题型:
【题目】关于烃通式的叙述正确的是( )
A. 分子式符合CnH2n+2的烃一定是烷烃 B. 分子式符合CnH2n的烃一定是烯烃
C. 分子式符合CnH2n-2的烃一定是炔烃 D. 分子式符合CnH2n-6的烃一定是苯的同系物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】判断下列概念的依据正确的是
A. 纯净物与混合物:是否仅含有一种元素
B. 溶液与胶体:本质不同的原因是能否发生丁达尔现象
C. 强电解质与弱电解质:溶液的导电能力大小
D. 氧化还原反应的本质:有电子转移
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】写出下列反应的化学方程式:
(1)实验室制取乙炔___________________。
(2)2 -氯丙烷的消去反应___________________。
(3)用甲苯制TNT的反应___________________。
(4)l,2-二氯乙烷与NaOH溶液共热___________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关说法正确的是( )
A. 同浓度、同体积的强酸与强碱溶液混合后,溶液的 pH 一定等于 7
B. 0.1 mol·L-1 NH4Cl 溶液与 0.1 mol·L-1 氨水等体积混合(pH>7):c(NH3 ·H2O)>c(NH4+)>c(Cl-)>c(OH-)
C. 0.1 mol AgCl 和 0.1 mol AgBr 混合后加入水中,所得溶液 c(Cl-)=c(Br-)
D. 向 0.10 mol·L-1Na2SO3溶液中通 SO2 气体至溶液 pH=7:c(Na+) = 2c(SO32-)+c(HSO3-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】近年来高铁酸钾(K2FeO4)已经被广泛应用在水处理方面,高铁酸钾的氧化性超过高锰酸钾,是一种集氧化、吸附、凝聚、杀菌的新型高效的多功能水处理剂。高铁酸钾在水处理过程中涉及到的过程正确的有 ( )
①蛋白质的变性 ②蛋白质的盐析
③胶体聚沉 ④盐类水解
⑤焰色反应 ⑥氧化还原反应
A.①②③④
B.①③④⑥
C.②③④⑤
D.②③⑤⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】科学家最近又发现了一种新能源——“可燃冰”。它的主要成分是甲烷分子的结晶水合物(CH4·nH2O)。其形成过程是:埋于海底地层深处的大量有机质在缺氧环境中,厌氧型细菌把有机质分解,最后形成石油和天然气,其中许多天然气被包进水分子中,在海底的低温与高压下形成了类似冰的透明晶体,这就是“可燃冰”。这种“可燃冰”的晶体类型是( )
A. 离子晶体 B. 分子晶体 C. 原子晶体 D. 金属晶体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有易溶强电解质的混合溶液10 L,其中可能含K+、Ba2+、Na+、![]() 、Cl、
、Cl、![]() 、
、![]() 、OH中的几种,向其中通入CO2气体,产生沉淀的量与通入CO2的量之间的关系如下图所示:
、OH中的几种,向其中通入CO2气体,产生沉淀的量与通入CO2的量之间的关系如下图所示:
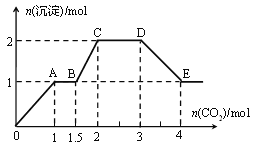
下列说法正确的是
A.该溶液中能确定存在的离子是Ba2+、![]() 、
、![]()
B.肯定不存在的离子是![]() 、OH
、OH
C.若不能确定的离子中至少还存在一种阳离子,则该离子的最小浓度为0.2 mol·L1
D.OA 段反应的离子方程式:2![]() +CO2+3H2O===2Al(OH)3↓+
+CO2+3H2O===2Al(OH)3↓+![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】由铁、锌、铝、镁四种金属中的两种组成的混合物11 g,与足量的盐酸反应产生的氢气在标准状况下为11.2 L,则混合物中一定含有的金属是( )
A. 铁 B. 锌 C. 镁 D. 铝
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com