
 £»
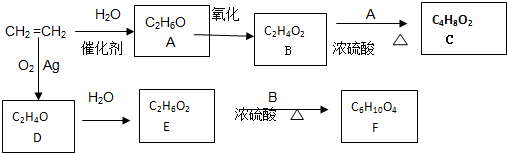
£»·ÖĪö ŅŅĻ©ÓėĖ®¼Ó³ÉÉś³ÉA£¬AĪŖŅŅ“¼£¬ŅŅ“¼“ß»ÆŃõ»ÆÉś³ÉB£¬BĪŖŅŅĖį£¬ŅŅĖįÓėŅŅ“¼·“Ӧɜ³ÉC£¬CĪŖŅŅĖįŅŅõ„£¬ŅŅĻ©ÓėŃõĘų·“Ӧɜ³ÉD£ØC2H4O£©£¬DĪŖ»·ŃõŅŅĶé £¬ŅņĪŖŗóĆęÉś³ÉĪļŅŖÓėŅŅĖį·¢Éśõ„»Æ·“Ó¦°“1£ŗ2·“Ó¦£¬D”śEŹĒæŖ»·¼Ó³É·“Ó¦£¬¹ŹEĪŖŅŅ¶ž“¼£¬ŅŅ¶ž“¼ÓėŅŅĖį·“Ӧɜ³ÉF£ØC6H10O4£©£¬FĪŖ¶žŅŅĖįŅŅ¶žõ„
£¬ŅņĪŖŗóĆęÉś³ÉĪļŅŖÓėŅŅĖį·¢Éśõ„»Æ·“Ó¦°“1£ŗ2·“Ó¦£¬D”śEŹĒæŖ»·¼Ó³É·“Ó¦£¬¹ŹEĪŖŅŅ¶ž“¼£¬ŅŅ¶ž“¼ÓėŅŅĖį·“Ӧɜ³ÉF£ØC6H10O4£©£¬FĪŖ¶žŅŅĖįŅŅ¶žõ„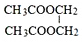 £¬ŅŌ“Ė½ā“šøĆĢā£®
£¬ŅŌ“Ė½ā“šøĆĢā£®
½ā“š ½ā£ŗŅŅĻ©ÓėĖ®¼Ó³ÉÉś³ÉA£¬AĪŖŅŅ“¼£¬ŅŅ“¼“ß»ÆŃõ»ÆÉś³ÉB£¬BĪŖŅŅĖį£¬ŅŅĖįÓėŅŅ“¼·“Ӧɜ³ÉC£¬CĪŖŅŅĖįŅŅõ„£¬ŅŅĻ©ÓėŃõĘų·“Ӧɜ³ÉD£ØC2H4O£©£¬DĪŖ»·ŃõŅŅĶé £¬ŅņĪŖŗóĆęÉś³ÉĪļŅŖÓėŅŅĖį·¢Éśõ„»Æ·“Ó¦°“1£ŗ2·“Ó¦£¬D”śEŹĒæŖ»·¼Ó³É·“Ó¦£¬¹ŹEĪŖŅŅ¶ž“¼£¬ŅŅ¶ž“¼ÓėŅŅĖį·“Ӧɜ³ÉF£ØC6H10O4£©£¬FĪŖ¶žŅŅĖįŅŅ¶žõ„
£¬ŅņĪŖŗóĆęÉś³ÉĪļŅŖÓėŅŅĖį·¢Éśõ„»Æ·“Ó¦°“1£ŗ2·“Ó¦£¬D”śEŹĒæŖ»·¼Ó³É·“Ó¦£¬¹ŹEĪŖŅŅ¶ž“¼£¬ŅŅ¶ž“¼ÓėŅŅĖį·“Ӧɜ³ÉF£ØC6H10O4£©£¬FĪŖ¶žŅŅĖįŅŅ¶žõ„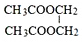 £¬
£¬
£Ø1£©ŹµŃéŹŅĄūÓĆŅŅ“¼ŌŚÅØĮņĖį×÷ÓĆĻĀ¼ÓČČ·¢ÉśĻūČ„·“Ó¦ÖĘŅŅĻ©£¬·“Ó¦·½³ĢŹ½ĪŖ£ŗCH3-CH2-OH$”ś_{170”ę}^{ÅØĮņĖį}$CH2=CH2”ü+H2O£¬
¹Ź“š°øĪŖ£ŗCH3-CH2-OH$”ś_{170”ę}^{ÅØĮņĖį}$CH2=CH2”ü+H2O£»
£Ø2£©BĪŖŅŅĖį£¬EĪŖŅŅ¶ž“¼£¬BŗĶE·“Ӧɜ³ÉFµÄ»Æѧ·½³ĢŹ½ĪŖHOCH2-CH2OH+2CH3COOH $?_{”÷}^{ÅØĮņĖį}$ CH3COOCH2CH2OOCCH3+2H2O£¬øĆ·“Ó¦µÄĄąŠĶĪŖõ„»Æ£ØČ”“ś£©·“Ó¦£¬
¹Ź“š°øĪŖ£ŗHOCH2-CH2OH+2CH3COOH $?_{”÷}^{ÅØĮņĖį}$ CH3COOCH2CH2OOCCH3+2H2O£»õ„»Æ£ØČ”“ś£©·“Ó¦£»
£Ø3£©ÓÉŅŌÉĻ·ÖĪöæÉÖŖDĪŖ»·ŃõŅŅĶé £¬¹Ź“š°øĪŖ£ŗ
£¬¹Ź“š°øĪŖ£ŗ £»
£»
£Ø4£©DĪŖ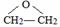 £¬Ķ¬·ÖŅģ¹¹ĢåµÄ½į¹¹¼ņŹ½ĪŖCH3CHO£¬øĆĶ¬·ÖŅģ¹¹ĢåÓėŅų°±ČÜŅŗ·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ£ŗCH3CHO+2Ag£ØNH3£©2OH $\stackrel{”÷}{”ś}$CH3COONH4+2Ag”ż+3NH3+H2O£¬
£¬Ķ¬·ÖŅģ¹¹ĢåµÄ½į¹¹¼ņŹ½ĪŖCH3CHO£¬øĆĶ¬·ÖŅģ¹¹ĢåÓėŅų°±ČÜŅŗ·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ£ŗCH3CHO+2Ag£ØNH3£©2OH $\stackrel{”÷}{”ś}$CH3COONH4+2Ag”ż+3NH3+H2O£¬
¹Ź“š°øĪŖ£ŗCH3CHO+2Ag£ØNH3£©2OH $\stackrel{”÷}{”ś}$CH3COONH4+2Ag”ż+3NH3+H2O£»
£Ø5£©CĪŖŅŅĖįŅŅõ„£¬CµÄĶ¬·ÖŅģ¹¹ĢåÖŠŗ¬Č©»łµÄ½į¹¹æÉŅŌŹĒOHC-C-C-CÉĻĮ¬ÓŠ-OH£¬»ņ½«ŃõŌ×Ó²åŌŚĢ¼Į“ÖŠ¼äŠĪ³É-O-½į¹¹£¬ÕāŃłµÄ½į¹¹ÓŠ6ÖÖ£¬Ģ¼Į“½į¹¹·Ö±šĪŖOHC-CH£ØOH£©-CH2-CH3”¢OHC-CH2-CH£ØOH£©-CH3”¢OHC-CH2-CH2-CH2-OH”¢OHC-O-CH2-CH2-CH3”¢OHC-CH2-O-CH2-CH3”¢OHC-CH2-CH2-O-CH3£¬Ņ²æÉŅŌŹĒOHC-CH£ØCH3£©2ÉĻĮ¬ÓŠ-OH£¬»ņ½«ŃõŌ×Ó²åŌŚĢ¼Į“ÖŠ¼äŠĪ³É-O-½į¹¹£¬ÕāŃłµÄ½į¹¹ÓŠ4ÖÖ£¬Ģ¼Į“½į¹¹·Ö±šĪŖOHC-CH£ØCH3£©-CH2-OH”¢OHC-CH£ØOH£©£ØCH3£©2”¢OHC-CH£ØCH3£©-O-CH3”¢OHC-O-CH£ØCH3£©2£¬ĖłŅŌ¹²ÓŠ10ÖÖ£¬
¹Ź“š°øĪŖ£ŗ10£®
µćĘĄ ±¾Ģāæ¼²éÓŠ»śĶʶĻ£¬Éę¼°Ļ©Ģž”¢“¼”¢Č©”¢ōČĖįµČŠŌÖŹŅŌ¼°Ń§ÉśĶĘĄķÄÜĮ¦µČ£¬ŹĒ¶ŌÓŠ»ś»ÆŗĻĪļÖŖŹ¶µÄ×ŪŗĻ漲飬ÄܽĻŗƵÄæ¼²éæ¼ÉśµÄĖ¼Ī¬ÄÜĮ¦£¬øł¾ŻŅŅĻ©ÓėDµÄ·Ö×ÓŹ½£¬½įŗĻEÓėŅŅĖį·“Ӧɜ³ÉF£¬ø÷·Ö×ÓÖŠCŌ×ÓŹżÄ棬Ŋ¶ĻDµÄ½į¹¹ŹĒ½āĢāµÄ¹Ų¼ü£¬ÄѶČÖŠµČ£¬ŹĒøßæ¼ČȵćĢāŠĶ£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
 £®
£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
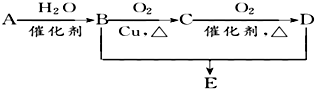 ÓŠ»śĪļAµÄ½į¹¹¼ņŹ½ĪŖCH2=CH2£¬æÉ·¢ÉśŅŌĻĀĻµĮŠ×Ŗ»Æ£¬ŅŃÖŖB”¢DŹĒÉś»īÖŠ³£¼ūµÄĮ½ÖÖÓŠ»śĪļ£¬DµÄĖ®ČÜŅŗ³ŹĖįŠŌ£¬BÓėDµÄ·“Ó¦ĪŖõ„»Æ·“Ó¦£®ĻĀĮŠĖµ·Ø²»ÕżČ·µÄŹĒ£Ø””””£©
ÓŠ»śĪļAµÄ½į¹¹¼ņŹ½ĪŖCH2=CH2£¬æÉ·¢ÉśŅŌĻĀĻµĮŠ×Ŗ»Æ£¬ŅŃÖŖB”¢DŹĒÉś»īÖŠ³£¼ūµÄĮ½ÖÖÓŠ»śĪļ£¬DµÄĖ®ČÜŅŗ³ŹĖįŠŌ£¬BÓėDµÄ·“Ó¦ĪŖõ„»Æ·“Ó¦£®ĻĀĮŠĖµ·Ø²»ÕżČ·µÄŹĒ£Ø””””£©| A£® | ÓÉB”¢DÖʱøE³£ÓĆÅØH2SO4×÷ĶŃĖ®¼Į | |
| B£® | D”¢E¶¼ÄÜÓėNaOHČÜŅŗ·“Ó¦ | |
| C£® | E”¢D”¢BČżÖÖĪļÖŹæÉŅŌÓƱ„ŗĶNa2CO3ČÜŅŗ¼ų±š | |
| D£® | 75%µÄBČÜŅŗ³£ÓĆÓŚŅ½ĮĘĻū¶¾ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 2.3g½šŹōÄĘÓė¹żĮæµÄŃõĘų·“Ó¦£¬ĪŽĀŪ¼ÓČČÓė·ń×ŖŅʵē×ÓŹż¾łĪŖ0.1NA | |
| B£® | 1molNa2CO3¾§ĢåÖŠŗ¬CO32-Ąė×ÓŹżŠ”ÓŚNA | |
| C£® | ¶čŠŌµē¼«µē½āŹ³ŃĪĖ®£¬ČōĻßĀ·ÖŠĶعżNAµē×ÓµēĮ棬ŌņŃō¼«²śÉśĘųĢå11.2L | |
| D£® | 0.1molCaO2£Ø¹żŃõ»ÆøĘ£©ÖŠŗ¬ŅõĄė×ÓŹżŹĒ0.2NA |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Į× | B£® | Ģś | C£® | µā | D£® | øĘ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ¼ĘĖćĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 25”ę£¬pH=13µÄNaOHČÜŅŗÖŠŗ¬ÓŠOH-ĪŖ0.1NA | |
| B£® | 1 L 0.1 mol•L-1 CuSO4ČÜŅŗÖŠŗ¬ÓŠCu2+ĪŖ0.1NA | |
| C£® | 2.24 L N2ŗĶNH3»ģŗĻĘųĢåÖŠŌ×Ó¼äŗ¬ÓŠµÄ¹²ÓƵē×Ó¶ŌŹżÄæĪŖ0.3NA | |
| D£® | 2 mol SO2ŗĶ1 mol O2ŌŚŅ»¶ØĢõ¼žĻĀ³ä·Ö·“Ó¦ŗó£¬ĖłµĆ»ģŗĻĘųĢåµÄ·Ö×ÓŹż“óÓŚ2NA |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Ō×ÓŹżÄæĻąµČµÄČżÖÖĘųĢå£¬ÖŹĮæ×ī“óµÄŹĒZ | |
| B£® | ĻąĶ¬Ģõ¼žĻĀ£¬Ķ¬ÖŹĮæµÄ¶žÖÖĘųĢ壬ĘųĢåĆܶČ×īŠ”µÄŹĒX | |
| C£® | ČōŅ»¶ØĢõ¼žĻĀ£¬ČżÖÖĘųĢåĢå»ż¾łĪŖ2.24 L£¬ŌņĖüĆĒµÄĪļÖŹµÄĮæŅ»¶Ø¾łĪŖ0.1mol | |
| D£® | Ķ¬ĪĀĻĀ£¬Ģå»żĻąĶ¬µÄĮ½ČŻĘ÷·Ö±š³ä2 g YĘųĢåŗĶl g ZĘųĢ壬ŌņĘäŃ¹Ēæ±ČĪŖ2£ŗ1 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
 æ“ČēĶ¼Ķź³ÉĻĀĆęµÄĢīæÕ£¬Š“³öµē¼«·“Ó¦Ź½ŗĶ×Ü·“Ó¦Ź½£®
æ“ČēĶ¼Ķź³ÉĻĀĆęµÄĢīæÕ£¬Š“³öµē¼«·“Ó¦Ź½ŗĶ×Ü·“Ó¦Ź½£®²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com