
| 强电解质 | 弱电解质 | 酸性氧化物 | 碱性氧化物 | |
| A | H2SO4 | CH3COOH | NO2 | Na2O |
| B | BaSO4 | HClO | Mn2O7 | CaO |
| C | NaCl | 氨水 | SO2 | MnO2 |
| D | HI | HF | CO2 | Fe3O4 |
| A. | A | B. | B | C. | C | D. | D |
分析 在水溶液中能完全电离为强电解质;
在水溶液中不能完全电离为弱电解质;
能和碱反应生成盐和水的氧化物为酸性氧化物;
能和酸反应生成盐和水的氧化物为碱性氧化物.据此分析.
解答 解:A、NO2和碱反应除了生成盐和水,还生成NO,故不是酸性氧化物,故A错误;
B、BaSO4在水溶液中能完全电离,故为强电解质;HClO在水溶液中不能完全电离,故为弱电解质;Mn2O7能和碱反应生成盐和水的氧化物,故为酸性氧化物;CaO能和酸反应生成盐和水的氧化物,故为碱性氧化物,故B正确;
C、氨水为混合物,故不是电解质;MnO2不能和酸反应生成盐和水,故不是碱性氧化物,故C错误;
D、Fe3O4和酸反应生成两种盐和水,故不是碱性氧化物,故D错误.
故选B.
点评 本题考查了强弱电解质、酸性氧化物碱性氧化物的概念,难度不大,应注意的是强弱电解质的本质区别是能否完全电离.


科目:高中化学 来源: 题型:解答题
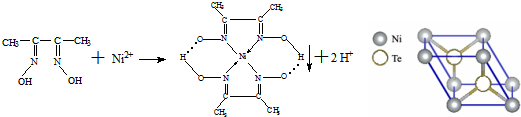
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
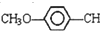 =CHCOOCH2CH2CH(CH3)2合成路线如下:
=CHCOOCH2CH2CH(CH3)2合成路线如下: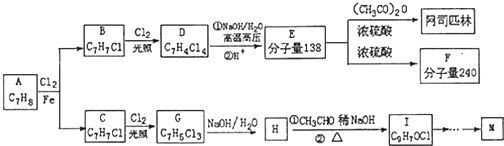
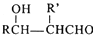 $\stackrel{△}{→}$RCH═
$\stackrel{△}{→}$RCH═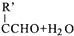
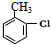 ,H→I两步反应的反应类型加成反应、消去反应
,H→I两步反应的反应类型加成反应、消去反应
 任意1种.
任意1种.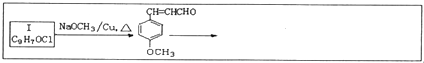
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
.| 0.01mol/LKIO3酸性溶液 (含淀粉)的体积/mL | 0.01mol/L Na2SO3溶液 的体积/mL | H2O 的体积 /mL | 实验温 度/℃ | 溶液出现 蓝色时所 需时间/s | |
| 实验1 | 5 | V1 | 35 | 25 | |
| 实验2 | 5 | 5 | 40 | 25 | |
| 实验3 | 5 | 5 | V2 | 0 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1:3 | B. | 1:7 | C. | 1:6 | D. | 5:3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,11.2 L乙醇所含分子数为0.5NA | |
| B. | 40 g氢氧化钠含有氧原子数为NA | |
| C. | 1mol任何纯净物都含有6.02×1023个原子 | |
| D. | 标准状况下,22.4 L氢气含有NA个氢原子 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2:7 | B. | 7:2 | C. | 2:1 | D. | 1:2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 跟金属钠反应 | |
| B. | 在足量氧气中完全燃烧生成CO2和H2O | |
| C. | 在浓硫酸存在时和乙酸发生酯化反应,生成乙酸乙酯和水 | |
| D. | 当银或铜存在时跟O2发生反应,生成乙醛和水 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
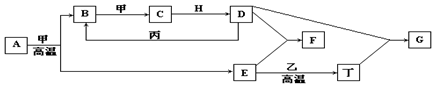
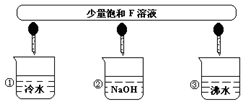
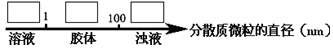
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com