
| A. | Cl | B. | O | C. | Mg | D. | Na |
分析 元素的原子核外最外层电子数决定元素最高化合价,最外层电子数越多,化合价越大,根据最外层电子数判断最高化合价,一般主族元素最高正化合价等于其最外层电子数,而F元素没有最高正化合价,稀有气体化合价一般为0价,O的最高化合价为+2价.
解答 解:A.Cl的最外层电子数为7,最高化合价为+7价,
B.O的最外层电子数为6,但最高化合价为+2价,如OF2中的氧元素;
C.Mg的最外层电子数为6,最高化合价为+2价;
D.Na的最外层电子数为1,最高化合价为+1价;
则化合价最高的为Cl,
故选A.
点评 本题考查化合价的判断,题目难度不大,本题注意根据元素在周期表中的位置可判断最外层电子数,根据最外层电子数判断化合价,注意F元素没有最高正化合价,O的最高化合价为+2价.


 全能测控期末小状元系列答案
全能测控期末小状元系列答案科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 在电解质溶液的导电性装置(如图所示)中,若向某一电解质溶液中逐滴加入另一溶液,则灯泡由亮变暗至熄灭,后又逐渐变亮的是( )
在电解质溶液的导电性装置(如图所示)中,若向某一电解质溶液中逐滴加入另一溶液,则灯泡由亮变暗至熄灭,后又逐渐变亮的是( )| A. | 盐酸中逐滴加入食盐溶液 | B. | 硫酸中逐滴加入NaOH溶液 | ||
| C. | 硫酸中逐滴加入Ba(OH)2溶液 | D. | 硫酸铜溶液中逐滴加入NaOH溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②③ | B. | ①③⑤ | C. | ②③⑤ | D. | ②④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
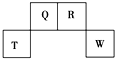 短周期元素Q、R、T、W在元素周期表中的位置如图所示,其中,T所处的周期序数与主族序数相等.请回答下列问题:
短周期元素Q、R、T、W在元素周期表中的位置如图所示,其中,T所处的周期序数与主族序数相等.请回答下列问题: .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 ,D元素位于周期表中的位置第三周期第ⅤⅡA族.
,D元素位于周期表中的位置第三周期第ⅤⅡA族.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 实验步骤 | 实验现象 | 结论 |
1向盛放溶液的试管中加入足量HNO3. | 有气泡产生 | 证明有CO32-. |
2继续向试管中加入足量Ba(NO3)2溶液 | 有白色沉淀生成 | 证明有SO42-. |
3过滤,向滤液中加适量的AgNO3溶液 | 有白色沉淀生成 | 证明有Cl-. |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
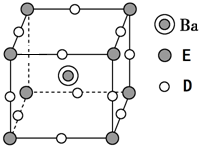 有原子序数依次增大的A、B、C、D、E、F、G 七种元素,A 是短周期中族序数等于周期数的非金属元素;B 元素的原子既不易失去也不易得到电子,其基态原子中每种能级电子数相同;D 的最外层电子数与电子层数之比为3:1;E是地壳中含量第二多的非金属元素;D、F同族; G 元素原子序数为24.
有原子序数依次增大的A、B、C、D、E、F、G 七种元素,A 是短周期中族序数等于周期数的非金属元素;B 元素的原子既不易失去也不易得到电子,其基态原子中每种能级电子数相同;D 的最外层电子数与电子层数之比为3:1;E是地壳中含量第二多的非金属元素;D、F同族; G 元素原子序数为24.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子晶体中的各相邻原子都以共价键相结合 | |
| B. | 金属导电的原因是在外电场作用下金属产生自由电子,电子定向运动 | |
| C. | 分子晶体的熔沸点很低,常温下都呈液态或气态 | |
| D. | 离子晶体中每个离子周围均吸引着6个带相反电荷的离子 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com