
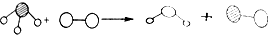 如图是两种气体发生反应的微观示意图,下列从示意图中获取的信息正确的是( )
如图是两种气体发生反应的微观示意图,下列从示意图中获取的信息正确的是( )

 名牌学校分层周周测系列答案
名牌学校分层周周测系列答案 黄冈海淀全程培优测试卷系列答案
黄冈海淀全程培优测试卷系列答案科目:高中化学 来源: 题型:
| Y | |||
| R | Q |
| ||
| ||

查看答案和解析>>
科目:高中化学 来源: 题型:
| 温度(℃) | 20 | 30 | 40 | 50 | 60 | 70 | 80 |
| 铜的平均溶解速率 (×10-3mol-L-1?min-1) |
7.34 | 8.01 | 9.25 | 7.98 | 7.24 | 6.73 | 5.76 |
查看答案和解析>>
科目:高中化学 来源:江西省(南昌一中、十中、新建二中)2006-2007学年度高三年级第一学期三校联考、化学试题 题型:022
| |||||||||||||||||||||||||||||
查看答案和解析>>
科目:高中化学 来源: 题型:
 在完全满足可逆反应:2H2O(g)
在完全满足可逆反应:2H2O(g) ![]() 2H2+O2,2CO+O2
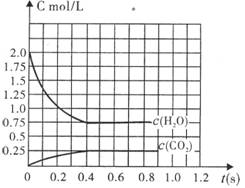
2H2+O2,2CO+O2 ![]() 2CO2能顺利进行的条件下,将2molH2O(g)和2molCO充入l L密闭容器中,使其发生反应,一段时间后反应达到平衡。反应过程中部分气体浓度随时间t的变化情况如下图所示:
2CO2能顺利进行的条件下,将2molH2O(g)和2molCO充入l L密闭容器中,使其发生反应,一段时间后反应达到平衡。反应过程中部分气体浓度随时间t的变化情况如下图所示:
(1)请在图中画出c(H2)随时间t的变化曲线图;
(2)平衡时c(O2)平为 mol/L。
(3)欲计算出平衡时O2的浓度,除已知“H2O(g)
和CO”的物质的量外,至少需要知道平衡体
系中某两种气体的平衡浓度。这两种气体除
可以是H2O和CO2外还可以是 。
(4)在其它条件不变的情况下,若改为起始时在
 容器中充入2molH2和2molCO2,则上述两反
容器中充入2molH2和2molCO2,则上述两反
应达到平衡时,c(O2)平= mol/L。
查看答案和解析>>
科目:高中化学 来源: 题型:
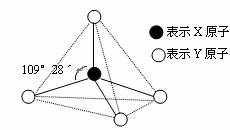
甲、乙、丙、戊都具有如图所示的结构或结构单元,图中正四面体以外可能有的部分未画出,虚线不表示化学键或分子间作用力,X、Y可以相同也可以不同。已知:
甲、乙是同一类晶体中的各自结构单元,单质甲能与乙发生置换反应,丙、丁、戊三种粒子含有等量的电子数,其中丙、丁是同一类晶体中的分子或分子集团,常温下丁呈液态,能产生两种等电子数的粒子,戊是阳离子。
(1)写出液态丁产生两种等电子粒子的电离方程式:
(2)室温下含有戊的盐溶液,其pH 。
A.>7 B.=7 C.<7 D.以上都有可能
(3)丙是目前重要的能源
①丙和丁在催化、加热条件下得到可燃性的两种气体,其反应的化学方程式是
②现代高能电池中,常用丙作燃料电池的原料,在碱性介质(KOH溶液)的情况下,其正极反应的电极方程式为
(4)甲、乙高温反应时,甲被破坏了1 mol共价键,则参加反应的乙为 g。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com