

| 第一次滴定 | 第二次滴定 | 第三次滴定 | |
| 消耗标准盐酸的体积(mL) | 24.98 | 25.00 | 25.02 |
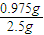 ×100%=39%,
×100%=39%,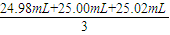 =25.00mL,根据反应NaOH+HCl=NaCl+H2O可知n(NaOH)=n(HCl)=0.02500L×0.2550mol?L-1×
=25.00mL,根据反应NaOH+HCl=NaCl+H2O可知n(NaOH)=n(HCl)=0.02500L×0.2550mol?L-1×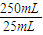 =0.06375mol,令样品中氢氧化钠的物质的量为xmol,过氧化钠为ymol,根据二者质量之和与消耗HCl的物质的量有40x+78y=2.5,x+2y=0.06375,联立解得x=0.01375,y=0.025,所以过氧化钠的质量为0.025mol×78g/mol=1.95g,样品中过氧化钠的纯度为
=0.06375mol,令样品中氢氧化钠的物质的量为xmol,过氧化钠为ymol,根据二者质量之和与消耗HCl的物质的量有40x+78y=2.5,x+2y=0.06375,联立解得x=0.01375,y=0.025,所以过氧化钠的质量为0.025mol×78g/mol=1.95g,样品中过氧化钠的纯度为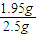 ×100%=78%,
×100%=78%,

科目:高中化学 来源: 题型:阅读理解
| 第一次滴定 | 第二次滴定 | 第三次滴定 | |
| 消耗标准盐酸的体积(mL) | 24.98 | 25.00 | 25.02 |
查看答案和解析>>
科目:高中化学 来源:杭州二模 题型:填空题

| 第一次滴定 | 第二次滴定 | 第三次滴定 | |
| 消耗标准盐酸的体积(mL) | 24.98 | 25.00 | 25.02 |
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
现有一定量含有NaOH杂质的Na2O2试样5.00 g,分成等质量两份,用两种方法测定Na2O2试样的纯度。请填写下列空白:
(1)第一种方法:取第一份试样,从下图中选用适当的实验装置,设计一个实验以测定过氧化钠的纯度(可供选用的反应物只有CaCO3固体、MnO2固体、6 mol·L-1盐酸和蒸馏水).

 ①若实验要求装置尽可能简单,应选用上图中的装置是(只要求写出图中装置的标号) 。
①若实验要求装置尽可能简单,应选用上图中的装置是(只要求写出图中装置的标号) 。
②所选用装置的连接顺序应是(填各接口的字母;连接胶管略). 。
③若实验过程中共产生氧气140 mL(已折算成标准状况),则试样中过氧化钠的纯度为 。
(2)第二种方法:取第二份试样,配成250.00 mL溶液,用0.255 0 mol·L-1的标准盐酸滴定。
① 取上述所配溶液25.00 mL于锥形瓶中,操作如下图所示(手持部分省略):正确的操作是图 ,
取溶液所用仪器的名称是 。
② 滴定操作平行实验的数据记录如下表:
|
| 第一次滴定 | 第二次滴定 | 第三次滴定 |
| 消耗标准盐酸的体积(mL) | 24.98 | 25.00 | 25.02 |
由表中数据计算样品中Na2O2纯度为 。
(3)若上述两个实验中不存在重大的操作失误,测得的实验数据也是真实可靠的,但以上两种方法测得的Na2O2纯度数据误差较大。
① 你认为上述两种方法中,哪种方法更为可靠 ?
② 产生较大实验误差的原因最可能是 。
③ 在题中所给出的仪器和药品范围内,如何用简单的方法加以改进,使实验误差大为减少,写出改进的方法 。
查看答案和解析>>
科目:高中化学 来源:2010年浙江省杭州二模 题型:实验题
现有一定量含有NaOH杂质的Na2O2试样5.00 g,分成等质量两份,用两种方法测定Na2O2试样的纯度。请填写下列空白:
(1)第一种方法:取第一份试样,从下图中选用适当的实验装置,设计一个实验以测定过氧化钠的纯度(可供选用的反应物只有CaCO3固体、MnO2固体、6 mol·L-1盐酸和蒸馏水).
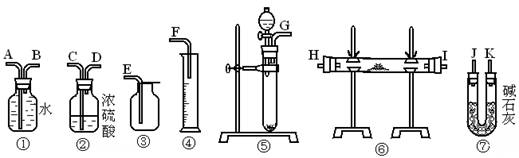
 ①若实验要求装置尽可能简单,应选用上图中的装置是(只要求写出图中装置的标号) 。
①若实验要求装置尽可能简单,应选用上图中的装置是(只要求写出图中装置的标号) 。
②所选用装置的连接顺序应是(填各接口的字母;连接胶管略). 。
③若实验过程中共产生氧气140 mL(已折算成标准状况),则试样中过氧化钠的纯度为 。
(2)第二种方法:取第二份试样,配成250.00 mL溶液,用0.255 0 mol·L-1的标准盐酸滴定。
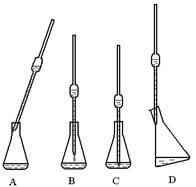
① 取上述所配溶液25.00 mL于锥形瓶中,操作如下图所示(手持部分省略):正确的操作是图 ,
取溶液所用仪器的名称是 。
② 滴定操作平行实验的数据记录如下表:
|
|
第一次滴定 |
第二次滴定 |
第三次滴定 |
|
消耗标准盐酸的体积(mL) |
24.98 |
25.00 |
25.02 |
由表中数据计算样品中Na2O2纯度为 。
(3)若上述两个实验中不存在重大的操作失误,测得的实验数据也是真实可靠的,但以上两种方法测得的Na2O2纯度数据误差较大。
① 你认为上述两种方法中,哪种方法更为可靠 ?
② 产生较大实验误差的原因最可能是 。
③ 在题中所给出的仪器和药品范围内,如何用简单的方法加以改进,使实验误差大为减少,写出改进的方法 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com