
金属铜与金属锰及其化合物在工业上有着广泛的应用:
(1)Cu2+的外围电子排布图可表示为_______________________________________;
(2)Mn基态原子核外处在能量最高的能级上的电子共有________种不同的运动状态;
(3)在铜锰氧化物的催化下,空气中CO被氧化成CO2,HCHO被氧化成CO2和H2O
① N3-和CO2是等电子体,则N3-的结构式为_________________________________;
② HCHO分子中C原子轨道的杂化类型为___________________________________;
(4)向CuSO4溶液中加入过量NaOH溶液可生成[Cu(OH)4]2-。不考虑空间构型,[Cu(OH) 4]2-的结构可用示意图表示为______________________________;
(5) 用晶体的x射线衍射法可以测得阿伏加德罗常数。对金属铜的测定得到以下结果:晶胞为面心立方最密堆积,边长为361pm(提示:3.613=47.05),又知铜的密度为9.00g·cm-3,则铜晶胞的质量是________________________g(保留两位小数);阿伏加德罗常数为_____________________________________(列式计算,保留两位小数)。
【知识点】物质结构、原子核外电子排布、晶胞计算
【答案解析】 (1)①(2分) (2)5(2分)
| | | | | |
3d
(3)①[N=N=N]- (2分) ②sp2 (2分)
(4) 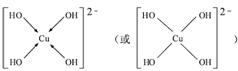 (2分)
(2分)
(5) 4.23×10-22g(2分) M(Cu)=64g/mol=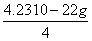 ×NA, NA=6.05×1023mol-1(3分)
×NA, NA=6.05×1023mol-1(3分)
| | | | | |
| 3d |
解析:(1)Cu2+是铜原子失去4S上1个电子和3d上1个电子,外围为3d9外围电子排布图可表示为
(2)Mn基态原子核外处在能量最高的能级上的电子为3d有5个电子,所以有5种不同的运动状态。
(3)① N3-和CO2是等电子体,CO2是直线型分子,所以N3-离子也是直线型,得其结构式为[N=N=N]- ② HCHO分子中C原子形成3个σ键,杂化轨道数为3,则杂化类型为sp2
(4)铜原子和4个羟基形成4个配位键,得
(5)1pm=10-10cm,故一个晶胞的体积为(361×10-10cm)3=4.7×10-23cm3;晶胞的质量=体积×密度,故一个晶胞的质量为4.7×10-23cm3×9.00g•cm-3=4.23×10-22g。金属铜晶胞为面心立方最密堆积则每个晶胞含有4个铜原子,铜的摩尔质量=1/4×晶胞质量×NA,所以64g•mol-1=1/4×4.23×10-22g×NA,得NA=6.05×1023mol-1。
【思路点拨】本题考查了物质结构原子结构、等电子体、杂化轨道有关知识,难度不大。


科目:高中化学 来源: 题型:
某课外兴趣小组测定某品牌牛奶中钙的含量,方法如下:取100mL牛奶,加入足量的草酸铵[(NH4)2C2O4]溶液,使牛奶中的钙转化成难溶的CaC2O4沉淀;过滤,用适量的蒸馏水洗涤沉淀表面吸附的少量(NH4)2C2O4、蛋白质等杂质;将沉淀转移至锥形瓶中,加足量的稀硫酸溶液溶解CaC2O4;然后以0.10mol・L-1的KMnO4溶液滴定生成的H2C2O4溶液,共消耗12.00mLKMnO4溶液。发生的反应为:
5H2C2O4+2KMnO4+3H2SO4 = 5CO2↑+2MnSO4+K2SO4+8H2O
(1)KMnO4溶液应盛在_________(填“酸式”或“碱式”)滴定管中。
(2)若滴定管的规格为25mL,滴定前滴定管中液面的读数为5.20 mL,则滴定管中液体的体积为______(填代号)。
A.5.20 mL B.19.80 mL C.大于19.80 mL D.小于19.80 mL
(3)本实验是否需要外加指示剂? (填“是”或者“否”)。如何判断滴定终点
(4)滴定时边滴边摇动锥形瓶,眼睛应观察
(5)该牛奶中钙的含量为_________mg/100mL。
(6)下列操作会使实验结果偏低的是____________(填代号)。
A.滴定管未用KMnO4溶液润洗就直接盛装KMnO4溶液
B.向锥形瓶转移沉淀时,损失部分沉淀
C.开始时平视读数,滴定完成时俯视读数
D.CaC2O4的表面没有洗涤干净,吸附少量C2O42-等杂质
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)某酯的分子式为C6H12O2,其变化如图所示:
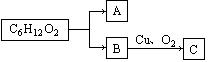
若A能发生银镜反应,C不能发生银镜反应,则该酯的可能结构有 种。
(2)将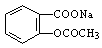 转变为
转变为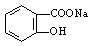 的流程为
的流程为
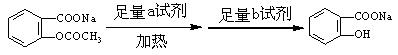
则a试剂是 ,b试剂是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
已知X、Y元素同周期,且电负性X>Y,下列说法错误的是 ( )
A X与Y形成化合物是,X可以显负价,Y显正价
B 第一电离能可能Y大于X
C 最高价含氧酸的酸性:X对应的酸性弱于于Y对应的
D 气态氢化物的稳定性:HmY小于HnX
查看答案和解析>>
科目:高中化学 来源: 题型:
下表为长式周期表的一部分,其中的序号代表对应的元素。
| ① |
| ||||||||||||||||
|
| ② |
| ③ | ④ | ⑤ | ⑥ |
| ||||||||||
|
| ⑦ |
| ⑧ |
|
|
|
| ||||||||||
|
|
|
|
|
| ⑨ |
|
|
|
| ⑩ |
|
|
|
|
|
|
|
(1)写出上表中元素⑤的轨道表示式_______,元素⑨原子的核外电子排布式__________。
(2)元素第一电离能的大小比较:④_____⑤(填写“>”“=”或“<”,下同);元素电负性的大小比较:④_____⑤(填写“>”“=”或“<”);请写出与元素④的单质互为等电子体的一种微粒的化学式_________。
(3)在测定元素①与⑥形成化合物的相对分子质量时,实验测得的值一般高于理论值的主要原因是__________。
(4)上述③与④元素组成的(CN)2化合物中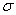 键与
键与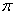 键之比________。
键之比________。
(5)⑦的氧化物是优良的耐高温材料,它的熔点比 CaO高,其原因是_____________。
(6)元素⑩的某种氧化物的晶体结构如图所示,其中实心球表示元素⑩原子,则该氧化物的化学式________。
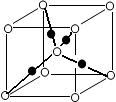
查看答案和解析>>
科目:高中化学 来源: 题型:
X、Y、Z、Q、M为常见的短周期元素,其原子序数依次增大。有关信息如下表:
| X | 动植物生长不可缺少的元素,是蛋白质的重要成分 |
| Y | 地壳中含量居第一位 |
| Z | 短周期中其原子半径最大 |
| Q | 生活中大量使用其合金制品,工业上可用电解其氧化物的方法制备 |
| M | 海水中大量富集的元素之一,其最高正化合价与负价的代数和为6 |
(1)X的气态氢化物的大量生产曾经解决了地球上因粮食不足而导致的饥饿和死亡问题,请写出该气态氢化物的电子式____________。
(2)已知37Rb和53I都位于第五周期,分别与Z和M同一主族。下列有关说法正确的是____________(填序号)。
A.原子半径: Rb>I B.RbM中含有共价键
C.气态氢化物热稳定性:M>I
D.Rb、Q、M的最高价氧化物对应的水化物可以两两发生反应
⑶若XM3最初水解产物是XH3和HMO,则X、M元素的电负性大小顺序是:X_____M((填>、<、或=);若已知磷与M元素电负性关系是:P<M,则PM3水解的化学反应方程式是 。
(4)已知QM3的熔点为190℃(2.02×105Pa),但它在180℃即开始升华,则QM3是_________(填“离子化合物”或“共价化合物”),如何通过实验判别__________________。在500K和1.01×105Pa时,它的蒸气密度(换算成标准状况时)为11.92g/L,则QM3的结构式为_________。
(5)X、Y组成的一种无色气体遇空气变为红棕色。将标准状况下40 L该无色气体与15 L氧气通入一定浓度的NaOH溶液中,恰好被完全吸收,同时生成两种盐。请写出该反应的离子方程式 。
查看答案和解析>>
科目:高中化学 来源: 题型:
洋中有丰富的食品、矿产、能源、药物和水产资源等(如下图所示)。

下列有关说法不正确的是
A .从能量转换角度来看,框图中的氯碱工业是一个将电能转化为化学能量的过程
.从能量转换角度来看,框图中的氯碱工业是一个将电能转化为化学能量的过程
B.过程②中结晶出的MgCl2·6H2O要在HCl氛围中加热脱水制得无水MgCl2
C.在过程③⑤中溴元素均被氧化
D.过程①中除去粗盐中的SO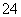 、Ca2+、Mg2+、Fe3+等杂质,加入的药品顺序为:Na2CO3溶液→NaOH溶液→BaCl2溶液→过滤后加盐酸
、Ca2+、Mg2+、Fe3+等杂质,加入的药品顺序为:Na2CO3溶液→NaOH溶液→BaCl2溶液→过滤后加盐酸
查看答案和解析>>
科目:高中化学 来源: 题型:
已知还原性 I— > Fe2+ > Br—,在只含有I—、Fe2+、Br—溶液中通入一定量的氯气,关于所得溶液离子成分分析正确的是(不考虑Br2 、I2和水的反应)( )
A.I—、Fe3+ 、Cl— B.Fe2+、Cl—、Br‑ C.Fe2+、Fe3+ 、Cl— D.Fe2+、I— 、Cl—
查看答案和解析>>
科目:高中化学 来源: 题型:
化学与生产、生活密切相关。下列叙述错误的是
A.光导纤维和陶瓷都是硅酸盐产品
B.晶体硅可用于制造芯片
C.钢铁厂用热还原法冶炼铁
D.焙制糕点的发酵粉主要成分之一是碳酸氢钠
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com