
 �̲��ں��ġ���ȼ�����Ǹ�ѹ���γɵ��������ļ���ˮ������壮��������ѧ��֪ʶ�ش��������⣺
�̲��ں��ġ���ȼ�����Ǹ�ѹ���γɵ��������ļ���ˮ������壮��������ѧ��֪ʶ�ش��������⣺���� ��1��C���������Ӳ㣬�����4�����ӣ�������Ԫ�����ڱ��е�λ��Ϊ�ڶ����ڣ��ڢ�A�壻
��2��̼�ж���ͬ�������壬C60�����ľ�������Ϊ���Ӿ��壬���ʯ�ۻ�ʱ�ƻ����������ǹ��ۼ�����ͼ��֪����C�����ʯ��+O2��g��=CO2��g����H1=-395.4kj/mol����C��ʯī��+O2��g��=CO2��g����H1=-393.5kj/mol�����ݸ�˹���ɢ�-�ٵã�C��ʯī��s��=C�����ʯ��s������H=-1.9kj/mol��
��3��4s����������ʾ�ķ�Ӧ����Ϊ0.3mol•L-1•s-1��������Ũ�ȱ仯��Ϊ��1.2mol/L���ɷ�Ӧ����ʽ��CH4+H2O=CO+3H2�������Ũ��Ϊ0.4mol/L������4sʱʣ��ļ����Ũ��Ϊ$\frac{2mol}{2L}$-0.4mol/L=0.6mol/L���ɴ˷������
��� �⣺��1��C���������Ӳ㣬�����4�����ӣ�������Ԫ�����ڱ��е�λ��Ϊ�ڶ����ڣ��ڢ�A�壬�ʴ�Ϊ���ڶ����ڣ��ڢ�A�壻
��2��̼�ж���ͬ�������壬C60�����ľ�������Ϊ���Ӿ��壬���ʯ�ۻ�ʱ�ƻ����������ǹ��ۼ�����ͼ��֪����C�����ʯ��+O2��g��=CO2��g����H1=-395.4kj/mol����C��ʯī��+O2��g��=CO2��g����H1=-393.5kj/mol�����ݸ�˹���ɢ�-�ٵã�C��ʯī��s��=C�����ʯ��s������H=1.9kj/mol���������Ľ��ʯ��ʯī��ȫȼ�ս��ʯ�ų��������࣬�ʴ�Ϊ�����Ӿ��壻���ۼ������ʯ��C��ʯī��s��=C�����ʯ��s������H=1.9kj/mol��
��3��4s����������ʾ�ķ�Ӧ����Ϊ0.3mol•L-1•s-1��������Ũ�ȱ仯��Ϊ��1.2mol/L���ɷ�Ӧ����ʽ��CH4+H2O=CO+3H2�������Ũ��Ϊ0.4mol/L������4sʱʣ��ļ����Ũ��Ϊ$\frac{2mol}{2L}$-0.4mol/L=0.6mol/L���ʴ�Ϊ��0.6mol/L��
���� ���⿼��Ԫ����Ԫ�����ڱ��е�λ�á���˹���ɡ������ı仯�Լ���ѧ��Ӧ���йؼ��㣬�ۺ��Խ�ǿ����һ�����Ѷȣ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | M��X��A��E | B�� | A��M��X��E | C�� | M��X��E��A | D�� | E��A��M |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | H2��I2��HI��Ũ����� | |
| B�� | ��������ܶȺ㶨���� | |
| C�� | ���������������ٸı� | |
| D�� | 1��I-I�����ѵ�ͬʱ����2��H-I������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �ڳ��³�ѹ�£�11.2L O2�к��е�ԭ����ΪNA | |
| B�� | �ڳ��³�ѹ�£�44g CO2�к��е�ԭ����Ϊ3NA | |
| C�� | �ڳ��³�ѹ�£�NA��ˮ���ӵ����ԼΪ22.4L | |
| D�� | �ڳ��³�ѹ�£�11.2L�������еĵ�����Ϊ2NA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | v��D��=0.4 mol/��L•min�� | B�� | v��B��=0.6 mol/��L•min�� | ||
| C�� | v��C��=0.35 mol/��L•min�� | D�� | v��A��=0.5 mol/��L•min�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���������ǵ���ɫ���壬�����ڿ����б�ɰ�ɫ���������ƹ��� | |
| B�� | �����������������ӱ���Ϊ1��2 | |
| C�� | �ù�������Ư��֯���ѵ��վ�����ɻ�ɫ | |
| D�� | Na2O��Na2O2���ܺ�ˮ��Ӧ���ɼ���Ƕ��Ǽ��������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��ƶ���

 ��F�����к��еĺ����������������ǻ����Ȼ���˳����Եߵ�����
��F�����к��еĺ����������������ǻ����Ȼ���˳����Եߵ����� ��
��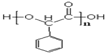 ��
�� �ĺϳ���·��H2C=CHCH2CH3$\stackrel{HBrO}{��}$HOCH2CHBrCH2CH3��CH3CH2CHBrCOOH$\stackrel{NaOH��aq����}{��}$CH3CH2CHOHCOOH��
�ĺϳ���·��H2C=CHCH2CH3$\stackrel{HBrO}{��}$HOCH2CHBrCH2CH3��CH3CH2CHBrCOOH$\stackrel{NaOH��aq����}{��}$CH3CH2CHOHCOOH���鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com