
·ÖĪö £Ø1£©øł¾Żc=$\frac{1000¦Ń¦Ų}{M}$¼ĘĖćŃĪĖįµÄĪļÖŹµÄĮæÅØ¶Č£»
£Ø2£©øł¾Żn=$\frac{m}{M}$¼ĘĖćKMnO4µÄĪļÖŹµÄĮ棬øł¾Ż·½³ĢŹ½¼ĘĖć²Ī¼Ó·“Ó¦µÄHCl£¬±»Ńõ»ÆµÄHClÉś³ÉĀČĘų£¬øł¾ŻĀČŌ×ÓŹĒ¼ĘĖć±»Ńõ»ÆHClĪļÖŹµÄĮ棻
£Ø3£©øł¾ŻV=nVm¼ĘĖćÉś³ÉĀČĘųµÄĢå»ż£®
½ā“š ½ā£ŗ£Ø1£©ÓÉc=$\frac{1000¦Ń¦Ų}{M}$æÉÖŖ£¬ĆܶČĪŖ1.19g/cm3£¬ČÜÖŹÖŹĮæ·ÖŹżĪŖ36.5%µÄŃĪĖįµÄĪļÖŹµÄĮæÅضČĪŖ$\frac{1000”Į1.19”Į36.5%}{36.5}$mol/L=11.9mol/L£¬
“š£ŗøĆŃĪĖįµÄĪļÖŹµÄĮæÅضČĪŖ11.9mol/L£»
£Ø2£©15.8g KMnO4µÄĪļÖŹµÄĮæĪŖ$\frac{15.8g}{158g/mol}$=0.1mol£¬øł¾Ż2KMnO4+16HClØT2KCl+2MnCl2+5Cl2”ü+8H2O£¬æÉÖŖ²Ī¼Ó·“Ó¦µÄHClĪŖn£ØHCl£©=8n£ØKMnO4£©=0.8mol£¬Ōņm£ØHCl£©=0.8mol”Į36.5g/mol=29.2g£»
n£ØCl2£©=$\frac{5}{2}$n£ØKMnO4£©=0.1mol”Į$\frac{5}{2}$=0.25mol£¬±»Ńõ»ÆµÄHClÉś³ÉĀČĘų£¬øł¾ŻĀČŌ×ÓæÉÖŖ£¬±»Ńõ»ÆHClĪļÖŹµÄĮæĪŖ0.25mol”Į2=0.5mol£¬ĖłŅŌ±»Ńõ»ÆHClµÄÖŹĮæĪŖ0.5mol”Į36.5g/mol=18.25g£»
“š£ŗ15.8g KMnO4ÄÜŹ¹29.2æĖHCl·¢ÉśÉĻŹö·“Ó¦£»18.25æĖHCl±»Ńõ»Æ£»
£Ø3£©ŌŚ±źæöĻĀÉś³ÉĀČĘųµÄĢå»żĪŖ0.25mol”Į22.4L/mol=5.6L£¬
“š£ŗCl2ŌŚ±ź×¼×“æöĻĀµÄĢå»żĪŖ5.6L£®
µćĘĄ ±¾Ģāæ¼²éĪļÖŹµÄĮæÅØ¶Č¼ĘĖć”¢»Æѧ·½³ĢŹ½¼ĘĖć£¬ÄŃ¶Č²»“ó£¬×¢Ņā¶Ō»ł“”ÖŖŹ¶µÄĄķ½āÕĘĪÕ£®


 ĘŚÄ©³å“Ģ100·Ö““ŠĀ½š¾ķĶźČ«ŹŌ¾ķĻµĮŠ“š°ø
ĘŚÄ©³å“Ģ100·Ö““ŠĀ½š¾ķĶźČ«ŹŌ¾ķĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
 £»ĒėŠ“³öøĆ·“Ó¦µÄŅ»øöÖŲŅŖÓĆĶ¾£ŗŗø½ÓøÖ¹ģ£®
£»ĒėŠ“³öøĆ·“Ó¦µÄŅ»øöÖŲŅŖÓĆĶ¾£ŗŗø½ÓøÖ¹ģ£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā

²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
 ČēĶ¼ŹĒŹµŃéŹŅÓĆŅŅ“¼ÓėÅØĮņĖįŗĶäå»ÆÄĘ·“Ó¦Ą“ÖʱøäåŅŅĶéµÄ×°ÖĆ£¬·“Ó¦ŠčŅŖ¼ÓČČ£¬Ķ¼ÖŠŹ”Č„ĮĖ¼ÓČČ×°ÖĆ£®ÓŠ¹ŲŹż¾Ż¼ūĻĀ±ķ£ŗ
ČēĶ¼ŹĒŹµŃéŹŅÓĆŅŅ“¼ÓėÅØĮņĖįŗĶäå»ÆÄĘ·“Ó¦Ą“ÖʱøäåŅŅĶéµÄ×°ÖĆ£¬·“Ó¦ŠčŅŖ¼ÓČČ£¬Ķ¼ÖŠŹ”Č„ĮĖ¼ÓČČ×°ÖĆ£®ÓŠ¹ŲŹż¾Ż¼ūĻĀ±ķ£ŗ| ŅŅ“¼ | äåŅŅĶé | äå | |
| דĢ¬ | ĪŽÉ«ŅŗĢå | ĪŽÉ«ŅŗĢå | Éīŗģ×ŲÉ«ŅŗĢå |
| ĆܶČ/g•cm-3 | 0.79 | 1.44 | 3.1 |
| ·Šµć/”ę | 78.5 | 38.4 | 59 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ½«Ņ»ŹųĒæ¹āĶعżµķ·ŪČÜŅŗ£¬Ņ²ÄܲśÉś¶”“ļ¶ūŠ§Ó¦ | |
| B£® | ŌŚČÜÓŠ1 mol Fe£ØOH£©3µÄ½ŗĢåÖŠ£¬Ō¼ŗ¬6.02”Į1023øöFe£ØOH£©3½ŗĮ£ | |
| C£® | Ņ»Ö¦øÖ±ŹŹ¹ÓĆĮ½ÖÖ²»Ķ¬ŠĶŗÅµÄĄ¶ŗŚÄ«Ė®£¬Ņ׳öĻÖ¶ĀČū | |
| D£® | ”°Óźŗó²Źŗē”±”°ŗ£ŹŠņ×Ā„”±¼ČŹĒŅ»ÖÖ×ŌČ»ĻÖĻóÓÖŹĒ¹āѧĻÖĻó£¬Ņ²Óė½ŗĢåµÄŠŌÖŹÓŠ¹Ų |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
| ŹµŃé·½·Ø | ŹµŃéĻÖĻó | ½įĀŪ |
| ŌŚČÜŅŗÖŠ¼ÓČėKSCNČÜŅŗ | ČÜŅŗ±äŗģÉ« | ¹ĢĢåĪļÖŹÖŠÓŠFeCl3 |
| ŌŚĖįŠŌKMnO4ČÜŅŗÖŠ¼ÓČėÉŁĮæA | KMnO4ČÜŅŗŃÕÉ«ĪŽĆ÷ĻŌ±ä»Æ | ¹ĢĢåĪļÖŹÖŠ²»ŗ¬FeCl2 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | C3H8 | B£® | C7H8O | C£® | CH4O | D£® | CH2Cl2 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
| ×°ÖĆĶ¼ | ĖłŹ¢ŹŌ¼Į | ŹµŃéĻÖĻó | |
| 1 | 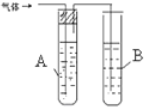 | AŹĒ Ė® BŹĒ ĖįŠŌøßĆĢĖį¼ŲČÜŅŗ | |
| 2 |  | CŹĒ äåµÄĖÄĀČ»ÆĢ¼ČÜŅŗ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com