

分析 (1)莫尔盐[(NH4)2Fe(SO4)2•6H2O]受热分解,分解时会产生氨气和二氧化硫、三氧化硫等酸性气体,根据装置图可知,碱石灰可以吸收酸性气体,氨气遇到酚酞溶液会变红色,A中绿色粉末逐渐变成红色粉末是亚铁氧化物变化为氧化铁,依据铁离子遇到硫氰酸钾溶液变红色设计验证;
(2)①要检验生成SO3(g)、SO2(g)及N2,在甲组实验中的装置A产生气体后,经过安全瓶后通过氯化钡溶液检验SO3,再通过品红溶液检验SO2,用浓氢氧化钠除去二氧化硫,用排水集气法收集氮气;
②由于产生的气体中有氨气,所以氯化钡溶液中加入足量的盐酸,可以吸收氨气并防止产生亚硫酸钡沉淀,排除SO2的干扰,SO3通入氯化钡溶液中可以产生硫酸钡沉淀,二氧化硫能使品红褪色;
(3)(NH4)2Fe(SO4)2分解生成红色粉末、SO2、N2、NH3和H2O,没有SO3生成,依据原子守恒配平书写化学方程式.
解答 解:(1)①莫尔盐[(NH4)2Fe(SO4)2•6H2O]受热分解,分解时会产生氨气和二氧化硫、三氧化硫等酸性气体,根据装置图可知,碱石灰可以吸收酸性气体,氨气遇到酚酞溶液会变红色,所以装置C 中可观察到的现象是溶液变红,由此可知莫尔盐晶体分解的产物中有 NH3,
故答案为:NH3;
②装置B的主要作用是 吸收分解产生的酸性气体,
故答案为:吸收分解产生的酸性气体;
③A中绿色粉末逐渐变成红色粉末是分解生成的亚铁氧化物变化为氧化铁,检验该红色粉末需要加入盐酸溶解得到溶液,在溶液中滴入KSCN溶液,溶液呈血红色,证明是氧化铁,
故答案为:HCl,KSCN;
(2)①要检验生成SO3(g)、SO2(g)及N2,在甲组实验中的装置A产生气体后,经过安全瓶后通过氯化钡溶液检验SO3,再通过品红溶液检验SO2,用浓氢氧化钠除去二氧化硫,用排水集气法收集氮气,所以装置依次连接的合理顺序为A、G、D、B、C、F,
故答案为:G、D、B、C、F;
②由于产生的气体中有氨气,所以氯化钡溶液中加入足量的盐酸,可以吸收氨气并防止产生亚硫酸钡沉淀,排除SO2的干扰,SO3通入氯化钡溶液中可以产生硫酸钡沉淀,二氧化硫能使品红褪色,所以装置D中足量盐酸的作用是 吸收氨气并将溶液酸化,排除SO2的干扰;含有SO3的实验现象是 D中有白色沉淀;含有SO2的实验现象是B中品红褪色,
故答案为:吸收氨气并将溶液酸化,排除SO2的干扰;D中有白色沉淀;B中品红褪色;
(3)(NH4)2Fe(SO4)2分解生成红色粉末为氧化铁、SO2、N2、NH3和H2O,没有SO3生成,反应的化学方程式为:2(NH4)2Fe(SO4)2$\frac{\underline{\;\;△\;\;}}{\;}$Fe2O3+N2+4SO2+2NH3+5H2O,
故答案为:2(NH4)2Fe(SO4)2$\frac{\underline{\;\;△\;\;}}{\;}$Fe2O3+N2+4SO2+2NH3+5H2O.
点评 本题考查性质实验方案设计,侧重考查学生知识综合应用、实验基本操作能力及实验方案设计能力,综合性较强,难点是排列实验先后顺序,根据实验目的及物质的性质进行排列顺序,注意要排除其它因素干扰,难度中等.


科目:高中化学 来源: 题型:选择题
| A. | 乙烷(乙烯):催化剂和H2,加热 | B. | 苯(苯酚):氢氧化钠溶液,分液 | ||
| C. | CO2(SO2):饱和碳酸钠溶液,洗气 | D. | 溴苯(溴):苯和铁粉,过滤 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
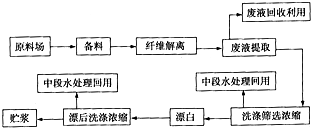
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
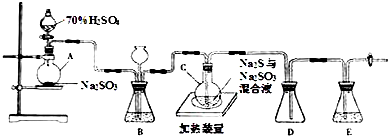
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
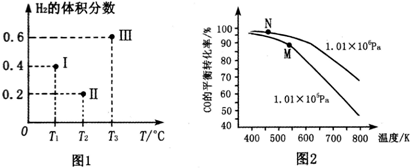
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| NaOH溶液 | 银氨溶液 | 新制Cu(OH)2 悬浊液 | 金属钠 | |
| X | 中和反应 | 无现象 | 溶解 | 产生氢气 |
| Y | 无现象 | 有银镜 | 加热后有砖红色沉淀 | 产生氢气 |
| Z | 水解反应 | 有银镜 | 加热后有砖红色沉淀 | 无现象 |
| W | 水解反应 | 无现象 | 无现象 | 无现象 |
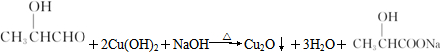 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用A表示的反应速率是0.4mol/(L•min) | |
| B. | 分别用B、C、D表示反应的速率,其比值是3:2:1 | |
| C. | 若在恒容时充入与反应无关的气体Ar,由于增大了容器内的压强,而加快了反应速率 | |
| D. | 当B的消耗速率与C的消耗速率相等时,反应达到了平衡 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
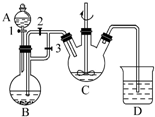 某化学兴趣小组用FeCl2(用铁粉与盐酸反应制得)和NH4HCO3制备FeCO3的装置示意图如图所示.回答下列问题:
某化学兴趣小组用FeCl2(用铁粉与盐酸反应制得)和NH4HCO3制备FeCO3的装置示意图如图所示.回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com