
化学实验有助于理解化学知识,形成化学观念,提高探究与创新能力,提升科学素养。
(1)在实验室中用浓盐酸与MnO2共热制取Cl2并进行相关实验。写出制取Cl2的离子方程式 ;某小组要从该混合物中回收MnO2并提取MnCl2晶体,则要多次用到的玻璃仪器是 。
(2)下图A~G都是常见的与气体制备、收集、尾气吸收有关的装置。例如,B、C都可以收集H2、CH4、NH3、Cl2等。如果收集Cl2并进行尾气处理,不能选用 ;如用B收集Cl2,应该从 (甲、乙)端进气。
(3)工业常用Cl2从海水中制备Br2,反应离子方程式是 。实验室模拟该实验,分离出Br2的操作是:取混合溶液于分液漏斗中,加入CCl4,振荡 ,
静置分层, 。
(4)次氯酸盐有强氧化性,如NaClO 可以氧化NH3制备高能燃料N2H4,反应方程式是:
。现有14.9g NaClO 最多可以制备 mol N2H4.








A B C D E F G
科目:高中化学 来源: 题型:
某同学为探究元素周期表中元素性质的递变规律,设计了如下系列实验。
Ⅰ.验证同周期主族元素非金属性的变化规律
(1)将钠、镁、铝各1 mol分别投入到足量的同浓度的盐酸中,试预测实验结果:______与盐酸反应最剧烈,______与盐酸反应的速率最慢;______与盐酸反应产生的气体最多。
(2)向Na2S溶液中通入氯气出现黄色浑浊,可证明Cl的非金属性比S强,反应的离子方程式为________________。
Ⅱ.利用下图装置验证同主族元素非金属性的变化规律
(3)仪器B的名称为________,干燥管D的作用为防止________。
(4)若要证明非金属性:Cl>I,则A中加浓盐酸,B中加KMnO4(KMnO4与浓盐酸常温下反应生成氯气),C中加淀粉碘化钾混合溶液,观察到C中溶液________的现象,即可证明。从环境保护的观点考虑,此装置缺少尾气处理装置,可用________溶液吸收尾气。
(5)若要证明非金属性:C>Si,则在A中加盐酸、B中加CaCO3、C中加Na2SiO3溶液观察到C中溶液________的现象,即可证明。但有的同学认为盐酸具有挥发性,可进入C中干扰实验,应在两装置间添加装有________溶液的洗气瓶除去。
 |
查看答案和解析>>
科目:高中化学 来源: 题型:
某研究小组进行Mg(OH)2沉淀溶解和生成的实验探究。
向2支盛有1 mL 1 mol·L-1 的MgCl2溶液中各加入10滴2 mol·L-1 NaOH,制得等量Mg(OH)2沉淀;然后分别向其中加入不同试剂,记录实验现象如下表:
| 实验序号 | 加入试剂 | 实验现象 |
| Ⅰ | 4 mL 2 mol·L-1 HCl 溶液 | 沉淀溶解 |
| Ⅱ | 4 mL 2 mol·L-1 NH4Cl 溶液 | 沉淀溶解 |
(1)从沉淀溶解平衡的角度解释实验Ⅰ的反应过程 。
(2)测得实验Ⅱ中所用NH4Cl溶液显酸性(pH约为4.5),用离子方程式解释其显酸性的原因 。
(3)甲同学认为应补充一个实验:向同样的Mg(OH)2沉淀中加4 mL蒸馏水,观察到沉淀不溶解。该实验的目的是 。
(4)同学们猜测实验Ⅱ中沉淀溶解的原因有两种:一是NH4Cl溶液显酸性,溶液中的H+可以结合OH- ,进而使沉淀溶解;二是 。
(5)乙同学继续进行实验:向4 mL 2 mol·L-1 NH4Cl溶液中滴加2滴浓氨水,得到pH约为8的混合溶液,向同样的Mg(OH)2沉淀中加入该混合溶液,观察现象。
①实验结果证明(4)中的第二种猜测是成立的,乙同学获得的实验现象是 。
③乙同学这样配制混合溶液的理由是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
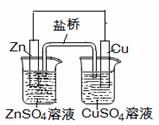 下列叙述正确的是
下列叙述正确的是
A.电镀时,通常把待镀的金属制品作阴极
B.氢氧燃料电池(酸性电解质)中O2通入负极
C.右图中电子由Cu极流向Zn,盐桥中的Cl–
移向CuSO4溶液
D.在海轮外壳镶嵌锌块保护外壳不受腐蚀是采用了
牺牲阳极的阴极保护法
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各组物质之间的化学反应,反应产物一定为纯净物的是
A.CH3—CH===CH2+H2O B.CH2===CH—CH2—CH3+HCl
B.CH2===CH—CH2—CH3+HCl
C.CH3—CH===CH—CH3+Br2(CCl4)→ D.CH3CH3+Cl2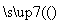
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是
A.相对分子质量相同,组成元素也相同的化合物一定是同分异构体
B.凡是分子组成相差一个或若干个CH2原子团的物质,彼此一定是同系物
C.两种物质组成元素相同,各元素的质量分数也相同,则二者一定是同分异构体
D.各组成元素的质量分数都相同且分子式也相同的不同有机物一定互为同分异构体
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于硅的说法,不正确的是
A.硅是非金属元素,它的单质是灰黑色有金属光泽的固体
B.硅的导电性能介于金属和绝缘体之间,是良好的半导体材料
C.硅的化学性质不活泼,常温下不与任何物质反应
D.加热到一定温度时硅能与H2、O2等非金属反应
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法中,正确的是
A.酸性高锰酸钾溶液具有强的氧化性,配制时用盐酸酸化
B.用25.00 mL碱式滴定管量取20.00 mL酸性高锰酸钾溶液
C.将KI溶液滴入酸性KMnO4溶液中,溶液的紫色能褪去
D.将SO2通入酸性高锰酸钾溶液,溶液紫色褪去,是SO2漂白性的表现
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com