
 子交换膜只允许阴离子通过,电极为惰性电极)
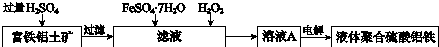
子交换膜只允许阴离子通过,电极为惰性电极)分析 铝土矿(含Al2O3及少量SiO2和FeO、Fe2O3),加入过量稀硫酸酸溶过滤,滤液为硫酸铝、硫酸亚铁、硫酸铁,滤渣为二氧化硅和不溶性杂质,滤液中加入绿矾晶体补充亚铁离子并利用过氧化氢氧化为铁离子,最后利用电解原理得到液体聚全硫酸铝铁,据此分解解题;
(1)氧化铝是两性氧化物溶于强酸强碱,与硫酸反应生成硫酸铝和水;
(2)滤液中$\frac{c(A{l}^{3+})}{c(F{e}^{3+})}$>1,新型净水剂液体聚合硫酸铝铁[AlaFeb(OH)m(SO4)n],当a=b时净水效果最好,故需要增加溶液里Fe3+的浓度;
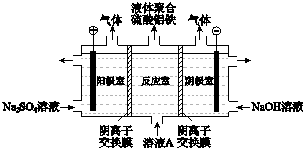
(3)①阴极上氢离子得电子生成氢气;
②电解过程中阳极发生氧化反应,水电离的OH-失电子被氧化为氧气,促进水的电离;
③阴离子交换膜只允许阴离子通过,则阴极室中的氢氧根离子进入反应室生成Alm(OH)nCl3m-n.
解答 解:(1)硫酸溶解氧化铝生成硫酸铝和水,反应的离子方程式为:Al2O3+6H+=2Al3++3H2O,故答案为:Al2O3+6H+=2Al3++3H2O;
(2)因滤液中$\frac{c(A{l}^{3+})}{c(F{e}^{3+})}$>1,加入绿矾晶体引入Fe2+,并利用过氧化氢氧化得到Fe3+,补充溶液里的Fe3+,使$\frac{c(A{l}^{3+})}{c(F{e}^{3+})}$=1,其中氧化Fe2+的离子反应式为2Fe2++H2O2+2H+=2Fe3++2H2O,故答案为:2Fe2++H2O2+2H+=2Fe3++2H2O,补充Fe3+;
(3)①阴极上氢离子得电子生成氢气,则阴极的电极反应式为:2H++2e-=H2↑;
故答案为:2H++2e-=H2↑;
②阳极上水电离的OH-被氧化,促进水的电离,阳极周围溶液里H+浓度增大,溶液的pH减小,故答案为:减小;
③阴离子交换膜只允许阴离子通过,电解过程中反应室中的氯离子通过阴离子交换膜进入阳极室,阴极室中的氢氧根离子进入反应室生成Alm(OH)nCl3m-n;
故答案为:电解过程中反应室中的SO42--通过阴离子交换膜进入阳极室,阴极室中的OH-通过阴离子交换膜进入反应室,生成聚合硫酸铝铁.
点评 本题是一道关于物质的分离和提纯知识的实验操作题,涉及基本实验操作、沉淀的生成、氧化还原反应、电解原理的应用等,侧重于考查学生分析和解决问题的能力,题目难度中等.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:选择题
| A. | 蛋白质是两性物质 | |
| B. | 蛋白质分子中的重要化学键是肽键(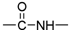 ) ) | |
| C. | 天然蛋白质水解的最终产物是α-氨基酸 | |
| D. | 蛋白质溶液中分别加入浓NaCl溶液、CuSO4溶液,其过程都是不可逆的 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
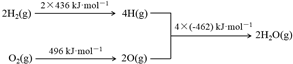
| A. | 1molC(s)完全燃烧放出110 kJ的热量 | |
| B. | H2(g)+$\frac{1}{2}$O2(g)═H2O(g)△H=-480 kJ•mol-1 | |
| C. | C(s)+H2O(g)═CO(g)+H2(g)△H=+130 kJ•mol-1 | |
| D. | 欲分解2 mol H2O(l),至少需要提供4×462 kJ的热量 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 实验编号 | 实验操作 | 实验现象 |
| ① | 滴入KSCN溶液 | 溶液变红色 |
| ② | 滴入AgNO3溶液 | 有黄色沉淀生成 |
| ③ | 滴入K3[Fe(CN)6]溶液 | 有蓝色沉淀生成 |
| ④ | 滴入淀粉溶液 | 溶液变蓝色 |
| A. | ①和② | B. | ②和④ | C. | ③和④ | D. | ①和③ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 使用前检查是否漏水 | B. | 溶液未冷却即注入容量瓶中 | ||
| C. | 容量瓶可长期存放溶液 | D. | 在容量瓶中直接溶解固体 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na+、Mg2+、SO42-、HCO3- | B. | Na+、Ba2+、Cl-、SO42- | ||
| C. | Cu2+、Ca2+、Cl-、NO3- | D. | Fe2+、K+、NO3-、Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氧化剂和还原剂混合不一定发生氧化还原反应 | |
| B. | 得电子越多的氧化剂,其氧化性就越强 | |
| C. | 阳离子只有氧化性,阴离子只有还原性 | |
| D. | 有单质参加且有单质生成的反应一定属于氧化还原反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 蔗糖与麦芽糖都具有还原性,水解产物都是葡萄糖 | |
| B. | 淀粉和纤维素互为同分异构体,水解产物都是葡萄糖 | |
| C. | 蛋白质在酶的作用下,水解为多肽,最终生成氨基酸 | |
| D. | 植物油和动物油都是高级脂肪酸甘油酯,前者的饱和程度更高 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com