
下列关于反应4NH3(g)+5O2(g)=4NO(g)+6H2O(g) △H= —1025kJ·mol-1描述不正确的是
A.该反应为放热反应
B.反应物的总能量大于生成物的总能量
C.该反应中每有4molNH3被氧化,放出1025kJ热量
D.该反应每形成6molH—O键,放出1025kJ热量
科目:高中化学 来源: 题型:
| 元素性质 | 元素编号 | |||||
| ① | ② | ③ | ④ | ⑤ | ⑥ | |
| 原子半径/nm | 0.102 | 0.110 | 0.074 | 0.075 | 0.071 | 0.099 |
| 最高化合价 | +6 | +5 | +5 | +7 | ||
| 最低化合价 | -2 | -3 | -2 | -3 | -1 | -1 |
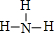
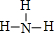
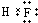
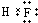
| ||
| △ |
| ||
| △ |
| ||
| 高温高压 |
| ||
| 高温高压 |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于反应4NH3(g)+5O2(g)=4NO(g)+6H2O(g)△H=—1025kJ·mol-1描述不正确的是
A.该反应为放热反应
B.反应物的总能量大于生成物的总能量
C.该反应中每有4molNH3被氧化,放出1025kJ热量
D.该反应每形成6molH—O键,放出1025kJ热量
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
查看答案和解析>>
科目:高中化学 来源:2011-2012学年江苏省新海高级中学高二下学期期中考试化学试卷(带解析) 题型:单选题
下列关于反应4NH3(g)+5O2(g)=4NO(g)+6H2O(g) △H= —1025kJ·mol-1描述不正确的是
| A.该反应为放热反应 |
| B.反应物的总能量大于生成物的总能量 |
| C.该反应中每有4molNH3被氧化,放出1025kJ热量 |
| D.该反应每形成6molH—O键,放出1025kJ热量 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com