
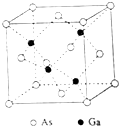
 砷化镓(GaAs)是优良的半导体材料,可用于制作微型激光器或太阳能电池的材料等.回答下列问题:
砷化镓(GaAs)是优良的半导体材料,可用于制作微型激光器或太阳能电池的材料等.回答下列问题:分析 (1)As原子核外有33个电子,根据构造原理书写As原子核外电子排布式;
(2)同一周期元素,原子半径随着原子序数增大而减小,元素第一电离能随着原子序数增大而呈增大趋势,但第IIA族、第VA族元素第一电离能大于其相邻元素;
(3)AsCl3分子中As原子价层电子对个数=3+$\frac{5-3×1}{2}$=4且含有一个孤电子对,根据价层电子对互斥理论判断该分子的立体构型及As原子杂化方式;
(4)离子晶体熔沸点较高、分子晶体熔沸点较低;
(5)该物质熔沸点较高,且原子之间以共价键结合形成空间网状结构,原子晶体具有该物质特点.
解答 解:(1)As原子核外有33个电子,根据构造原理书写As原子核外电子排布式为[Ar]3d104s24p3,故答案为:[Ar]3d104s24p3;
(2)同一周期元素,原子半径随着原子序数增大而减小,元素第一电离能随着原子序数增大而呈增大趋势,但第IIA族、第VA族元素第一电离能大于其相邻元素,Ga位于第IIIA族、As位于第VA族,且二者位于同一周期,所以原子半径Ga>As,第一电离能Ga<As,
故答案为:大于;小于;
(3)AsCl3分子中As原子价层电子对个数=3+$\frac{5-3×1}{2}$=4且含有一个孤电子对,根据价层电子对互斥理论判断该分子的立体构型为三角锥形,As原子杂化方式为sp3,
故答案为:三角锥形;sp3;
(4)离子晶体熔沸点较高、分子晶体熔沸点较低,GaF3为离子晶体,GaCl3为分子晶体,所以前者沸点高于后者,故答案为:GaF3为离子晶体,GaCl3为分子晶体;
(5)该物质熔沸点较高,且原子之间以共价键结合形成空间网状结构,原子晶体具有该物质特点,所以该物质是原子晶体,Ga和As以共价键结合,
故答案为:原子晶体;共价.
点评 本题考查物质结构和性质,为高频考点,涉及原子杂化方式判断、微粒空间构型判断、晶体类型判断、元素周期律等知识点,综合性较强,侧重考查学生判断及知识综合应用能力,易错点是孤电子对公式的计算方法,题目难度不大.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | ①② | B. | ②③④ | C. | ②③ | D. | ①③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 有害垃圾 | B. | 不可回收垃圾 | C. | 可回收垃圾 | D. | 可堆肥垃圾 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 22.4aVL | B. | $\frac{22.4aV}{(1-22.4a)}$ | ||
| C. | $\frac{22400aV}{(1000d-17a)L}$ | D. | $\frac{22400aV}{(1000d+17a)L}$ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
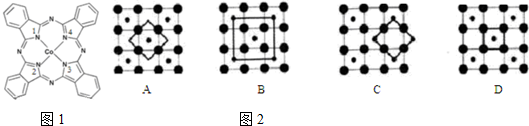
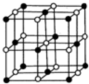 ),在该晶体中与一个钴原子等距离且最近的钴原子有12个;筑波材料科学国家实验室一个科研小组发现了在 5K 下呈现超导性的晶体,该晶体具有CoO2的层状结构(如2所示,小球表示Co原子,大球表示O原子).下列用粗线画出的重复结构单元示意图不能描述CoO2的化学组成的是D.
),在该晶体中与一个钴原子等距离且最近的钴原子有12个;筑波材料科学国家实验室一个科研小组发现了在 5K 下呈现超导性的晶体,该晶体具有CoO2的层状结构(如2所示,小球表示Co原子,大球表示O原子).下列用粗线画出的重复结构单元示意图不能描述CoO2的化学组成的是D.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 外界条件不能改变平衡状态 | B. | 达平衡时正、逆反应速率相等 | ||
| C. | 各组分的含量不随时间而变化 | D. | 是动态平衡 |
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 标准状况下,22.4L水所含有的原子数目为3NA | |
| B. | 标准状况下,22.4 L H2中含质子数为2NA | |
| C. | 0.1mol•L-1稀硫酸100mL中含有硫酸根个数为0.1NA | |
| D. | 0.1molOH-含NA个电子 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com