
A����֪һ���¶��£�������Һ�����ʵ���Ũ��Ϊc�������Ϊ����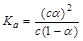 �����������������ƹ��壬��CH3COOH �����������������ƹ��壬��CH3COOH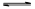 CH3COO����H�������ƶ�������С��Ka��С CH3COO����H�������ƶ�������С��Ka��С |
B�������£���Ӧ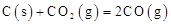 �����Է����У���÷�Ӧ�� �����Է����У���÷�Ӧ��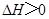 |
C��һ���¶��£��Ȼ��ˮ�����ӷ���ʽ��NH+4+H2O NH3��H2O+H+������KW��ʾ�����ӻ��� NH3��H2O+H+������KW��ʾ�����ӻ���Kb��ʾ��ˮ���볣�������Ȼ��ˮ��ƽ�ⳣ��K=KW/Kb |
| D��һ�֡��˹��̵������·������ڹ��������£�N2�ݴ���������ˮ����������Ӧ����NH3������,��֪�� |

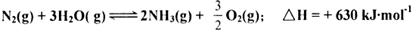

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
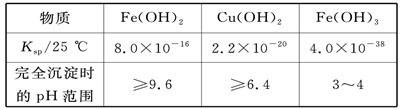
| A����û����Һ����μ���NaOH��Һ�����ȿ������ɫ���� |
| B�������Һ�м���������ˮ��������pH��3��4����ˣ��ɻ�ô�����CuSO4��Һ |
| C������Һ��c(SO)��[c(Cu2��)��c(Fe2��)��c(Fe3��)]>5��4 |
| D����pH��5����Һ��Fe3�����ܴ������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 ͼ4 ͼ5 ͼ6 ͼ7
ͼ4 ͼ5 ͼ6 ͼ7�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��

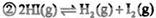
| A��9 | B��16 | C��20 | D��25 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
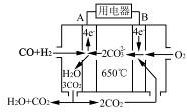
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A������ѹǿ������Ӱٷ������䣬��ѧ��Ӧ�������� |
| B�������¶ȣ�����Ӱٷ�������ѧ��Ӧ�������� |
| C�����뷴Ӧ�����Ӱٷ�������ѧ��Ӧ�������� |
| D��ʹ�ô���������Ӱٷ�������ѧ��Ӧ�������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
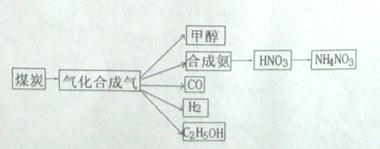
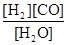 ��������Ӧ�Ļ�ѧ��ӦΪ��
��������Ӧ�Ļ�ѧ��ӦΪ�� 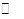 2C0(g)��K1 ����
2C0(g)��K1 ����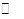 H2(g)+C02(g)��K2 �������� ��
H2(g)+C02(g)��K2 �������� ��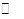 CO(g)+H2(g)��K3 ������������
CO(g)+H2(g)��K3 ������������ K1��K2��K3��֮��Ĺ�ϵ�ǣ�������������������Ӧ�ٵ�ƽ�ⳣ��K���¶ȵ����߶� ���� (����С������)��
K1��K2��K3��֮��Ĺ�ϵ�ǣ�������������������Ӧ�ٵ�ƽ�ⳣ��K���¶ȵ����߶� ���� (����С������)��
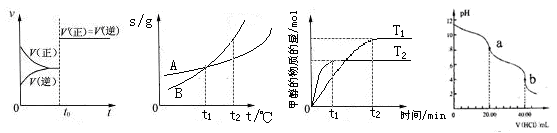
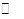 2N02(g) ��H>O�����¶�ΪT1��T2ʱ��ƽ����ϵ��N02�����������ѹǿ�仯������ͼ��ʾ������˵����ȷ����( )
2N02(g) ��H>O�����¶�ΪT1��T2ʱ��ƽ����ϵ��N02�����������ѹǿ�仯������ͼ��ʾ������˵����ȷ����( )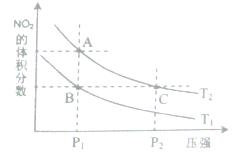
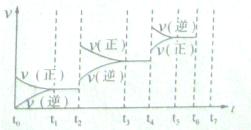
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
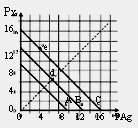
|
| A��A����AgCl��C����AgI | B��e���ʾ�ɹ�����KI��AgNO3��Ӧ����AgI���� |
| C��d������ˮ�м���������AgBr�γɵı�����Һ | |
| D��B��һ����AgBr |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com