
在宾馆、医院等公共场所,常常使用一种电离式烟雾报警器,其关键部件是一个放有镅﹣241( )放射源的电离室,
)放射源的电离室, 原子核内中子数与核外电子数之差是
原子核内中子数与核外电子数之差是
A.241 B.146 C.95 D.51
 走进文言文系列答案
走进文言文系列答案科目:高中化学 来源:2015-2016学年贵州凯里一中高一下期中理科化学试卷(解析版) 题型:选择题
关于如图所示装置的叙述错误的是( )

A.锌是负极,其质量逐渐减小
B.氢离子在铜表面被还原
C.电子从锌片经导线流向铜片
D.电流从锌片经导线流向铜片
查看答案和解析>>
科目:高中化学 来源:2015-2016学年山西大学附中高一下期中化学试卷(解析版) 题型:实验题
在锌与盐酸反应的实验中,某同学得到的结果如下表所示:
锌的质量/g | 锌的形状 | 温度/℃ | 锌完全溶解的时间/s | |
A | 2 | 薄片 | 5 | 400 |
B | 2 | 薄片 | 15 | 200 |
C | 2 | 薄片 | 25 | 100 |
D | 2 | 薄片 | 35 | t1 |
E | 2 | 颗粒 | 15 | t2 |
F | 2 | 粉末 | 15 | t3 |
G | 2 | 薄片(含少量杂质Cu) | 35 | t4 |
(1)反应的离子方程式是 ,该反应为 反应(填“放热”或“吸热”)。
(2)t1=________s, 完成下列时间对温 度的曲线图(纵轴表示时间,横轴表示温度)。
度的曲线图(纵轴表示时间,横轴表示温度)。
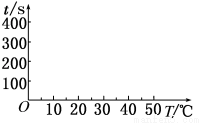
(3)利用所画的曲线图和相关数据,可得出该反应中温度影响反应速率的规律是__________。
(4)t1______(填“>”或“<”)t4,原因是________________________________。
t2________t3(填“>”或“<”),原因是_______________________________。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年山西大学附中高一下期中化学试卷(解析版) 题型:选择题
下列反应过程中,同时有离子键、极性共价键和非极性共价键的断裂和形成的反应是
A.H2+CuO===Cu+H2O
B.2Na2O2+2H2O===4NaOH+O2↑
C.H2+Cl2===2HCl
D.2NaOH+Cl2===NaCl+NaClO+H2O
查看答案和解析>>
科目:高中化学 来源:2015-2016学年山西大学附中高一下期中化学试卷(解析版) 题型:选择题
科学家预测原子序数为114的元素具有相当稳定的同位素,它的位置是 在第七周期、第ⅣA族,称为“类铅”,关于它的性质的预测错误的是
在第七周期、第ⅣA族,称为“类铅”,关于它的性质的预测错误的是
A.它的原子最外层有4个电子
B.它具有+2、+4价
C.金属铜能从114号元素的硝酸盐溶液中置换出该元素的单质
D.它的金属性比铅强
查看答案和解析>>
科目:高中化学 来源:2015-2016学年青海师大附二中高一下期中化学试卷(解析版) 题型:填空题
(1)铅蓄电池是典型的可充型电池,电池总反应式为:Pb+PbO2+4H++2SO42-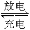 2PbSO4+2H2O。请回答下列问题(不考虑氢、氧的氧化还原):放电时,正极的电极反应式是____________;电解液中H2SO4的浓度将变________;当外电路通过1 mol电子时,理论上负极板的质量增加____g。
2PbSO4+2H2O。请回答下列问题(不考虑氢、氧的氧化还原):放电时,正极的电极反应式是____________;电解液中H2SO4的浓度将变________;当外电路通过1 mol电子时,理论上负极板的质量增加____g。
(2)微型纽扣电池在现代生活中有广泛应用。有一种银锌电池,其电极分别是Ag2O和Zn,电解质溶液为KOH溶液,电极反应为Zn+2OH--2e-===ZnO+H2O,Ag2O+H2O+2e-===2Ag+2OH-。

根据上述反应式,完成下列题目。
(1)下列叙述正确的是________。
A.在使用过程中,电解质KOH被不断消耗
B.使用过程中,电子由Ag2O极经外电路流向Zn极
C.Zn是负极,Ag2O是正极
D.Zn电极发生还原反应,Ag2O电极发生氧化反应
(2)写出电池的总反应式:___________________________________________________________。
(3)使用时,负极区的pH________(填“增大”“减小”或“不变”,下同),正极区的pH______,电解质溶液的pH________。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年青海师大附二中高一下期中化学试卷(解析版) 题型:选择题
镁及其化合物一般无毒(或低毒)、无污染,且镁原电池放电时电压高而平稳,使镁原电池越来越成为人们研制绿色原电池的关注焦点.其中一种镁原电池的反应为xMg+Mo3S4 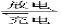 MgxMo3S4;在镁原电池放电时,下列说法错误的是( )
MgxMo3S4;在镁原电池放电时,下列说法错误的是( )
A.Mg2+向正极迁移 B.正极反应为:Mo3S4+2xe-===Mo3S42x-
C.Mo3S4发生氧化反应 D.负极反应为:xMg-2xe-===xMg2+
查看答案和解析>>
科目:高中化学 来源:2015-2016学年青海师大附二中高二下期中化学试卷(解析版) 题型:选择题
室温下向10mL0.1 mol·L-1NaOH溶液中加入0.1 mol·L-1的一元酸HA,溶液pH的变化曲线如图所示。下列说法正确的是
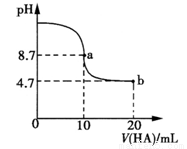
A.a点所示溶液中c(Na+)>c(A—)>c(H+)>c(HA)
B.a、b两点所示溶液中水的电离程度相同
C.pH=7时,c(Na+)= c(A—)+ c(HA)
D.b点所示溶液中c(A—)> c(HA)
查看答案和解析>>
科目:高中化学 来源:2015-2016学年江苏省高二下期中化学试卷(解析版) 题型:选择题
下列说法不正确的是
A.已知冰的熔化热为6.0 kJ/mol,冰中氢键键能为20 kJ/mol,假设1 mol冰中有2 mol 氢键,且熔化热完全用于破坏冰的氢键,则最多只能破坏冰中15%的氢键
B.对于CaCO3(s)===CaO(s)+CO2(g) 任何温度下都不能自发进行
C.实验测得环己烷(l)、环己烯(l)和苯(l)的标准燃烧热分别为-3916 kJ/mol、-3747 kJ/mol和-3265 kJ/mol,可以证明在苯分子中不存在独立的碳碳双键
D.已知:Fe2O3(s)+3C(石墨) 2Fe(s)+3CO(g),△H=+489.0 kJ/mol。
2Fe(s)+3CO(g),△H=+489.0 kJ/mol。
CO(g)+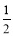 O2(g)
O2(g) CO2(g),△H=-283.0 kJ/mol。
CO2(g),△H=-283.0 kJ/mol。
C(石墨)+O2(g) CO2(g),△H=-393.5 kJ/mol。
CO2(g),△H=-393.5 kJ/mol。
则4Fe(s)+3O2(g) 2Fe2O3(s),△H=-1641.0 kJ/mol
2Fe2O3(s),△H=-1641.0 kJ/mol
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com