
用CCl4萃取溴水中的溴,下列说法不正确的是( )
A.实验使用的主要仪器是分液漏斗
B.溴在CCl4中的溶解度比在水中的溶解度大
C.溴的CCl4溶液呈橙红色
D.分液时,水从分液漏斗下口流出,溴的CCl4溶液从漏斗上口倒出
科目:高中化学 来源: 题型:
被称之为“软电池”的纸质电池总反应为Zn+2MnO2+H2O=ZnO+2MnOOH。下列说法正确的是 ( )
A.该电池中Zn作负极,发生还原反应
B.该电池反应中MnO2起催化作用
C.该电池工作时电流由Zn经导线流向MnO2
D.该电池正极反应式为:MnO2+e-+H2O=MnOOH+OH-
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)写出Na2CO3在水溶液中电离的电离方程式 。
(2)在3Cu + 8HNO3(稀) = 3Cu(NO3)2 + 2NO↑ + 4H2O的反应中,作为氧化剂的物质是 (填化学式);用双线桥法,标出该氧化还原反应的电子转移情况和数目。
(3)在一定条件下,RO3n- 和氯气可发生如下反应:
RO3n- + Cl2 + 2OH- = RO42- + 2Cl- +H2O 由以上反应可知RO3n-被 (填“氧化”或“还原”), RO3n-中元素R的化合价是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
把100 g某NaOH溶液,其密度是1.22 g/cm3,加热蒸发浓缩后,留下溶液50 mL时,其物质的量浓度是8 mol/L,原溶液的浓度是
A.160 g/L B.3.28 mol/L C.4.88 mol/L D.16%
查看答案和解析>>
科目:高中化学 来源: 题型:
现有两份溶液,一是质量分数24.5%,密度1.2g/mL的硫酸,二是200mL的混合溶液,其中H2SO4的浓度为0.5mol/L,Na2SO4的浓度为2.0mol/L,实验室需要浓度为1.0mol/LH2SO4,浓度为0.4mol/LNa2SO4的混合溶液,为配制所需溶液,回答下列问题:
(1)质量分数24.5%,密度1.2g/mL的硫酸浓度c(H2SO4)= mol/L
(2)原200mL的混合溶液中n(H2SO4)= mol n(Na2SO4)= mol
(3)为配制所需溶液,要质量分数24.5%,密度1.2g/mL的硫酸体积= mL.
(4)简述配制过程:①将200mL的混合溶液倒入大烧杯中,
②
③将烧杯中的溶液沿玻璃棒倒入 mL的容量瓶中,
④
⑤加水至离刻度线2-3cm处
⑥
以下略。
查看答案和解析>>
科目:高中化学 来源: 题型:
物质的量浓度相同的NaNO3、Mg(NO3)2、Al(NO3)3三种溶液,取三种溶液的体积比为3:2:1时,三种溶液中c(NO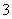 ) 之比为( )
) 之比为( )
A.1:1:1 B.1:2:3
C.3:2:1 D.3:4:3
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)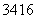 S2-中的质子数是________,中子数是________,核外电子数是________,质量数是________。
S2-中的质子数是________,中子数是________,核外电子数是________,质量数是________。
(2)Fe、Fe2+、Fe3+是________元素的三种粒子,它们的________数相同,它们所带的________数不相同。
(3)由1H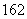 O与2H
O与2H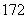 O所代表的物质中,共有________种元素,________种原子,互为同位素的原子有________________。
O所代表的物质中,共有________种元素,________种原子,互为同位素的原子有________________。
(4)已知元素X、Y的核电荷数分别为a和b,它们的离子Xm+和Yn-核外电子排布相同,则a、b、m、n之间的关系是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
单质X和Y相互反应生成X2+和Y2-,现有下列叙述:
(a)X被氧化 (b)X是氧化剂
(c)X具有氧化性 (d)Y2-是还原产物
(e)Y2-具有还原性 (f) X2+具有氧化性
其中正确的是( )
A.(a)(b)(c)(d) B.(b)(c)(d)
C.(a)(d)(e)(f) D.(a)(c)(d)(e)
查看答案和解析>>
科目:高中化学 来源: 题型:
某科学家利用二氧化铈(CeO2)在太阳能作用下将H2O、CO2转变为H2、CO。其过程如下:
mCeO2太阳能①(m-x)CeO2·xCe+xO2
(m-x)CeO2·xCe+xH2O+xCO2900 ℃②mCeO2+xH2+xCO
下列说法不正确的是( )
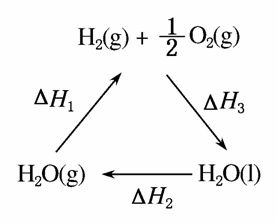
A.该过程中CeO2没有消耗
B.该过程实现了太阳能向化学能的转化
C.右图中ΔH1=ΔH2+ΔH3
D.以CO和O2构成的碱性燃料电池的负极反应式为CO+4OH--2e-===CO+2H2O
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com