
工业上用CO生产燃料甲醇。一定温度和容积条件下发生反应:CO(g)+2H2(g)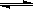 CH3OH(g)。图1表示反应中的能量变化;图2表示一定温度下,在体积为1L的密闭容器中加入2mol H2和一定量的CO后,CO和CH3OH(g)的浓度随时间变化。
CH3OH(g)。图1表示反应中的能量变化;图2表示一定温度下,在体积为1L的密闭容器中加入2mol H2和一定量的CO后,CO和CH3OH(g)的浓度随时间变化。
请回答下列问题:
(1)在“图1”中,曲线 (填“a”或“b”)表示使用了催化剂;没有使用催化剂时,在该温度和压强条件下反应CO(g)+2H2(g)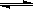 CH3OH(g)的△H = 。
CH3OH(g)的△H = 。
(2)从反应开始到建立平衡,v(CO)= ;该温度下CO(g)+2H2(g) 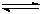 CH3OH(g)的化学平衡常数为 。达到平衡后若保持其它条件不变,将反应体系升温,则该反应化学平衡常数____(填“增大”、“减小”或“不变”)。
CH3OH(g)的化学平衡常数为 。达到平衡后若保持其它条件不变,将反应体系升温,则该反应化学平衡常数____(填“增大”、“减小”或“不变”)。
(3)已知CH3OH(g)+3/2O2(g)=CO2(g)+2H2O(g)ΔH=-193kJ/mol,又知H2O(l)= H2O(g) ΔH=+44 kJ/mol,请写出32g的CH3OH(g)完全燃烧生成液态水的热化学方程式 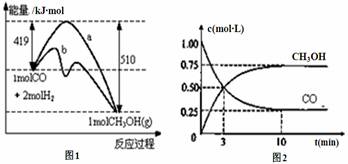 。
。
 同步练习强化拓展系列答案
同步练习强化拓展系列答案科目:高中化学 来源: 题型:
某课外兴趣小组欲测定某NaOH溶液的浓度,其操作步骤如下:
①将碱式滴定管用蒸馏水洗净后,用待测溶液润洗后,再注入待测溶液,调节滴定管的尖嘴部分充满溶液,并使液面处于"0"刻度以下的位置,记下读数;将锥形瓶用蒸馏水洗净后,用待测溶液润洗锥形瓶2~3次;从碱式滴定管中放入25.00mL待测溶液到锥形瓶中。
②将酸式滴定管用蒸馏水洗净后,立即向其中注入0.1000mol/L标准盐酸,调节滴定管的尖嘴部分充满溶液,并使液面处于"0"刻度以下的位置,记下读数。
③向锥形瓶中滴入酚酞作指示剂,进行滴定。 滴定至指示剂刚好变色,且并不马上变色为止,测得所耗盐酸的体积为V1mL。
④重复以上过程,但在滴定过程中向锥形瓶加入5mL的蒸馏水,测得所耗盐酸的体积为V2mL。试回答下列问题:
(1)锥形瓶中的溶液从 色变为 色时,停止滴定。
 (2)滴定时边滴边摇动锥形瓶,眼睛应观察
(2)滴定时边滴边摇动锥形瓶,眼睛应观察
A. 滴定管内液面的变化 B. 锥形瓶内溶液颜色的变化
(3)该小组在步骤①中的错误是
由此造成的测定结果 (偏高、偏低或无影响)
(4)步骤②缺少的操作是
(5)右图,是某次滴定时的滴定管中的液面,其读数为 mL
(6)根据下列数据:
| 滴定次数 | 待测液体积(mL) | 标准盐酸体积(mL) | |
| 滴定前读数(mL) | 滴定后读数(mL) | ||
| 第一次 | 25.00 | 0.50 | 20.40 |
| 第二次 | 25.00 | 4.00 | 24.10 |
请计算待测烧碱溶液的浓度: mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各式中,属于正确的电离方程式的是
A.HCO3- + H2O 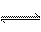 H2CO3 + OH- B.CH3COONa
H2CO3 + OH- B.CH3COONa CH3COO-+Na+
CH3COO-+Na+
C. Ca(OH)2  Ca2++2OH- D.NH3·H2O
Ca2++2OH- D.NH3·H2O  NH4+ + OH-
NH4+ + OH-
查看答案和解析>>
科目:高中化学 来源: 题型:
用4种溶液进行实验,下表中“操作及现象”与“溶液”对应关系错误的是( )
| 选项 | 操作及现象 | 溶液 |
| A | 向溶液中加入KSCN溶液,观察无明显现象,继续加入氯水,溶液变红色 | 含有Fe2+溶液 |
| B | 向溶液中加入盐酸,产生使澄清石灰水变浑浊的无色无味气体 | 含有CO32-溶液 |
| C | 通入CO2,溶液变浑浊。再加入品红溶液,红色褪去。 | 可能为Ca(ClO)2溶液 |
| D | 通入CO2,溶液变浑浊,继续通CO2至过量,浑浊消失,再加入足量NaOH溶液,又变浑浊。 | 可能为Ca(OH)2溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
如下图,向A中充入1molX、1molY,向B中充入2molX、2molY,起始时A、B的体积相等都等于a L,在相同温度和催化剂存在的条件下,关闭活塞K,使两容器中各自发生下述反
应,X(g)+Y(g) 2Z(g)+W(g);ΔH<0。A保持恒压,B保持恒容,达平衡时,A的体积为1.4aL。下列说法错误的是( )
2Z(g)+W(g);ΔH<0。A保持恒压,B保持恒容,达平衡时,A的体积为1.4aL。下列说法错误的是( )
A.反应速率:v(B)>v(A) B.A容器中X的转化率为80%
C.平衡时Y体积分数:A<B D.打开活塞K重新达平衡VA=2.2aL

查看答案和解析>>
科目:高中化学 来源: 题型:
氮化硅(Si3N4)是一种新型陶瓷材料,它可由石英与焦炭在高温的氮气流中,通过以下反应制得:3SiO2(s)+6C(s)+ 2N2(g) 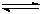 Si3N4(s) + 6CO(g)
Si3N4(s) + 6CO(g)
(1)该反应的氧化剂是 ,2molN2参加反应转移电子数为 。
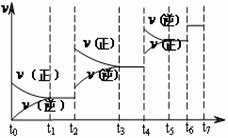
(2) 达到平衡后,改变某一外界条件(不改变N2、CO的量),反应速率v与时间t的关系如图。图中t4时引起平衡移动的条件可能是 ;图中表示平衡混合物中CO的含量最高的一段时间是 。
(3)若该反应的平衡常数为 K=729,则在同温度下1L密闭容器中,足量的SiO2和C与2mol N2充分反应,则N2的转化率是
(提示:272 = 729)
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述中正确的是( )
A.Al、Fe、Cu三者对应的氧化物均为碱性氧化物
B.向污水中投放明矾,能生成凝聚悬浮物的Al(OH)3胶体,起到净水的作用
C.向NaAlO2溶液中通入过量CO2:2AlO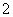 +CO2+3H2O===2Al(OH)3↓+CO
+CO2+3H2O===2Al(OH)3↓+CO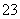
D.加入铝粉能产生H2的溶液中,一定存在大量的Na+、Ba2+、AlO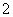 、Cl
、Cl
查看答案和解析>>
科目:高中化学 来源: 题型:
随着社会的发展,人们日益重视环境问题。下列做法或说法正确的是
A.提倡使用一次性发泡塑料餐具和塑料袋
B.绿色化学的核心是应用化学原理治理环境污染
C.推广以植物秸秆为原料的综合利用技术,避免焚烧秸秆造成空气污染
D.PM2.5是指大气中直径接近2.5×10-6m的颗粒物,分散在空气中形成胶体
查看答案和解析>>
科目:高中化学 来源: 题型:
已知95℃时,水的离子积常数为1×10-12。在此温度下,将pH=8的NaOH溶液与pH=4的H2SO4溶液相混合,得到pH=7的混合溶液,则NaOH溶液与H2SO4溶液的体积比为______︰______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com