
 ČēĶ¼ĖłŹ¾×Ŗ»Æ¹ŲĻµ£¬AĪŖµ„ÖŹ£¬ŹŌ¶ŌĻĀĮŠĒéæö½ųŠŠĶʶĻ£¬²¢»Ų“šĻĀĮŠĪŹĢā£ŗ
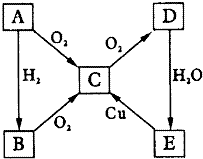
ČēĶ¼ĖłŹ¾×Ŗ»Æ¹ŲĻµ£¬AĪŖµ„ÖŹ£¬ŹŌ¶ŌĻĀĮŠĒéæö½ųŠŠĶʶĻ£¬²¢»Ų“šĻĀĮŠĪŹĢā£ŗ·ÖĪö AĪŖµ„ÖŹ£¬ÓÉ×Ŗ»Æ¹ŲĻµæÉÖŖ£¬BĪŖĒā»ÆĪļ£¬CĪŖŃõ»ÆĪļ£¬DĪŖŃõ»ÆĪļ£¬EĪŖĖį£¬ÖŠŃ§ÖŠN”¢SŌŖĖŲµ„ÖŹ»ÆŗĻĪļ·ūŗĻ×Ŗ»Æ¹ŲĻµ£®
£Ø1£©AĪŖ¹ĢĢ壬ŌņAĪŖS£¬BĪŖH2S£¬CĪŖSO2£¬DĪŖSO3£¬EĪŖH2SO4£»
£Ø2£©AĪŖĘųĢ壬ŌņAĪŖN2£¬BĪŖNH3£¬CĪŖNO£¬DĪŖNO2£¬EĪŖHNO3£®
½ā“š ½ā£ŗAĪŖµ„ÖŹ£¬ÓÉ×Ŗ»Æ¹ŲĻµæÉÖŖ£¬BĪŖĒā»ÆĪļ£¬CĪŖŃõ»ÆĪļ£¬DĪŖŃõ»ÆĪļ£¬EĪŖĖį£¬ÖŠŃ§ÖŠN”¢SŌŖĖŲµ„ÖŹ»ÆŗĻĪļ·ūŗĻ×Ŗ»Æ¹ŲĻµ£®
£Ø1£©AĪŖ¹ĢĢ壬ŌņAĪŖS£¬BĪŖH2S£¬CĪŖSO2£¬DĪŖSO3£¬EĪŖH2SO4£¬
¢ŁAµÄ»ÆѧŹ½ĪŖS£¬¹Ź“š°øĪŖ£ŗS£»
¢ŚÓÉCÉś³ÉDµÄ»Æѧ·½³ĢŹ½£ŗ2SO2+O2$\frac{\underline{“߻ƼĮ}}{”÷}$2SO3£¬¹Ź“š°øĪŖ£ŗ2SO2+O2$\frac{\underline{“߻ƼĮ}}{”÷}$2SO3£»
¢ŪÓÉEÉś³ÉCµÄ»Æѧ·½³ĢŹ½£ŗCu+2H2SO4£ØÅØ£©$\frac{\underline{\;\;”÷\;\;}}{\;}$CuSO4+SO2”ü+2H2O£¬¹Ź“š°øĪŖ£ŗCu+2H2SO4£ØÅØ£©$\frac{\underline{\;\;”÷\;\;}}{\;}$CuSO4+SO2”ü+2H2O£»
£Ø2£©AĪŖĘųĢ壬ŌņAĪŖN2£¬BĪŖNH3£¬CĪŖNO£¬DĪŖNO2£¬EĪŖHNO3£®
¢ŁAµÄ»ÆѧŹ½ĪŖ£ŗN2£¬¹Ź“š°øĪŖ£ŗN2£»
¢ŚÓÉBÉś³ÉCµÄ»Æѧ·½³ĢŹ½£ŗ4NH3+5O2$\frac{\underline{“߻ƼĮ}}{”÷}$4NO+6H2O£¬¹Ź“š°øĪŖ£ŗ4NH3+5O2$\frac{\underline{“߻ƼĮ}}{”÷}$4NO+6H2O£»
¢ŪÓÉDÉś³ÉEµÄĄė×Ó·½³ĢŹ½£ŗ3NO2+H2OØT2H++2NO3-+NO£¬¹Ź“š°øĪŖ£ŗ3NO2+H2OØT2H++2NO3-+NO£»
¢ÜÓÉEÉś³ÉCµÄĄė×Ó·½³ĢŹ½£ŗ3Cu+8H++2NO3-ØT3Cu2++2NO”ü+4H2O£¬¹Ź“š°øĪŖ£ŗ3Cu+8H++2NO3-ØT3Cu2++2NO”ü+4H2O£®
µćĘĄ ±¾Ģāæ¼²éĪŽ»śĪļµÄĶʶĻ£¬Éę¼°N”¢SŌŖĖŲµ„ÖŹ»ÆŗĻĪļŠŌÖŹ£¬×¢ŅāŹ¶¼Ē֊ѧ³£¼ūµÄĮ¬ŠųŃõ»Æ·“Ó¦£¬ŹģĮ·ÕĘĪÕŌŖĖŲ»ÆŗĻĪļŠŌÖŹ£¬±Č½Ļ»ł“”£®


 ÖŠæ¼½ā¶Įæ¼µć¾«Į·ĻµĮŠ“š°ø
ÖŠæ¼½ā¶Įæ¼µć¾«Į·ĻµĮŠ“š°ø ø÷µŲĘŚÄ©ø“Ļ°ĢŲѵ¾ķĻµĮŠ“š°ø
ø÷µŲĘŚÄ©ø“Ļ°ĢŲѵ¾ķĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ¶žŃõ»Æ¹čæÉÓĆÓŚÖĘŌģ¹āµ¼ĻĖĪ¬ | |
| B£® | ŹÆÓ¢²£Į§æÉÓĆÓŚÖĘŌģ¹āѧŅĒĘ÷ | |
| C£® | ²£Į§ŌŚ¼ÓČČČŚ»ÆŹ±ÓŠ¹Ģ¶ØµÄČŪµć | |
| D£® | ÖĘĘÕĶز£Į§µÄŌĮĻŹĒ“æ¼ī”¢ŹÆ»ŅŹÆ”¢ŹÆÓ¢ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
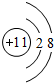 £»YW2µÄµē×ÓŹ½
£»YW2µÄµē×ÓŹ½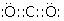 £®
£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Li”¢Na”¢KŌŖĖŲµÄ½šŹōŠŌŅĄ“Ī¼õČõ | |
| B£® | P”¢S”¢ClŌŖĖŲµÄ×īøßÕż¼ŪŅĄ“Ī½µµĶ | |
| C£® | Li”¢Be”¢BµÄŌ×Ó×īĶā²ćµē×ÓŹżŅĄ“Ī¼õÉŁ | |
| D£® | Na+”¢Mg2+”¢Al3+µÄĄė×Ó°ė¾¶ŅĄ“Ī¼õÉŁ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | H2£Øg£©+Br2£Øg£©?2HBr£Øg£© ŗćĪĀ”¢ŗćČŻĻĀ£¬·“Ó¦ĢåĻµÖŠĘųĢåµÄŃÕÉ«±£³Ö²»±ä | |
| B£® | 2NO2£Øg£©?N2O4£Øg£© ŗćĪĀ”¢ŗćČŻĻĀ£¬·“Ó¦ĢåĻµÖŠĘųĢåµÄŃ¹Ēæ±£³Ö²»±ä | |
| C£® | CaCO3£Øs£©?CO2£Øg£©+CaO£Øs£© ŗćĪĀ”¢ŗćČŻĻĀ£¬·“Ó¦ĢåĻµÖŠĘųĢåµÄĆܶȱ£³Ö²»±ä | |
| D£® | 3H2£Øg£©+N2£Øg£©?2NH3£Øg£© ·“Ó¦ĢåĻµÖŠH2ÓėN2µÄĪļÖŹµÄĮæÖ®±Č±£³Ö3£ŗ1 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Ęū³µĪ²ĘųÖŠµÄCO©pNOµČ¶¼ŹĒ“óĘųĪŪČ¾Īļ | |
| B£® | Ēā¼ü©pĄė×Ó¼ü©p¹²¼Ū¼ü¶¼ŹĒĪ¢Į£¼äµÄ×÷ÓĆĮ¦£¬ĒŅŹōÓŚ»Æѧ¼ü | |
| C£® | øßŃ¹Äʵʷ¢³öµÄ»Ę¹āÉä³ĢŌ¶£¬ĶøĪķÄÜĮ¦Ē棬³£ÓĆÓŚµĄĀ·ŗĶ¹ć³”µÄÕÕĆ÷ | |
| D£® | ÓĆŹ³“×æÉŅŌ³żČ„ČČĖ®ŗųÄŚ±ŚµÄĖ®¹ø |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
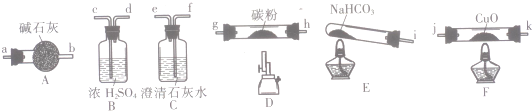
| ŹµŃ鱹ŗÅ | ²Ł×÷ | ĻÖĻó |
| a | ¼ÓČė×ćĮæĻ”ĻõĖį”¢Õńµ“ | ŹŌ¹ÜÄŚŗģÉ«¹ĢĢåĶźČ«Čܽā£¬ČÜŅŗ±äĪŖĄ¶É«£¬²¢ÓŠĪŽÉ«ĘųĢå²śÉś |
| b | ¼ÓČė×ćĮæĻ”ĮņĖį”¢Õńµ“ | ŹŌ¹ÜÄŚÓŠŗģÉ«¹ĢĢ壬ČÜŅŗĪŖĪŽÉ« |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ×īøßÕż»ÆŗĻ¼Ū£ŗF£¾O£¾N£¾C£¾Al | B£® | Ąė×Ó°ė¾¶£ŗF-£¾O2-£¾Na+£¾Al3+ | ||
| C£® | ČČĪČ¶ØŠŌ£ŗPH3£¼H2S£¼HCl£¼HF | D£® | ¼īŠŌĒæČõ£ŗNaOH£¾Mg£ØOH£©2£¾Al£ØOH£©3£¾KOH |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com