
工业上用某矿渣(含有Cu2O、Al2O3、Fe2O3、SiO2)提取铜的操作流程如下:
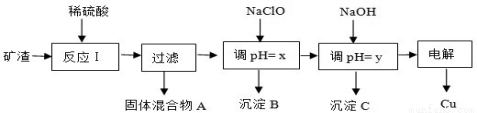
已知: Cu2O + 2H+ = Cu + Cu2+ + H2O
沉淀物 | Cu(OH)2 | Al(OH)3 | Fe(OH)3 | Fe(OH)2 |
开始沉淀pH | 5.4 | 4.0 | 1.1 | 5.8 |
沉淀完全pH | 6.7 | 5.2 | 3.2 | 8.8 |
(1)固体混合物A中的成分是 。
(2)反应Ⅰ完成后,铁元素的存在形式为 。(填离子符号)请写出生成该离子的离子方程式 。
(3)x、y对应的数值范围分别是 、 。
(4)电解法获取Cu时,阴极反应式为 ,阳极反应式为 。
(5)下列关于NaClO调pH的说法正确的是 。
a. 加入NaClO可使溶液的pH降低
b. NaClO能调节pH的主要原因是由于发生反应ClO-+ H+ HClO, ClO-消耗H+,从而达到调节pH的目的
HClO, ClO-消耗H+,从而达到调节pH的目的
c .NaClO能调节pH的主要原因是由于NaClO水解ClO-+ H2O HClO+OH-,OH-消耗H+ ,从而达到调节pH的目的
HClO+OH-,OH-消耗H+ ,从而达到调节pH的目的
(6)用NaClO调pH,生成沉淀B的同时生成一种具有漂白作用的物质,该反应的离子方程式为_________________________ 。
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源:2015-2016学年湖南省五市十校教研教改共同体高二下期末化学试卷(解析版) 题型:实验题
G是一种新型香料的主要成分之一,其结构中含有三个六元环。G的合成路线如下(部分产物和部分反应条件略去):


已知:
①B中核磁共振氢谱图显示分子中有6种不同环境的氢原子;
②D和F互为同系物。
请回答下列问题:
(1)(CH3)2C=CH2的系统命名法名称为 ,生成B这一步的反应类型为 。
(2)E的结构简式为 ,F分子中含有的含氧官能团名称是 。
(3)C经氧化后可得到一种能与新制银氨溶液发生银镜反应的物质,请写出该银镜反应的化学方程式 。
(4)F可在一定条件下合成高分子化合物,请写出该高分子化合物的结构简式 。
(5)同时满足下列条件:①与FeCl3溶液发生显色反应;②苯环上有两个取代基;③能与碳酸氢钠溶液反应放出气体;这样的D的同分异构体共有 种(不包括立体异构);
(6)请参照合成路线中苯乙烯合成F的方法,写出由1-丁烯制取2-羟基丁酸 的合成线路: 。
的合成线路: 。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年黑龙江省高一下期末化学试卷(解析版) 题型:填空题
A、B、C、D、E五种元素的原子序数依次增大,且均小于18;A原子的最外层比B原子的最外层少2个电子,A原子的最外层电子数是次外层电子数的两倍;A、B、C三种元素能结合成化合物C2AB3,在1 mol C2AB3中共有52 mol电子;0.5mo1D元素的单质与酸全部反应时,有9.03×1023个电子转移,在B与D形成的化合物中,D的质量分数为52.94%,D原子核内有14个中子;每个E原子与氢原子化合时只生成了一个共价键。试填写下列空白:
(1)元素的名称D ,E 。
(2)C在B中燃烧生成的化合物的化学式
(3)A.B.C结合成的化合物的化学式是 。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年黑龙江省高一下期末化学试卷(解析版) 题型:选择题
在恒温恒容条件下,将4molA和2molB放入一密闭容器中2A(g)+B(g) 2C(g)+D(s),达到平衡时,C的体积分数为a;在相同条件下,按下列配比分别投放A、B、C、D,达到平衡时,C的体积分数不等于a的是( )
2C(g)+D(s),达到平衡时,C的体积分数为a;在相同条件下,按下列配比分别投放A、B、C、D,达到平衡时,C的体积分数不等于a的是( )
A.4mol、2mol、0mol、2mol
B.2mol、1mol、2mol、2mol
C.2mol、1mol、2mol、1mol
D.2mol、1mol、0mol、1mol
查看答案和解析>>
科目:高中化学 来源:2015-2016学年黑龙江省高一下期末化学试卷(解析版) 题型:选择题
下列有关描述正确的是( )
A. 两种同位素137Cs和133Cs形成的单质化学性质几乎完全相同
B. 非金属元素的原子半径越小越容易得电子,该元素最高价氧化物的水化物酸性一定也越强
C. 随原子序数的增大,碱金属元素单质的密度逐渐增大,ⅦA元素的单质的熔沸点逐渐升高
D. 主族元素A、B、C、D的离子aA2+、bB+、cC2ˉ、dDˉ(n为正整数)具有相同的电子层结构,则原子序数大小关系为a>b>c>d
查看答案和解析>>
科目:高中化学 来源:2015-2016学年黑龙江省高二下期末化学试卷(解析版) 题型:选择题
某物质中可能有甲酸、乙酸、甲醇和甲酸乙酯1种物质中1种或几种,在鉴别时有下列现象:(1)有银镜反应;(2)加入新制Cu(OH)2悬浊液沉淀不溶解;(3)与含酚酞的NaOH溶液共热发现溶液中红色逐渐消失以至无色,下列叙述正确的有( )
A.几种物质都有
B.有甲酸乙酯,可能有甲酸
C.有甲酸乙酯和甲醇
D.有甲酸乙酯,可能有甲醇
查看答案和解析>>
科目:高中化学 来源:2015-2016学年黑龙江省高二下期末化学试卷(解析版) 题型:选择题
在浓度为0.01mol/L Mg(HCO3)2,0.02mol/LCaCl2的水溶液1L中,要同时除去Mg2+,Ca2+应选用的试剂是( )
A. NaHCO3 B. Na2CO3 C. Ca(OH)2 D. NaOH
查看答案和解析>>
科目:高中化学 来源:2015-2016学年河北省唐山市高一下期末文科化学试卷(解析版) 题型:填空题
将4mol A气体和2mol B气体在2L的容器中混合并在一定条件下发生如下反应:2A(g)+B(g) 2C(g), 若经2s 后测得C的浓度为 0.6mol•L-1。
2C(g), 若经2s 后测得C的浓度为 0.6mol•L-1。
(1)现有下列几种说法:
① 物质A表示的反应的平均速率为 0.6mol•(L•s)-1;
② 物质B表示的反应的平均速率为 0.15mol•(L•s)-1;
③ 2s 时物质A的浓度为1.4mol•L-1;
④2s 时物质B的转化率为70%。
其中正确的是___________
A. ①③ B. ①④ C. ②③ D. ③④
(2) 若①②中用物质A、B表示的反应速率分别为 0.6mol• (L•s)-1、 0.15mol•(L•s)-1,则_______(填A或B)物质表示的反应速率更快
查看答案和解析>>
科目:高中化学 来源:2015-2016学年辽宁省大连市高一下期末化学试卷(解析版) 题型:填空题
研究NO2、SO2、CO等大气污染气体的处理具有重要意义。
(1)已知:2SO2(g)+O2(g) 2SO3(g) ΔH= -196.6kJ·mol-1
2SO3(g) ΔH= -196.6kJ·mol-1
2NO(g)+O2(g) 2NO2(g) ΔH= -113.0kJ·mol-1
2NO2(g) ΔH= -113.0kJ·mol-1
则反应NO2(g)+SO2(g) SO3(g)+NO(g)的ΔH= kJ·mol-1
SO3(g)+NO(g)的ΔH= kJ·mol-1
(2)一定条件下将NO2与SO2以体积比2∶1置于密闭容器中发生上述反应,下列能说明反应达到平衡状态的是
A.体系压强保持不变
B.混合气体颜色保持不变
C.SO3和NO的体积比保持不变
D.每消耗1molSO3的同时生成1mol NO
测得上述反应达平衡时NO2与SO2的体积比为5∶1,则NO2的转化率 =
(3)CO可用于合成甲醇,反应方程式为CO(g)+2H2(g) CH3OH(g)。CO在不同温度下的平衡
CH3OH(g)。CO在不同温度下的平衡
转化率与压强的关系如图(2)所示。该反应ΔH 0(填“>”或“<”)。实际生产条件控制在250℃、1.3×104kPa左右,选择此压强的理由是: 。

(4)依据燃烧的反应原理,合成的甲醇可以设计如图(3)所示的原电池装置。
① 该电池工作时,OH- 向 极移动(填“正”或“负”)。
② 该电池正极的电极反应式为 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com