
| A. | 16 g | B. | 24 g | C. | 32 g | D. | 64g |
分析 铜与一定量浓硝酸反应,得到硝酸铜溶液和NO、N2O4、NO2 的混合气体,这些气体与11.2L O2(标准状况)混合后通入水中,所有气体完全被水吸收生成硝酸,说明铜失去的电子给做氧化剂的硝酸,生成气体,气体和氧气全部反应生成硝酸,证明氧气得到电子和铜失去的电子相同,依据电子守恒计算得到.
解答 解:铜与一定量浓硝酸反应,得到硝酸铜溶液和NO、N2O4、NO2 的混合气体,这些气体与11.2L O2(标准状况)混合后通入水中,所有气体完全被水吸收生成硝酸,完全生成HNO3,则整个过程中HNO3 反应前后没有变化,说明铜失去的电子给做氧化剂的硝酸,生成气体,气体和氧气全部反应生成硝酸,证明氧气得到的电子和铜失去的电子相同,即Cu失去的电子都被O2得到,
由电子守恒可知n(Cu)×2=n(O2)×4,
n(Cu)=$\frac{\frac{11.2L}{22.4L/mol}×4}{2}$=1mol,
消耗铜的质量=1mol×64g/mol=64g,
故选D.
点评 本题考查了氧化还原反应的电子守恒的计算应用,物质性质的变化和反应过程的分析是解题关键,题目难度中等.


 海淀黄冈名师导航系列答案
海淀黄冈名师导航系列答案 普通高中同步练习册系列答案
普通高中同步练习册系列答案科目:高中化学 来源: 题型:选择题
| A. | △H3=+0.33 kJ•mol-1 | |
| B. | 单斜硫转化为正交硫的反应是吸热反应 | |
| C. | △H3<0,正交硫比单斜硫稳定 | |
| D. | △H3>0,单斜硫比正交硫稳定 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 硫酸亚铁是重要的亚铁盐,在农业上用作农药,主要治小麦黑穗病,还可以用作除草剂;在工业上用于染色、制造蓝黑墨水和木材防腐等.
硫酸亚铁是重要的亚铁盐,在农业上用作农药,主要治小麦黑穗病,还可以用作除草剂;在工业上用于染色、制造蓝黑墨水和木材防腐等.| 操作步骤 | 预期实验现象 | 预期实验结论 |
| 向其中一份溶液中加入KSCN溶液 , | 溶液变成血红色 | 固体中含有Fe2O3 |
| 向另一份溶液中滴加2滴黄色K3[Fe(CN)6]溶液 | 产生蓝色沉淀 | 固体中含有FeO |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
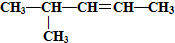
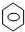 ⑥
⑥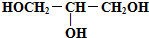 ⑦CH3CH2CH3
⑦CH3CH2CH3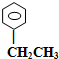 ⑨
⑨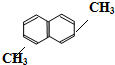 ⑩
⑩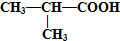
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ②④⑥⑦ | B. | ②⑤⑦⑧ | C. | ①③⑤⑥ | D. | ②⑤⑥⑧ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
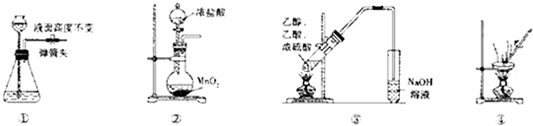
| A. | 装置①所示气密性良好 | |
| B. | 装置②可用于实脸室制取氯气 | |
| C. | 装置③可用于制取并收集乙酸乙脂 | |
| D. | 装置④可用于除去硫酸铜晶体中的结晶水 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向Ag(NH3)2NO3溶液中加入盐酸:Ag(NH3)2++2H+=Ag++2NH4+ | |
| B. | 向Na2O2中加入足量的水:2Na2O2+2H2O=4Na++4OH-+O2↑ | |
| C. | 向硫酸铝溶液中加入过量氨水:Al3++3OH-=Al(OH)3↓ | |
| D. | 向Ca(HCO3)2溶液中加入澄清石灰水:Ca2++2HCO3-+2OH-=CaCO3↓+CO32-+2H2O |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com