
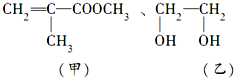
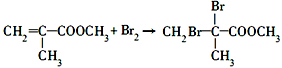 ,
,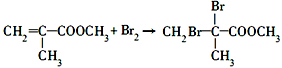 ;
;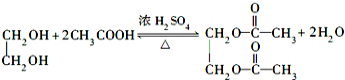 ,
,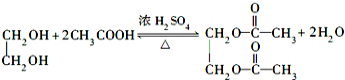 .
.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
| A、2240mL |
| B、4480mL |
| C、3360mL |
| D、1120mL |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、质子数c>b |
| B、原子半径X<W |
| C、氢化物的稳定性H2Y>HZ |
| D、离子的还原性Y2->Z- |
查看答案和解析>>
科目:高中化学 来源: 题型:
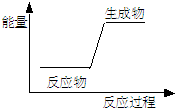
| A、生石灰加水生成熟石灰 |
| B、C+H2O═CO+H2 |
| C、金属钠与水反应 |
| D、HNO3+NaOH═NaNO3+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 温度/℃ | 400 | 500 | 800 |
| 平衡常数K | 9.94 | 9 | 1 |
| 实验序号 | 反应温度/℃ | H2C2O4溶液 | 酸性KMnO4溶液 | H2O | ||
| V/mL | c/(mol?L-1) | V/mL | c/(mol?L-1) | V/mL | ||
| ① | 25 | 8.0 | 0.20 | 5.0 | 0.010 | 0 |
| ② | 25 | 6.0 | 0.20 | 5.0 | 0.010 | x |
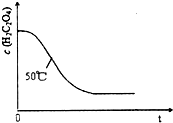
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、17g羟基(-OH)所含有的电子数是10NA个 |
| B、1mol苯乙烯中含有的碳、碳双键数为4NA个 |
| C、常温下,14g乙烯和丙烯的混合物中总原子数为3NA个 |
| D、4.2g C3H6中含有的碳碳双键数一定为0.1NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com