
 2SO3(g)��
2SO3(g)��

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
 Z��g��+2W��g����H��0�ﵽƽ�⣨��ʱV��B��=0.9a�����Իش�
Z��g��+2W��g����H��0�ﵽƽ�⣨��ʱV��B��=0.9a�����Իش�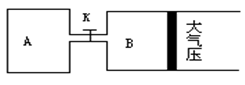
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 2NH3 (g)������;���ֱ���ƽ�⣺
2NH3 (g)������;���ֱ���ƽ�⣺| A��;������;�������û������İٷ������ͬ |
| B��;�����ƽ������v (N2)��;�����ƽ������v (NH3)�ı�ֵΪ1��2 |
| C��;��������NH3��Ũ����;��������NH3��Ũ��֮��Ϊ1��2 |
| D��;������;��������ƽ������������ʵ���֮��Ϊ1��2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
 ��ǰ�ƻ����̶���ͼ��λ�ã�NO2��ת���ʽ� (���������С�������䡱)��
��ǰ�ƻ����̶���ͼ��λ�ã�NO2��ת���ʽ� (���������С�������䡱)��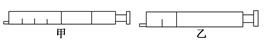
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��

A��c0 (g)+H (g)+H (g) (g)  F=e=CO(g)+H F=e=CO(g)+H 0(g)��H>0 0(g)��H>0 |
B��CH CH CH 0H(g) 0H(g)  CH CH =CH =CH (g)+H (g)+H 0(g)��H>0 0(g)��H>0 |
C��2C H H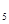 CH CH CH CH (g)+0 (g)+0 (g) (g)  2C 2C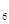 H H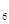 CH=CH CH=CH (g)+2H (g)+2H O(g)��H<0 O(g)��H<0 |
D��C0 (g)+2NH (g)+2NH (g) (g)  CO(NH CO(NH ) ) (s)+H (s)+H 0(g)��H<0 0(g)��H<0 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
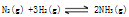 �ﵽƽ���ƽ��������ƽ����Է�������Ϊ12.5�������к���������Ϊ
�ﵽƽ���ƽ��������ƽ����Է�������Ϊ12.5�������к���������Ϊ| A��32.64 g | B��65.28 g | C��3.84 g | D��38.4 g |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 C(g)��A�ĺ������¶ȵĹ�ϵ��ͼ��ʾ�����н�����ȷ���ǣ�
C(g)��A�ĺ������¶ȵĹ�ϵ��ͼ��ʾ�����н�����ȷ���ǣ�
| A��T1>T2, ����Ӧ���� | B��T1<T2, ����Ӧ���� |
| C��T1>T2, ����Ӧ���� | D��T1<T2, ����Ӧ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
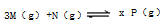 ��ע��xΪP����
��ע��xΪP����| A�����ٴ�ƽ��ʱ�����������и�����l mol M��N��P����N��ת����һ������ |
| B�������ƽ�����ټ���3mol M��2 mol N��P���������������a�����ж�x>4 |
| C����x=2�������ϵ��ʼ���ʵ���Ӧ������3 n��N��=n��M�� |
| D��������ϵ��ʼ���ʵ�������3 n��P��+8 n��M��="12" n��N�������ж�x=4 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
| �������� | A | B | C | D |
ƽ��ʱ ���죩 ���죩 | | | 16 | 17 |
| ƽ��ʱN2ת���� | 20% | �� | �� | �� |
| ƽ��ʱH2ת���� | | 30% | | |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com