
| A. | 充电时阴极发生氧化反应 | |
| B. | 充电时将碳电极与电源的正极相连 | |
| C. | 放电时碳电极反应为H2-2e -=2H+ | |
| D. | 放电时镍电极反应为NiO(OH)+H20+e-=Ni( OH)2+OH - |
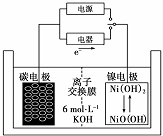
分析 根据图片中电子流向知,放电时,石墨电极是负极,电极反应式为H2+2OH--2e-=2H2O,正极反应式为NiO(OH)+H2O+e-═Ni(OH)2+OH-,充电时阴阳极与放电时负极、正极反应式正好相反,据此分析解答.
解答 解:根据图片中电子流向知,放电时,石墨电极是负极,电极反应式为H2+2OH--2e-=2H2O,正极反应式为NiO(OH)+H2O+e-═Ni(OH)2+OH-,充电时阴阳极与放电时负极、正极反应式正好相反,
A.充电时,阴极上得电子发生还原反应,故A错误;
B.充电时,C电极作阴极,所以应该与电源负极相连,故B错误;
C.放电时,电解质溶液呈碱性,负极上氢气失电子和氢氧根离子反应生成水,电极反应式为H2+2OH--2e-=2H2O,故C错误;
D.放电时镍电极是正极,正极上得电子发生还原反应,电极反应式为NiO(OH)+H2O+e-═Ni(OH)2+OH-,故D正确;
故选D.
点评 本题考查化学电源新型电池,为高考高频点,明确各个电极上发生的反应是解本题关键,会结合电解质溶液酸碱性书写电极反应式,知道放电时和充电时电极反应式关系,题目难度中等.


科目:高中化学 来源: 题型:选择题
| A. | 检验Fe2(SO4)3溶液中是否含有FeSO4的实验操作是:取少量待测液于试管中,滴加1-2滴酸性KMnO4溶液 | |
| B. | 碱金属与卤素所形成的化合物具有熔点较高,能溶于水,水溶液能导电,熔融状态下能导电的性质 | |
| C. | 配制FeCl2溶液的实验操作是:在装有适量固体的大试管中加入适量的蒸馏水,再滴加少量稀盐酸并搅拌,同时加入少量的铁粉 | |
| D. | 向紫色石蕊试液中加入过量的过氧化钠粉末振荡,可观察到溶液中有气泡产生,溶液最终变为无色 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 该温度下醋酸银的溶解度约为0.668g | |
| B. | 该温度下饱和醋酸水溶液的pH=2.5-$\frac{1}{2}$lg1.8 | |
| C. | 某溶液中含有CH3COO-和CO32-,浓度均为0.01mol/L,向其中逐滴加入0.01 mol/L的AgNO3溶液,CH3COO-离子先产生沉淀 | |
| D. | 醋酸溶液加水稀释后,溶液中导电粒子的数目减少 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. |  如图:可以表示CO2的比例模型 | |
| B. | 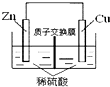 如图表示的锌铜原电池,电池工作一段时间后,右侧溶液的pH不变 | |
| C. | 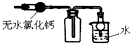 如图:可用于收集干燥氨气 | |
| D. | 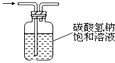 如图:可用于除去氯气中的HCl气体 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用纯碱溶液清洗餐具上油污 | B. | 用稀硫酸清洗水壶里水垢 | ||
| C. | 用漂白液洗涤白衬衣上红色墨迹 | D. | 用汽油清洗皮肤上的油漆 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | X、Y、Z三种元素既可形成只含共价键的化合物,又可形成既含共价键又含离子键的化合物 | |
| B. | Z、W、Q三种元素所形成的简单离子的半径由大到小的顺序是W>Q>Z | |
| C. | Y的简单氢化物通入Q的氧化物的水化物水溶液中可能生成两种盐 | |
| D. | X与W组成的化合物可与水发生氧化还原反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A.食用碱的主要成分为氢氧化钠 | B.光纤的主要成分为晶体硅 | C.铜绿的主要成分为氢氧化铜 | D.漂白液的有效成分为次氯酸钠 |
 |  |  |  |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
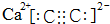 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com