
取体积相同的KI、Na2SO3、FeBr2溶液,分别通入足量氯气,当恰好完全反应时,三种溶液消耗氯气的物质的量相同,则KI、Na2SO3、FeBr2溶液的物质的量浓度之比为( )
A. 2:1:2 B. 2:1:3
C. 6:3:2 D. 3:7:1
科目:高中化学 来源:广东省2016-2017学年高二上学期期末考试化学(文)试卷 题型:选择题
下列说法正确的是
A. 乙烷和乙醇是同系物
B. 苯和甲苯都属于饱和烃
C. 有机化合物一定含有碳元素
D. 含有碳元素的化合物一定是有机化合物
查看答案和解析>>
科目:高中化学 来源:2017届浙江省温州市高三第二次选考模拟考试(2月)化学试卷(解析版) 题型:选择题
下列说法不正确的是
A. 乙烯能使溴水、酸性高锰酸钾溶液褪色,其褪色原理不相同
B. 苯在一定条件下能与浓硝酸反应得到硝基苯,发生了取代反应
C. 乙醛在一定条件下能与氢气反应生成乙醇,发生了还原反应
D. 相同物质的量的乙炔与乙二醇(HOCH2CH2OH)在足量的氧气中完全燃烧,消耗氧气的质量不相同
查看答案和解析>>
科目:高中化学 来源:2016-2017学年辽宁省六校协作体高二下学期期初化学试卷 题型:推断题
五种短周期元素A、B、C、D、E、F的原子序数依次增大.A和C同族,B和E同族,C离子和B离子具有相同的电子层结构,D的最外层电子数与电子层数相同.A和B、E、F均能形成共价化合物(由分子构成的化合物).A和B形成的化合物在水中呈碱性,C和F形成的化合物在水中呈中性.
回答下列问题:
(1)五种元素中,原子半径最大的是______(填元素名称).最高价氧化物对应水化物酸性最强的元素为____ (填元素符号),其最高价氧化物对应水化物与NaOH反应的离子方程式为___________________________.
(2)由A和B、E、F所形成的化合物中,热稳定性最差的是_________________ (用化学式表示).
(3)A和F形成的化合物与A和B形成的化合物反应,产物的化学式为________.
(4)D元素最高价氧化物的化学式为_______,最高价氧化物对应水化物与氢氧化钠反应的离子方程式为___________________________.
(5)单质F与水反应的离子方程式为___________________..
查看答案和解析>>
科目:高中化学 来源:2016-2017学年辽宁省六校协作体高二下学期期初化学试卷 题型:选择题
交通警察执法时常使用的便携式酒精检查仪可能应用了:3CH3CH2OH+2K2Cr2O7(橙色)+ 8H2SO4=3CH3COOH +2Cr2(SO4)3(蓝绿色)+2K2SO4+11H2O这一反应原理,关于该反应,下列说法正确的是( )
A. 该反应证明了,含最高价元素的化合物,一定具有强氧化性
B. 1mol还原剂反应时,转移的电子数为2NA
C. H2SO4在反应中表现了氧化性和酸性
D. 可以利用该反应原理,将它设计成原电池,通过检测电流强度判断司机是否饮酒
查看答案和解析>>
科目:高中化学 来源:2016-2017学年辽宁省六校协作体高二下学期期初化学试卷 题型:选择题
下列实验中,对应的现象以及结论都正确且两者具有因果关系的是( )
选项 | 实验 | 现象 | 结论 |
A | 将氯气通入品红溶液 | 溶液红色褪去 | 氯气具有漂白性 |
B | 将铜粉加入1.0mol·L﹣1 的Fe2(SO4)3溶液中 | 溶液变蓝,有黑色固体出现 | 金属Fe比Cu活泼 |
C | 用坩埚钳夹住用砂纸仔细打磨过的铝箔在酒精灯上加热 | 熔化后的液态铝滴落下来 | 金属铝的熔点比较低 |
D | 向盛有少量浓硝酸、稀硝酸的两支试管中分别加入一片大小相同的铜片 | 浓硝酸中铜片很快开始溶解,并放出红棕色气体;稀硝酸中过一会铜片表面才出现无色气体,气体遇空气变红棕色 | 浓硝酸氧化性强于稀硝酸 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源:2017届陕西省宝鸡市高三教学质量检测(一)理综化学试卷(解析版) 题型:实验题
某探究性实验小组的同学将打磨过的镁条投入到滴有酚酞的饱和NaHCO3溶液中,发现反应迅速,产生大量气泡和白色不溶物,溶液的浅红色加深。该小组同学对白色不溶物的成分进行了探究和确定。
Ⅰ、提出假设:
(1)甲同学:可能只是MgCO3;
乙同学:可能只是 ;
丙同学:可能是xMgCO3·yMg(OH)2
(2)在探究沉淀成分前,须将沉淀从溶液中过滤、洗涤、低温干燥,洗涤沉淀的操作方法是 。
Ⅱ、定性实验探究:
(3)取沉淀物少许于试管中,加入稀盐酸时固体溶解,产生大量气泡,则 同学假设错误(选填“甲”、“乙”或“丙”)。
Ⅲ、定量实验探究:取一定量已干燥过的沉淀样品,利用下列装置测定其组成(部分固定夹持类装置未画出),经实验前后对比各装置的质量变化来分析沉淀的组成,得出丙同学的假设是正确的。请回答下列问题:
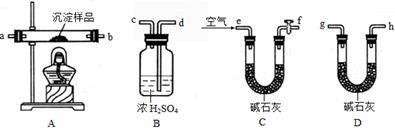
(4)实验中合理的连接顺序为:e→ → → → → → g→h(各装置只使用一次)。
(5)实验一段时间后,当B装置中 (填实验现象),停止加热,说明固体已分解完全;打开f处的活塞,缓缓通入空气数分钟的目的是 ,装置C中碱石灰的作用是 。
(6)指导老师认为在上述实验装置中末端还需再连接一个D装置,若无此装置,会使测出的x :y的值 (选填“偏大”、“偏小”或“无影响”)。
(7)若改进实验后,最终装置B质量增加m克,装置D质量增加了n克,则x :y= 。(用含m、n的代数式表示)
查看答案和解析>>
科目:高中化学 来源:2017届安徽省A10联盟高三下学期开年考试理综化学试卷(解析版) 题型:选择题
下列实验能达到实验目的且符合实验设计要求的是( )
A.  测定反应生成氢气的速率
测定反应生成氢气的速率
B.  模拟海水中铁的防护
模拟海水中铁的防护
C. 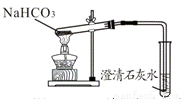 证明碳酸氢钠热稳定性差
证明碳酸氢钠热稳定性差
D.  制备乙酸甲酯
制备乙酸甲酯
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河北省石家庄市高一上学期期末考试化学试卷(解析版) 题型:选择题
实验室可用K2Cr2O7固体与浓盐酸混合加热制备氯气。发生的离子反应如下:
____Cr2O72-+____Cl-+____H+=____Cl2↑+____Cr3++____ ,下列有关叙述不正确的是
,下列有关叙述不正确的是
A. 以上各物质对应的计量数依次为1、6、14、3、2、7
B. Cr2O72-发生了还原反应
C.  处对应的物质是H2O
处对应的物质是H2O
D. 若0.1mol Cr2O72-参加反应,产生氯气物质的量是0.5mol
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com