
(1)标准状况下通入氯气的体积。
(2)原溴化钾溶液的物质的量浓度。
标准状况下通入氯气的体积为1.4 L,原KBr溶液物质的量浓度为1.0 mol·L-1。
解析:本题考查信息转化能力及审题能力。
由题给信息,一定量氯气与KBr反应后,固体残留物中含溴说明Cl2不是过量而是不足。
再由K+和Cl-的物质的量之比为2∶1,可知K+与Br-的物质的量之比也为2∶1,则n(Cl)∶n(Br)=1∶1,说明反应掉的Br-与反应剩下的Br-的物质的量相等,也说明反应消耗的Cl2与生成Br2的物质的量相等。
(1)设标准状况下通入Cl2的体积为V L。
2KBr+Cl2====2KCl+Br2
化学计量数之比 2 1
物质的量之比 ![]() n(Cl2)
n(Cl2)
![]()
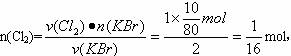
V(Cl2)=n(Cl2)·Vm=116 mol×22.4 L·mol-1=1.4 L。
(2)因为反应的KBr与剩余KBr的物质的量相等,所以原KBr的物质的量
n(KBr)=2×![]() mol=
mol=![]() mol,
mol,
则
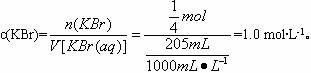


 快乐暑假暑假能力自测中西书局系列答案
快乐暑假暑假能力自测中西书局系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、n(Na+):n(C1-)可能为7:3 | B、n(NaCl):n(NaClO):n(NaClO3)可能为11:1:2 | C、参加反应氯气物质的量为0.15mol | D、反应中转移电子物质的量n的范围:0.15mol<n<0.25mol |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com