
【题目】下列状态的物质,既能导电又属于电解质的是( )
A. MgCl2晶体 B. NaCl溶液 C. 液态氯化氢 D. 熔融的KOH
科目:高中化学 来源: 题型:
【题目】25℃时,二元弱酸H2R的pKa1=1.85,pKa2=7.45(已知pKa=﹣lgKa).在此温度下向20mL0.1molL﹣1H2R溶液中滴加0.1molL﹣1的NaOH溶液,溶液的pH随NaOH溶液体积的变化如图所示.
下列有关说法正确的是( )
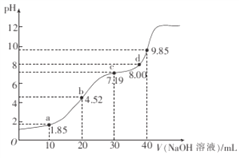
A. a点所示溶液中:c(H2R)+c(HR﹣)+c(R2﹣)=0.1molL﹣1
B. b点所示溶液中:c(Na+)>c(HR﹣)>c(H2R)>c(R2﹣)
C. c点所示溶液中:c(Na+)<3c(R2﹣)
D. d点所示溶液中:c(Na+)>c(R2﹣)>c(HR﹣)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E、F是原子序数依次增大的短周期主族元素,A的最外层电子数是次外层电子数的2倍,B是短周期中金属性最强的元素,C是同周期中阳离子半径最小的元素,D元素的最高价氧化物对应水化物与B元素的最高价氧化物对应水化物反应的产物M是制备木材防火剂的原料,E的最外层电子数与内层电子数之比为3∶5。请回答:
(1)D的元素名称为___。F在元素周期表中的位置是___________。
(2)C离子结构示意图为______,A、D形成的氢化物中稳定性更好的是:______,以上元素最高价氧化物对应水化物中碱性最强的是____,E和F元素的单质氧化性较强的是:_________(填化学式)。
(3)用电子式表示由元素B和F组成的化合物的过程:____________。
(4)B单质与氧气反应的产物与C的单质同时放入水中,产生两种无色气体,有关的化学方程式为_____________、______________。
(5)工业上将干燥的F单质通入熔融的E单质中可制得化合物E2F2,该物质可与水反应生成一种能使品红溶液褪色的气体,0.2 mol该物质参加反应时转移0.3 mol电子,其中只有一种元素化合价发生改变,该反应的化学方程式为___________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将适量铁粉放入FeCl3溶液中,完全反应后,溶液中的Fe2+和Fe3+浓度相等,则已反应的Fe3+和未反应的Fe3+的物质的量之比是( )
A. 2∶3 B. 3∶2
C. 1∶2 D. 1∶1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二氧化碳被认为是加剧温室效应的主要物质,资源化利用二氧化碳不仅可减少温室气体的排放,还可重新获得燃料或重要工业产品。
Ⅰ.有科学家提出可利用FeO吸收和利用CO2,相关的热化学方程式如下:
6FeO(s)+CO2(g)=2Fe3O4(s)+C(s) , ΔH=-76.0 kJ·mol-1
②3FeO(s)+H2O(g)= Fe3O4(s)+H2(g) ΔH=-18.7 kJ·mol-1
(1)在上述反应中①中,每吸收1molCO2,就有_______molFeO被氧化。
(2)试写出C(s)与水蒸气反应生成CO2和H2的热化学方程式___________。
Ⅱ.一定条件下,二氧化碳转化为甲烷。向一容积为2L的恒容密闭容器中充人一定量的CO2和H2,在300℃时发生上述反应的反应CO2(g)+4H2(g) ![]() CH4(g)+2H2O(g) 。达到平衡时,各物质的浓度分别为CO2 0.2mol·L-1、CH4 0.8mol·L-1、H2 0.8mol·L-1,H2O 1.6mol·L-1。
CH4(g)+2H2O(g) 。达到平衡时,各物质的浓度分别为CO2 0.2mol·L-1、CH4 0.8mol·L-1、H2 0.8mol·L-1,H2O 1.6mol·L-1。
(3)在300℃是,将各物质按下列起始浓度(mol·L-1)加入该反应容器中,达到平衡后,各组分浓度与上述题中描述的平衡浓度相同的是_____________。
选项 | CO | H2 | CH4 | H2O |
A | 0 | 0 | 1 | 2 |
B | 2 | 8 | 0 | 0 |
C | 1 | 4 | 1 | .2 |
D | 0.5 | 2 | 0.5 | 1 |
(4)若保持温度不变,再向该容器内充入与起始量相等的CO2和H2,重新达到平衡时,CH4的浓
度________(填字母)。
A.c(CH4)=0.8mol·L-1 B.0.8mol L-1 >c(CH4) >1.6mol L-1
C.c(CH4)=l.6mol·L-1 D.C(CH4)>1.6mol L-1
(5)在300时,如果向该容器中加入CO20.8 mol·L-1、H21.0 mol·L-1、CH4 2.8 mol·L-1、H2O 2.0mol·L-1,则该可逆反应初始速率v正_____v逆 (填“>” 或“<”)。
(6)若已知200℃时该反应的平衡常数K=64.8 则该反应的△H_________0(填“>”或“<”)。
Ⅲ.某高校的研究人员研究出一种方法,可实现水泥生产时CO2零排放,其基本原理如图所示

(7)上述电解反应在温度小于900℃时进行,碳酸钙先分解为CaO和CO2,电解质为熔融合碳酸钙,阴极的电极反应式为3CO2+4e- =C+2CO32-,则阳极的电极反应式为______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学采用硫铁矿焙烧取硫后的烧渣(主要成分为Fe2O3、SiO2、Al2O3,不考虑其他杂质)制取七水合硫酸亚铁(FeSO4·7H2O),设计了如下流程:

下列说法不正确的是
A. 溶液1中的阳离子可与NH4+、HCO3-、I-、SO42-在同一溶液中大量共存
B. 向溶液2中加入3-5滴K3[Fe(CN)6](铁氰化钾)溶液,可观察到有蓝色沉淀生成
C. 向固体2中加入足量NaOH溶液,发生反应的离子方程式:Al(OH)3+OH-=AlO2-+2H2O
D. 从溶液2得到FeSO4·7H2O产品的过程中,须控制条件防止其氧化和分解
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与人类生活、生产、环境密切相关,下列说法不正确的是
A. 干燥剂硅胶、硅橡胶和光导纤维的主要成分都是二氧化硅
B. 把石灰浆喷涂在树干上可消灭树皮上的过冬虫卵
C. 防伪荧光油墨由颜料与树脂连接料等制成,其中树脂属于有机高分子材料
D. 新能源汽车的推广使用有助于减少光化学烟雾
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种碳纳米管新型二次电池的装置如图所示。下列说法中正确的是
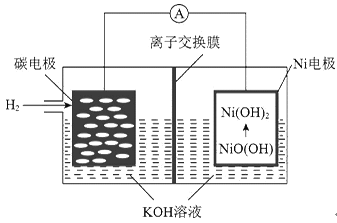
A. 离子交换膜选用阳离子交换膜(只允许阳离子通过) B. 正极的电极反应为NiO(OH)+H2O+e-=Ni(OH)2+OH-
C. 导线中通过1mol电子时,理论上负极区溶液质量增加1g D. 充电时,碳电极与电源的正极相连
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I、依据事实,写出下列反应的热化学方程式。
(1)在25 ℃、101 kPa下,1 g甲烷燃烧生成CO2和液态水时放热55.625 kJ。则表示甲烷燃烧热的热化学方程式为________________________。
(2)若适量的N2和O2完全反应,每生成23 g NO2需要吸收16.95 kJ热量,则表示该反应的热化学方程式为______________。
(3)在25 ℃、101 kPa条件下,C(s)、H2(g)、CH3COOH(1)的燃烧热分别为393.5 kJ/mol、285.8 kJ/mol、870.3 kJ/mol,则2C(s)+2H2(g)+O2(g)===CH3COOH(1)的反应热ΔH为________。
II、锌锰干电池是应用最普遍的电池之一。其基本反应为:
X极:Zn-2e-===Zn2+
Y极:2MnO2+2NH![]() +2e-===Mn2O3+2NH3+H2O
+2e-===Mn2O3+2NH3+H2O
(1)X是电池的________(填“正”或“负”,下同)极,Y是电池的________极。
(2)该电池总反应的离子方程式为:_______________________。
(3)若反应消耗16.25gZn,则电池中转移电子的物质的量为________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com