
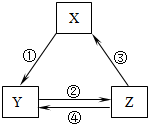
 下表各组物质之间通过一步反应不可以实现如图所示的转化关系的是( )
下表各组物质之间通过一步反应不可以实现如图所示的转化关系的是( )| 选项 | X | Y | Z |
| A | CaO | Ca(OH)2 | CaCO3 |
| B | AlCl3 | NaAlO2 | Al(OH)3 |
| C | Fe2O3 | FeCl3 | Fe(OH)3 |
| D | Fe | FeCl2 | FeCl3 |
| A. | A | B. | B | C. | C | D. | D |
分析 A.CaCO3不能一步生成Ca(OH)2 ;
B.AlCl3与过量氢氧化钠反应生成NaAlO2,NaAlO2与弱酸反应生成Al(OH)3,Al(OH)3与盐酸反应生成AlCl3,Al(OH)3与氢氧化钠反应生成NaAlO2;
C.Fe2O3与盐酸反应生成FeCl3,FeCl3与氢氧化钠反应生成Fe(OH)3,Fe(OH)3受热分解得Fe2O3,Fe(OH)3与盐酸反应生成FeCl3;
D.FeCl3不能一步反应生成Fe;
解答 解:A.CaCO3不能一步生成Ca(OH)2 ,故A错误;
B.AlCl3与过量氢氧化钠反应生成NaAlO2,NaAlO2与弱酸反应生成Al(OH)3,Al(OH)3与盐酸反应生成AlCl3,Al(OH)3与氢氧化钠反应生成NaAlO2,故B正确;
C.Fe2O3与盐酸反应生成FeCl3,FeCl3与氢氧化钠反应生成Fe(OH)3,Fe(OH)3受热分解得Fe2O3,Fe(OH)3与盐酸反应生成FeCl3,故C正确;
D.FeCl3不能一步反应生成Fe,被还原先生成亚铁离子,进而生成Fe,故D错误;
故选AD.
点评 该题是中等难度的试题,试题设计新颖,基础性强,紧扣教材,侧重对学生基础知识的检验和训练,同时坚固对学生能力的培养,有利于激发学生的学习积极性,提高学生灵活运用基础知识解决实际问题的能力


科目:高中化学 来源: 题型:选择题
| A. | 用广泛pH试纸测得氯水的pH=5.2 | |
| B. | 若H2O2分解产生1molO2,理论上转移的电子数约为4×6.02×1023 | |
| C. | 在氧化还原反应中,还原剂得到电子总数等于氧化剂失去电子的总数 | |
| D. | Mg在CO2中燃烧生成MgO和C.在该反应条件下,Mg的还原性强于C的 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
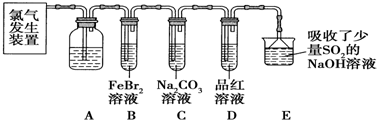
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
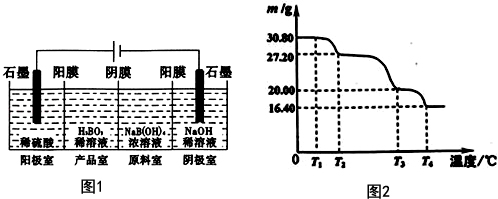 硼酸(H3BO3)与铝酸(H3AlO3)结构相似,可写成B(OH)3.
硼酸(H3BO3)与铝酸(H3AlO3)结构相似,可写成B(OH)3.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
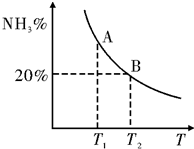 合成氨技术的发明使工业化人工固氮成为现实.
合成氨技术的发明使工业化人工固氮成为现实.| 温度/℃ CO2转化率% $\frac{n(N{H}_{3})}{n(C{O}_{2})}$ | 100 | 150 | 200 |
| 1 | 19.6 | 27.1 | 36.6 |
| 1.5 | a | b | c |
| 2 | d | e | f |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在101kPa下氢气的燃烧热△H=-285.5kJ•mol-1,则水分解的热化学方程式:2H2O(l)=2H2(g)+O2(g)△H=+285.5 kJ•mol-1 | |
| B. | pH=3和pH=5的盐酸各10mL混合,所得溶液的pH=4 | |
| C. | 一定温度下,1L0.50mol/LNH4Cl溶液与2L0.25NH4Cl溶液含NH4+物质的是不同 | |
| D. | 吸热反应“TiO2(g)+2Cl2(g)=TiCl4(g)+O2(g)”在一定条件下可自发进行,则该反应的△S<0 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na2FeO4溶液显强碱性,能消毒杀菌 | |
| B. | Na2FeO4具有强氧化性,能消毒杀菌 | |
| C. | Na2FeO4的氧化产物Fe3+易水解为Fe(OH)3,可以净水 | |
| D. | Na2FeO4的还原产物Fe2+易水解为Fe(OH)2,可以净水 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 实验室用大理石跟稀盐酸制取二氧化碳:2H++CO32-═CO2↑+H2O | |
| B. | 氯化铝中加入氨水:Al3++3OH-═Al(OH)3↓ | |
| C. | 铁粉与氯化铁溶液反应:Fe+Fe3+═2Fe2+ | |
| D. | 硫酸铜与氢氧化钡溶液反应:Cu2++SO42-+Ba2++2OH-═Cu(OH)2↓+BaSO4↓ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com