
| A、SO32- |
| B、ClO4- |
| C、NO2- |
| D、ClO3- |
| 1 |
| 2 |
| 1 |
| 2 |
| 1 |
| 2 |
| 1 |
| 2 |
| 1 |
| 2 |


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
| A | 向FeCl2溶液中滴入氯水 2Fe2++Cl2=2Fe3++2Cl- | 向FeCl2溶液中滴入碘水 2Fe2++I2=2Fe3++2I- |
| B | 向澄清石灰水中通入少量CO2 气体 Ca2++2OH-+CO2=CaCO3↓+H2O | 向澄清石灰水中通入少量SO2 气体 Ca2++2OH-+SO2=CaSO3↓+H2O |
| C | 向Na2CO3溶液中滴入稀HNO3 CO32-+2H+=CO2↑+H2O | 向Na2SO3溶液中滴入稀HNO3 SO32-+2H+=SO2↑+H2O |
| D | CO2通入漂白粉溶液中 CO2+Ca2++2ClO-+H2O=CaCO3↓+2HClO | SO2通入漂白粉溶液中 SO2+Ca2++2ClO-+H2O=CaSO3↓+2HClO |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
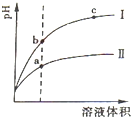 常温下有0.1mol?L-1四种溶液NaOH、NH3?H2O、HCl、CH3COOH
常温下有0.1mol?L-1四种溶液NaOH、NH3?H2O、HCl、CH3COOH查看答案和解析>>
科目:高中化学 来源: 题型:
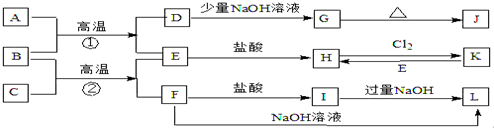
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1.1 mol |
| B、0.87 mol |
| C、0.8 mol |
| D、0.5 mol |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、CH4 |
| B、C3H4 |
| C、C3H6 |
| D、C6H6 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、0.l mol/L醋酸钙溶液中,c(Ca2+)>c(CH3COO-)>c(OH-)>c(H+) |
| B、体积和pH都相同的NH4Cl溶液、盐酸,完全溶解少量且等质量的锌粉,前者所用时间少 |
| C、将n mol H2(g)、n mol I2(g)和2n mol H2 (g)、2n mol I2(g)分别充入两个恒温恒容的容器中,平衡时H2的转化率前者小于后者 |
| D、某物质的溶液中由水电离出的c(H+)=1×10-a mol?L-1,若a>7时,则该溶液的pH一定为14-a |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 弱酸 | HCOOH | HCN | H2CO3 |
| 电离平衡常数(25℃) | Ki=1.77×10-4 | Ki=4.9×10-10 | Ki1=4.3×10-7 Ki2=5.6×10-11 |
| A、0.1 mol?L-lNaHCO3溶液中各离子浓度的大小顺序为:c( Na+)>c(HCO3-)c(HJ-)>c(OH-) |
| B、少量的CO2通人到NaCN溶液中:CN-+H2O+CO2═HCN+HCO3- |
| C、用0.1 mol?L-l NaOH溶液中和等浓度的HCN溶液和HCOOH溶液时,前者所需NaOH溶液体积大 |
| D、相同体积的0.1 mol?L-l HCOONa溶液比0.1 mol?L-l NaCN溶液所含离子总数小 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 一定条件下,在体积为3L的密闭容器中,一氧化碳与氢气反应生成甲醇(催化剂为Cu2O/ZnO):
一定条件下,在体积为3L的密闭容器中,一氧化碳与氢气反应生成甲醇(催化剂为Cu2O/ZnO):| 1 |
| 2 |
| n(H2) |
| n(CH3OH) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com