
| A. | 1 molAl3+含有的核外电子数为3NA | |
| B. | 将58.5g NaCl溶于1.00 L水中,所得NaCL溶液的浓度为1.00mol•L-1 | |
| C. | 1 molCl2与足量的铁反应,转移的电子为数3Na | |
| D. | 常温下,10LpH=1的硫酸溶液中含有的H+离子数为NA. |
分析 A.1个铝离子含有10个电子;
B.溶液的体积大于1L;
C.1molCl2和过量Fe反应生成氯化铁,氯气不足,依据氯气的物质的量计算转移电子数;
D.依据pH=-lg[H+]计算氢离子浓度,依据n=CV计算氢离子的物质的量;
解答 解:A.1个铝离子含有10个电子,1 molAl3+含有的核外电子数为10NA,故A错误;
B.将58.5g NaCl溶于1.00 L水中,溶液的体积大于1L,所得NaCL溶液的浓度小于1.00mol•L-1,故B错误;
C.1molCl2和过量Fe反应生成氯化铁,转移2mol电子,转移电子数为2NA个,故C错误;
D.10L pH=1的硫酸溶液中氢离子浓度为0.1mol/L,1L溶液中含有0.1mol氢离子,含有的H+离子数为NA,故D正确;
故选:D.
点评 本题考查阿伏加德罗常数的有关计算和判断,掌握好以物质的量为中心的各化学量与阿伏加德罗常数的关系,准确弄清分子、原子、原子核内质子中子及核外电子的构成关系是解题关键,注意物质的量浓度中的体积是指溶液的体积,不是溶剂的体积,题目难度不大.


 七彩题卡口算应用一点通系列答案
七彩题卡口算应用一点通系列答案科目:高中化学 来源: 题型:选择题
| A. | 氢气中混有一定量的氧气,可通过灼热的铜网来除去氧气 | |
| B. | 用无水硫酸铜检验CO2气体中是否含有水蒸气 | |
| C. | 除去SO2气体中的CO2,将混合气体通过澄清的石灰水 | |
| D. | 工业上将氯气通入澄清石灰水水制漂白粉 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 卤素 | 氰 | 硫氰 | ① | |
| “单质” | X2 | (CN)2 | (SCN)2 | (OCN)2 |
| 酸 | HX | HCN | ② | HOCN |
| 盐 | KX | KCN | KSCN | ③ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | N2O5 | B. | NO | C. | NO2 | D. | N2O3 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
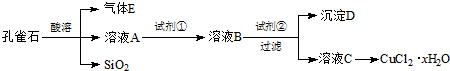
| 离子种类 pH | Fe3+ | Cu2+ | Fe2+ |
| 开始沉淀 | 2.7 | 5.4 | 8.1 |
| 沉淀完全 | 3.7 | 6.9 | 9.6 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 装 置 | NaOH溶液的存放 | 固体物质的称量 | 向容量瓶中转移溶液 |
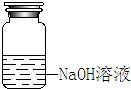 | 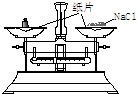 | 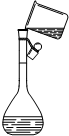 | |
| 错误之处 | 放在了带有磨口玻璃塞的广口瓶中 | 被称量的药品放在右边托盘 | 直接向容量瓶中转移溶液 |
| 如何改正 | 应放在带有橡胶塞的细口瓶中 | 应放在左边托盘中 | 应该用玻璃棒引流 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向漂白粉溶液中通入过量的SO2气体:ClO-+SO2+H2O═HSO3-+HClO | |
| B. | 氯气与水反应:Cl2+H2O═2H++Cl-+ClO- | |
| C. | 向Fe(NO3) 3溶液中加入过量的HI溶液:2Fe3++2I-═2Fe2++I2 | |
| D. | 向NaAlO2溶液中通入过量CO2制Al(OH)3:CO2+AlO2-+2H2O═Al(OH)3↓+HCO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 该气体的摩尔质量 71 g•mol-1 | |
| B. | 标准况况下2.24 L该气体含电子数为1.7 NA | |
| C. | 将1mol该气体通入足量的NaOH中反应,转移电子数为 NA | |
| D. | 该气体的水溶液具有强氧化性,能杀菌消毒和漂白某些物质 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com