
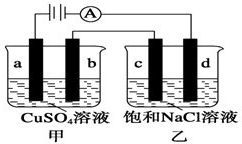
 如图a、b、c、d均为石墨电极,通电进行电解(电解液足量).下列说法不正确的是( )
如图a、b、c、d均为石墨电极,通电进行电解(电解液足量).下列说法不正确的是( )| A、甲中a的电极反应式为4OH--4e-═O2↑+2H2O |
| B、向乙中加入适量盐酸,溶液组成可以恢复 |
| C、电解时向乙中滴入酚酞溶液,d电极附近先变红 |
| D、当b极有6.4g Cu析出时,c电极产生7.1g气体 |
| ||
| ||
| ||


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:

| A、1mol A最多能与4mol H2发生加成反应 |
| B、有机物A与浓硫酸混合加热,可以发生消去反应 |
| C、有机物A可以在一定条件下与HBr发生反应 |
| D、1mol A与足量的NaOH溶液反应,消耗NaOH的物质的量为2mol |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、2mol |
| B、1.5mol |
| C、1mol |
| D、0.5mol |
查看答案和解析>>
科目:高中化学 来源: 题型:
 高铁酸钾(K2FeO4)具有极强的氧化性,是一种优良的水处理剂.其水溶液中FeO
高铁酸钾(K2FeO4)具有极强的氧化性,是一种优良的水处理剂.其水溶液中FeO2- 4 |
| A、不论溶液酸碱性如何变化,铁元素都有4种存在形态 |
| B、向pH=2的这种溶液中加KOH溶液至pH=10,HFeO4-的分布分数先减小后增大 |
| C、pH=2的这种溶液中存在如下等式关系:2[K+]=[H3FeO4+]+[H2FeO4]+[HFeO4-] |
| D、pH=8的这种溶液中存在如下等式关系:[K+]+[H+]=[OH-]+[HFeO4-]+2[FeO42-] |
查看答案和解析>>
科目:高中化学 来源: 题型:
| V |
| 2 |
A、
| ||
B、
| ||
C、
| ||
D、
|
查看答案和解析>>
科目:高中化学 来源: 题型:
| ||
| A、79.97 |
| B、22.85 |
| C、159.91 |
| D、45.69 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、0.1mol?l-1盐酸溶液和0.1mol?l-1氢氧化钠溶液 |
| B、0.1mol?l-1盐酸溶液和0.1mol?l-1氢氧化钡溶液 |
| C、pH=4醋酸溶液和pH=10氢氧化钠溶液 |
| D、pH=4盐酸溶液和pH=10氢氧化钡溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、R2+ |
| B、R+ |
| C、R3+ |
| D、R4+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com