
| A. | SrO可与盐酸反应 | B. | Sr(OH)2难溶于水 | C. | SrSO4难溶于水 | D. | Sr(OH)2是强碱 |
分析 根据第二周期到到第六周期的元素从上往下金属性增强,与水反应越容易,最高氧化物对应的水化物的溶解性增强,碳酸盐都难溶于水,由此分析解答.
解答 解:A、氧化钙与盐酸反应生成盐与水,根据同主族元素及其化合物性质的相似性,所以SrO可与盐酸反应也与盐酸反应生成相应的盐与水,故A正确;
B、氢氧化钙微溶于水,根据同主族元素及其化合物性质的相似性,所以Sr(OH)2溶解性大于氢氧化钙,而不是难溶于水,故B错误;
C、硫酸钙和硫酸钡不溶于水,根据同主族元素及其化合物性质的相似性,所以SrSO4难溶于水,故C正确;
D、氢氧化钙和氢氧化钡都是强碱,根据同主族元素及其化合物性质的相似性,所以Sr(OH)2是强碱,故D正确;
故选B.
点评 本题考查同主族元素性质的相似性和递变性,题目难度不大,本题有类推的方法思考.


 名校练考卷期末冲刺卷系列答案
名校练考卷期末冲刺卷系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 同族元素中Z的氢化物稳定性最高 | |
| B. | 原子半径:X>Y,离子半径:X+>Z2- | |
| C. | 同周期元素中X的金属性最强 | |
| D. | 同周期元素中Y的最高价含氧酸的酸性最强 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | X的最高正价比Y的小 | |
| B. | X的最高价氧化物一定是X2O,Y的气态氢化物为H2Y | |
| C. | X的离子半径比Y的大 | |
| D. | X的核电荷数比Y的小 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 煤的干馏就是将煤隔绝空气在高温使之分解,得到焦炭、煤焦油等物质的过程 | |
| B. | 煤的液化就是将煤转化成甲醇、乙醇等其液态物质的过程 | |
| C. | 煤的气化就是将煤在高温条件由固态转化为气态的物理变化过程 | |
| D. | 通过催化裂化或裂解,可以获得碳原子数较少的轻质油 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①④ | B. | ②③④ | C. | ②④ | D. | 全部正确 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
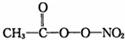 (PAN)等二次污染物.
(PAN)等二次污染物.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com