
| A. | ②③④⑤⑥ | B. | ③⑤⑥ | C. | ①③⑤⑥⑦ | D. | ③⑤⑥⑧ |
分析 该反应中适当增大反应物浓度、升高温度、增大反应物接触面积、形成原电池等方法都能加快反应速率,加入的物质和铁不能反应时生成氢气总量不变,据此分析解答.
解答 解:①3mol/L的硝酸溶液,氢离子浓度增大反应速率加快,但硝酸和Fe反应不是生成氢气,不符合条件,故错误;
②少量CuSO4(s),Fe和硫酸铜发生置换反应生成Cu,Fe、Cu和酸构成原电池而加快反应速率,但生成氢气总量减小,故错误;
③加入一定量的铜,Fe、Cu和酸构成原电池,加快反应速率,且生成氢气质量不变,故正确;
④少量CH3COONa(s),酸和醋酸钠反应生成醋酸导致溶液中氢离子浓度减小,反应速率降低,但生成氢气总量不变,故错误;
⑤对溶液加热(假定盐酸溶质不挥发),增大活化分子百分数,反应速率加快,且生成氢气总量不变,故正确;
⑥向反应液中通入HCl气体,增大氢离子浓度,反应速率加快,且生成氢气总量不变,故正确;
⑦加入过量铁粉,不影响反应速率且生成氢气总量增大,故错误;
⑧将铁粉改为铁片,减小反应物接触面积,反应速率降低,故错误;
故选B.
点评 本题考查化学反应速率影响因素,为高频考点,明确化学反应速率影响原理是解本题关键,注意反应速率影响因素适用范围,题目难度不大,易错选项是①.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:解答题
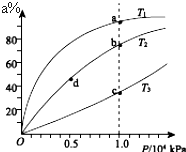 现有反应:mA+nB?ρC,在某温度下达到平衡状态.
现有反应:mA+nB?ρC,在某温度下达到平衡状态.查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 饱和碳酸钠溶液中通入过量二氧化碳气体:CO32-+CO2+H2O═2HCO3- | |
| B. | NaHCO3溶液中滴入偏铝酸钠溶液:HCO3-+AlO2-+H2O═Al(OH)3↓+CO32- | |
| C. | NaHSO3溶液与FeCl3溶液混合溶液颜色变浅:SO32-+2Fe3++H2O═SO42-+2Fe2++2H+ | |
| D. | 向NH4Al(SO4)2溶液中加入Ba(OH)2溶液至SO42-恰好沉淀完全:Al3++2SO42-+2Ba2++4OH-═2BaSO4↓+AlO2-+2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NaHSO3溶液与FeCl3反应:HSO3-+2 Fe3++H2O═SO42-+2Fe2++3H+ | |
| B. | NaHSO3溶液和足量Ca(OH)2溶液反应:Ca2++OH-+HSO3-═CaSO3↓+H2O | |
| C. | NaHSO3溶液和稀HNO3反应:HSO3-+H+═SO2↑+H2O | |
| D. | NaHSO3溶液和NaAlO2溶液反应:HSO3-+AlO2-+H2O═SO32-+Al(OH)3↓ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | a=b=c | B. | c>a>b | C. | a>c>b | D. | a>b>c |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向水中加人稀氨水,平衡逆向移动,c(OH-)降低 | |
| B. | 向水中加入少量固体硫酸氢钠,c(H+)增大,Kw不变 | |
| C. | 向水中加人少量固体NaCl,平衡逆向移动,c(H+)降低 | |
| D. | 将水加热,Kw增大,pH不变 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氧化还原反应中一定有氧元素参与 | |
| B. | 氧化还原反应中所有元素化合价都变化 | |
| C. | 氧化还原反应只有一种元素的化合价变化 | |
| D. | 氧化还原反应中电子有得必有失,化合价有升必有降 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com