
科目:高中化学 来源: 题型:
下列与化学反应能量变化相关的叙述正确的是( )
A.生成物总能量一定低于反应物总能量
B.放热反应的反应速率总是大于吸热反应的反应速率
C.应用盖斯定律,可计算某些难以直接测量的反应焓变
D.同温同压下,H2(g)+Cl2(g)═2HCl(g)在光照和点燃条件下的△H不同
查看答案和解析>>
科目:高中化学 来源: 题型:
两种化合物A和B只含C、H、O三种元素。若A和B以任意物质的量比混合,完全燃烧后生成CO2的体积都是消耗O2体积的2倍(同温同压下测定),即它们的分子组成符合通式:
(CO)x(H2O)y(x、y为正整数)。已知A和B的相对分子质量分别是a和b,且a>b。
请按要求回答下列问题:
(1)若A、B分子中氢原子数相同,A、B相对分子质量的差值一定是(填一个数字)
的整数倍。
(2)试写出符合此条件且A和B的相对分子质量最小的化合物的分子式:A ,B ;结构简式:A ,B 。
(3)写出与(2)中B相对分子质量相差14,且不属于同类物质的两种分子的结构简式: 、 。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关物质用途的说法错误的是( )
|
| A. | 过氧化钠可用作潜艇里氧气的来源 | B. | 单质硅是光导纤维的主要成分 |
|
| C. | 乙醇可用作燃料 | D. | 食醋可用于清除暖水瓶中的水垢 |
查看答案和解析>>
科目:高中化学 来源: 题型:
某学生用NaHCO3和KHCO3组成的某混合物进行实验,测得如下数据(盐酸的物质的量浓度相等):
| 50mL盐酸 | 50mL盐酸 | 50mL盐酸 | |
| m(混合物) | 9.2g | 15.7g | 27.6g |
| V(CO2)(标况) | 2.24L | 3.36L | 3.36L |
则下列分析推理中不正确的是( )
|
| A. | 根据表中数据不能计算出混合物中NaHCO3的 |
|
| B. | 加入混合物9.2 g时盐酸过量 |
|
| C. | 盐酸的物质的量浓度为3.0 mol•L﹣1 |
|
| D. | 15.7 g混合物恰好与盐酸完全反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
在给定一定物质的量的理想气体,影响其所占体积大小的主要因素是 ( )
A.分子直径的大小 B.分子间距离的大小
C.分子间引力的大小 D.分子数目的多少
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各电离方程式中,书写正确的是 ( )
A.CH3COOH 
 H++CH3COO-
H++CH3COO-
B.KHSO4 
 K++H++SO
K++H++SO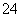
C.Al(OH)3===Al3++3OH-
D.NaH2PO4 
 Na++H2PO
Na++H2PO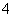
查看答案和解析>>
科目:高中化学 来源: 题型:
硫酸铜是一种应用极其广泛的化工原料。铜不能与稀硫酸直接反应,本实验中将适量浓硝酸分多次加入到铜粉与稀硫酸的混合物中,加热使之反应完全,通过蒸发、结晶得到硫酸铜晶体(装置如图1、2所示)。
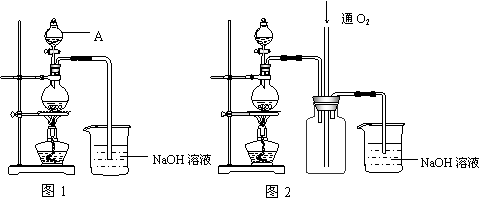

(1)图1烧瓶中发生的离子反应方程式为:
(2)图2是图1的改进装置,其优点有:
① ;② 。
(3)为符合绿色化学的要求,某研究性学习小组进行如下设计:
方案1:以空气为氧化剂。将铜粉在仪器B中反复灼烧,使铜与空气充分反应生成氧化铜,再将氧化铜与稀硫酸反应。
方案2:将空气或氧气直接通入到铜粉与稀硫酸的混合物中,发现在常温下几乎不反应。向反应液中加FeSO4或Fe2(SO4)3,即发生反应。反应完全后向其中加物质甲调节pH到3~4,产生Fe(OH)3沉淀,过滤.蒸发.结晶,滤渣作催化剂循环使用。(已知Fe(OH)3和Cu(OH)2完全沉淀时的pH分别为3.7.6.4。)
请回答下列问题:
①方案1中的B仪器名称是 。
②方案2中甲物质是 (填字母序号)。a.CaO b.CuCO3 c.CaCO3 d.NH3▪H2O
以加入FeSO4为例,用离子方程式解释反应发生的原因
。
方案3 :将3.2g铜丝放到45 mL 1.5mol/L的稀硫酸中,控温在50℃。加入18mL 10%的H2O2,反应0.5小时后,升温到60℃,持续反应1 小时后,过滤.蒸发结晶.减压抽滤等,用少量95%的酒精淋洗后晾干,得CuSO4·5H2O10.6g。
③上述三种方案中,更符合绿色化学理念的是 ,(填方案1、方案2、方案3)
理由是 . . 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com