
用NA表示阿伏加德罗常数的值。下列叙述正确的是 ( )。
A.常温常压下,5.6 g乙烯和环丙烷的混合气体中含有的碳原子数为0.4 NA
B.1 mol Cl2通入足量水中反应转移的电子数为NA
C.0.1 mol·L-1 Na2CO3溶液中CO32-、HCO3-和H2CO3总数为0.1 NA
D.标准状况下,2.24 L三氯甲烷中含有C—Cl数目为0.3 NA
 长江作业本同步练习册系列答案
长江作业本同步练习册系列答案科目:高中化学 来源: 题型:
常温常压下,将x mol CO2气体通入1 L y mol/L的NaOH溶液中,下列对所得溶液 的描述不正确的
A.当x=2y时,随着CO2气体的通入,溶液中
由水电离出的c(H+)有如右图变化关系
B.当x=y时,所得溶液中存在:
c(OH-)+c(CO32—)=c(H+)+c(H2CO3)
C.当2x=y时,所得溶液中存在:
c(Na+)>c(CO32—)>c(OH-)>c(HCO3-)>c(H+)
D.当1/2<x/y<1时,所得溶液中一定存在:
c(Na+)=c(CO32—)+c(HCO3-)+c(H2CO3)
查看答案和解析>>
科目:高中化学 来源: 题型:
用铁片与稀硫酸反应时,下列措施不能使反应速率加快的是
A.加热 B.滴加少量的CuSO4溶液
C.不用稀硫酸,改用98%浓硫酸 D.不用铁片,改用铁粉
查看答案和解析>>
科目:高中化学 来源: 题型:
NA代表阿伏加德罗常数。下列叙述正确的是 ( )。
A.标准状况下,22.4 L己烷中C—C共价键数目为5NA
B.0.1 mol·L-1 AlCl3溶液中含有氯离子数为0.3NA
C.1 mol Fe在1 mol Cl2中充分燃烧,转移电子数为3NA
D.20 g重水(12H2O)所含的电子数为10NA
查看答案和解析>>
科目:高中化学 来源: 题型:
设NA为阿伏加德罗常数的值。下列叙述正确的是
( )。
 A.3 mol NF3与水完全反应生成HNO3和NO,转移
A.3 mol NF3与水完全反应生成HNO3和NO,转移
电子数2 NA
B.标准状况下,32 g硫(结构见图)含SS的数目为2 NA
C.标准状况下11.2 L正戊烷所含共用电子对数为8NA
D.含a mol·L-1 H+的醋酸溶液稀释10倍后,H+为0.1aNA
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各组离子在指定溶液中能大量共存的是 ( )。
A.使酚酞变红色的溶液:Fe3+、Mg2+、SO42-、NO3-
B.KNO3的酸性溶液:Fe2+、Ca2+、Al3+、Cl-
C.常温下,由水电离出的c(H+)=1.0×10-10 mol·L-1的溶液:NH4+、Na+、
SiO32-、CO32-
D.透明的溶液:Cu2+、Fe3+、NO3-、MnO4-
查看答案和解析>>
科目:高中化学 来源: 题型:
在下述条件下,一定能大量共存的离子组是 ( )。
A.无色透明的水溶液中:K+、Ba2+、Cl-、MnO4-
B.含有大量NO3-的水溶液中:NH4+、Fe2+、SO42-、H+
C.滴入酚酞试剂显红色的溶液中:Na+、K+、CO32-、Br-
D.强碱性溶液中:ClO-、S2-、HSO3-、Na+
查看答案和解析>>
科目:高中化学 来源: 题型:
我国某大型电解铜生产企业,其冶炼工艺中铜、硫回收率达到97%、87%。下图表示其冶炼加工的流程:

冶炼中的主要反应:Cu2S+O2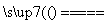 2Cu+SO2
2Cu+SO2
(1)烟气中的主要废气是________,从提高资源利用率和减排考虑,其综合利用方式是_________________________________________________________。
(2)电解法精炼铜时,阳极是________(填“纯铜板”或“粗铜板”);粗铜中含有的金、银以单质的形式沉淀在电解槽________(填“阳极”或“阴极”)的槽底,阴极的电极反应式是_______________________________________。
(3)在精炼铜的过程中,电解质溶液中c(Fe2+)、c(Zn2+)会逐渐增大而影响进一步电解。
几种物质的溶度积常数(Ksp)
| 物质 | Fe(OH)2 | Fe(OH)3 | Zn(OH)2 | Cu(OH)2 |
| Ksp | 8.0×10-16 mol3·L-3 | 4.0×10-38 mol4·L-4 | 3.0×10-17 mol3·L-3 | 2.2×10-20 mol3·L-3 |
①调节电解液的pH是除去杂质离子的常用方法。根据上表中溶度积数据判断,含有等物质的量浓度的Fe2+、Zn2+、Fe3+、Cu2+的溶液,随pH升高最先沉淀下来的离子是________。
②一种方案是先加入过量的H2O2,再调节pH到4左右,加入H2O2的目的是_________________________________________________________________。
加入H2O2后发生反应的离子方程式为________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
最近科学家发现了氧元素的一种新的粒子O4,对于这种新粒子,下列说法不正确的
是( )
A.它是氧气的一种同素异形体 B.它是氧元素的一种同位素
C.它的摩尔质量是64 g·mol-1 D.它具有很强的氧化性
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com