
【题目】(1)气态烃D是石油裂解产品之一,标准状况下D的密度为1.25 g·L-1,根据下列转化关系推断:
A![]() B
B![]() C、A
C、A![]() D
D![]() E
E
请写出A、C、E的结构简式:A________、C________、E________。
(2)写出下列反应的化学方程式:A―→B:_________________________________________;
D―→E:_________________________________________。
【答案】HC≡CH ![]()
![]() CH≡CH+HCl
CH≡CH+HCl![]() CH2=CHCl nCH2=CH2
CH2=CHCl nCH2=CH2![]()
![]()
【解析】
若气态烃D的密度为1.25gL1(标准状况),其摩尔质量=1.25g/L×22.4L/mol=28g/mol,则D结构简式为CH2=CH2,A和氢气发生反应生成D,则A为HC≡CH,D发生加聚反应生成E,则E为聚乙烯,其结构简式为![]() ,A和HCl发生加成反应生成B,B发生加聚反应生成C,C是聚氯乙烯,C结构简式为
,A和HCl发生加成反应生成B,B发生加聚反应生成C,C是聚氯乙烯,C结构简式为![]() ,B为CH2=CHCl,据此分析解答。
,B为CH2=CHCl,据此分析解答。
若气态烃D的密度为1.25gL1(标准状况),其摩尔质量=1.25g/L×22.4L/mol=28g/mol,则D结构简式为CH2=CH2,A和氢气发生反应生成D,则A为HC≡CH,D发生加聚反应生成E,则E为聚乙烯,其结构简式为![]() ,A和HCl发生加成反应生成B,B发生加聚反应生成C,C是聚氯乙烯,C结构简式为
,A和HCl发生加成反应生成B,B发生加聚反应生成C,C是聚氯乙烯,C结构简式为![]() ,B为CH2=CHCl;
,B为CH2=CHCl;
(1)通过以上分析知,A、C、E结构简式分别为HC≡CH、![]() 、
、![]() ,故答案为:HC≡CH;
,故答案为:HC≡CH;![]() ;
;![]() ;
;
(2)A、B结构简式分别为HC≡CH、CH2=CHCl,A发生加成反应生成B,反应方程式为CH≡CH+HCl![]() CH2=CHCl,D、E结构简式分别为CH2=CH2、
CH2=CHCl,D、E结构简式分别为CH2=CH2、![]() ,D发生加聚反应生成E,反应方程式为:nCH2=CH2
,D发生加聚反应生成E,反应方程式为:nCH2=CH2![]()
![]() ,故答案为:CH≡CH+HCl
,故答案为:CH≡CH+HCl![]() CH2=CHCl;nCH2=CH2
CH2=CHCl;nCH2=CH2![]()
![]() 。
。


 课课优能力培优100分系列答案
课课优能力培优100分系列答案 优百分课时互动系列答案
优百分课时互动系列答案科目:高中化学 来源: 题型:
【题目】下列关于有机物的说法中正确的是
①棉花、蚕丝和人造丝的主要成分都是纤维素
②淀粉、油脂、蛋白质在一定条件下都能发生水解
③除去溴苯中的少量溴:加入NaOH溶液,振荡、静置分层后,除去水层
④除去乙酸乙酯中残留的乙酸,加过量饱和![]() 溶液振荡后,静置分液
溶液振荡后,静置分液
⑤塑料、橡胶和光导纤维都是合成高分子材料
⑥石油的分馏、裂化和煤的干馏都是化学变化
A.①⑤⑥B.①②③⑤C.②③④D.③④⑤⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯化亚铜(CuCl)是一种重要的化工产品。它不溶于H2SO4、HNO3 和醇,微溶于水,可溶于浓盐酸和氨水,在潮湿空气中易水解氧化成绿色的碱式氯化铜[Cu2(OH)4-nCln],n随着环境酸度的改变而改变。以海绵铜(主要成分是Cu和少量CuO)为原料,采用硝酸铵氧化分解技术生产CuCl的工艺过程如图:
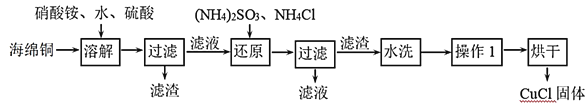
(1)还原过程中主要反应的离子方程式为_______。
(2)实验室为了加快过滤速度,往往采用抽滤的操作(如图)。仪器A的名称__________,有关抽滤,下列说法正确的是__________
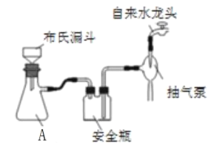
A.抽滤完毕,应先拆下连接抽气泵和吸滤瓶的橡胶管,再关闭水龙头,最后将滤液从吸滤瓶上口倒出
B.在布氏漏斗中放入滤纸后,直接用倾析法转移溶液和沉淀,再打开水龙头抽滤
C.在抽滤装置中洗涤晶体时,为减少晶体溶解损失,应使洗涤剂快速通过滤纸
D.减压过滤不宜用于过滤胶状或颗粒太小的沉淀
(3)操作1为马上再洗涤,然后在真空干燥机内于70℃干燥2h,冷却、密封包装。其中最合理的洗涤试剂__________
A. 浓盐酸 B. 浓氨水 C. 无水乙醇 D. 水+乙醇
真空干燥的原因是___________。
(4)随着pH减小,Cu2(OH)4-nCln中铜的质量分数__________
A. 增大 B. 不变 C. 减小 D. 不能确定
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】右图中的曲线是在其他条件一定时反应:2NO(g)+O2(g)![]() 2NO2(g)(正反应放热)中NO的最大转化率与温度的关系。图上标有A、B、C、D、E五点,其中表示未达到平衡状态,且υ正>υ逆的点是 ( )
2NO2(g)(正反应放热)中NO的最大转化率与温度的关系。图上标有A、B、C、D、E五点,其中表示未达到平衡状态,且υ正>υ逆的点是 ( )
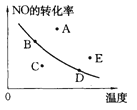
A.A或EB.CC.BD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】聚合硫酸铁是一种新型高效的无机高分子絮凝剂。用硫酸亚铁晶体及硫酸为原料催化氧化法生成硫酸铁,再水解、聚合成产品。实验室模拟生产过程如下:
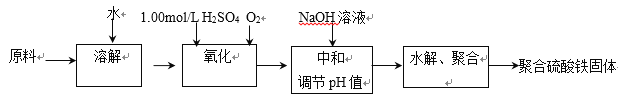
(1)①用原料配制2.50 mol/L的FeSO4溶液时用到的定量仪器有:____________________
②写出氧化过程中的离子方程式:_________________________________________
(2)综合考虑实际投料硫酸亚铁与硫酸的物质的量之比为![]() 左右最佳。 加入的硫酸比理论值稍多,但不能过多的原因是____________________________________________________________________。
左右最佳。 加入的硫酸比理论值稍多,但不能过多的原因是____________________________________________________________________。
(3)硫酸铁溶液水解可以得到一系列具有净水作用的碱式硫酸铁(x Fe2O3·y SO3·z H2O),现采用重量法测定x、y、z的值。
①测定时所需的试剂____________。
(a) NaOH (b) Ba(OH)2 (c) BaCl2 (d) FeSO4
②需要测定____________和____________的质量(填写化合物的化学式)。
(4)选出测定过程中所需的基本操作____________(按操作先后顺序列出)。
a.过滤、洗涤
b.蒸发、结晶
c.萃取、分液
d.冷却、称量
e.烘干或灼烧
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲醇质子交换膜燃料电池中将甲醇蒸气转化为氢气的两种反应原理是:
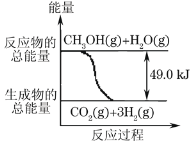
①CH3OH(g)+H2O(g)→CO2(g)+3H2(g) -49.0kJ
②CH3OH(g)+![]() O2(g)→CO2(g)+2H2(g)+192.9kJ
O2(g)→CO2(g)+2H2(g)+192.9kJ
下列说法正确的是( )
A.1molCH3OH完全燃烧放热192.9kJ
B.反应①中的能量变化如图所示
C.CH3OH转变成H2的过程一定要吸收能量
D.根据②推知反应:CH3OH(l)+![]() O2(g)→CO2(g)+2H2(g)+Q的Q<192.9kJ
O2(g)→CO2(g)+2H2(g)+Q的Q<192.9kJ
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲元素原子的![]() 能层上只有一个空原子轨道;乙元素原子的核电荷数为33。根据甲、乙两元素的信息,回答有关问题:
能层上只有一个空原子轨道;乙元素原子的核电荷数为33。根据甲、乙两元素的信息,回答有关问题:
(1)甲的元素符号是______;其电子排布图为______。
(2)乙元素原子的最外层电子排布式为______,其在元素周期表中的位置是______。
(3)甲属于______区元素,乙属于______区元素。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】1mol某烃A和1 mol苯完全燃烧,在相同条件下,生成CO2体积相同,烃A比苯多消耗1mol O2,若A分子结构中无支链或侧链 ,则:
(1)若A为环状化合物,它能与等物质的量的Br2发生加成反应,则A的结构简式为____________________________;
(2)若A为链状烯烃,1mol A最多可和2mol Br2发生加成反应且A与等物质的量的Br2加成后的可能产物只有2种,则A的结构简式为_________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某稀溶液中含有等物质的量的ZnSO4、Fe2(SO4)3、H2SO4、CuSO4,向其中逐渐加入铁粉。下列各图表示溶液中Fe2+的物质的量和加入铁粉的物质的量之间的关系,其中可能正确的是( )
A.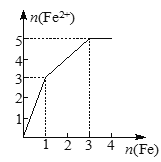 B.
B.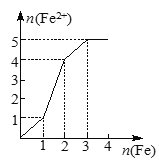
C. D.
D.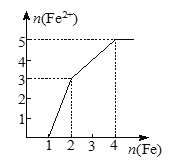
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com