
【题目】现有前四周期A、B、C、D、E、X六种元素,已知B、C、D、E、A五种非金属元素原子半径依次减小,其中B的s能级上电子总数等于p能级上电子总数的2倍.X原子的M能层上有4个未成对电子.请回答下列问题: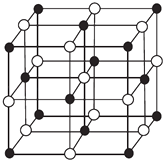
(1)写出C、D、E三种原子第一电离能由大到小的顺序为 . (用元素符号表示)
(2)A原子与B、C、D原子形成最简单化合物的稳定性由强到弱的顺序为(用分子式表示),根据价层电子对互斥理论预测BA2D的分子构型为 .
(3)某蓝色晶体,其结构特点是X2+、X3+离子分别占据六面体互不相邻的顶点,而六面体的每条棱上均有一个BC﹣ . 与A同族且相隔两个周期的元素R的离子位于立方体的恰当位置上.根据其结构特点可知该晶体的化学式为(用最简正整数表示) .
(4)科学家通过X射线探明,KCl、MgO、CaO、TiN的晶体结构与NaCl的晶体结构相似(如图所示),其中3种离子晶体的晶格能数据如下表:
离子晶体 | NaCl | KCl | CaO |
晶格能/kJmol﹣1 | 786 | 715 | 3401 |
根据表格中的数据:判断KCl、MgO、TiN三种离子晶体熔点从高到低的顺序是 . MgO晶体中一个Mg2+周围和它最邻近且等距离的O2﹣有个.
(5)研究物质磁性表明:金属阳离子含未成对电子越多,则磁性越大,磁记录性能越好.离子型氧化物V2O5和Cr2O3中,适合作录音带磁粉原料的是 .
【答案】
(1)F>N>O
(2)H2O>NH3>CH4;平面三角形
(3)KFe2(CN)6
(4)TiN>MgO>KCl;6
(5)Cr2O3
【解析】解:B的s能级上电子总数等于p能级上电子总数的2倍,B的电子排布是1s22s22p2 , 则B是碳元素;结合B、C、D、E、A五种非金属元素原子半径依次减小,根据元素周期律知元素分别是碳、氮、氧、氟、氢,即A为H、C为N、D为O、E为F.X原子的M能层上有4个未成对电子,则其价电子排布式是3d64s2 , 则X是Fe.(1)同周期主族元素,从左到右元素的第一电离能呈增大趋势,但是氮原子的2p轨道上电子半充满,较稳定,第一电离能比氧的大,故第一电离能:F>N>O,所以答案是:F>N>O;(2)元素的电负性越强,气态氢化物就越稳定,非金属性O>N>C,氢化物稳定性由强到弱的顺序为:H2O>NH3>CH4 , 根据价层电子对互斥理论,CH2O的中心原子的杂化方式为sp2杂化,为平面三角形,所以答案是:H2O>NH3>CH4;平面三角形;(3)与A同族且相隔两个周期的元素R为K元素,由题目信息,根据均摊法,晶胞中铁原子有8× ![]() =1,Fe2+、Fe3+离子各占一半,总电荷为+2.5,CN﹣为12×
=1,Fe2+、Fe3+离子各占一半,总电荷为+2.5,CN﹣为12× ![]() =3,所带电荷为﹣3,根据电中性知K+应是0.5个,故化学式为:KFe2(CN)6 , 所以答案是:KFe2(CN)6;(4)对于离子晶体,晶格能越大,熔点越高,则熔沸点TiN>MgO>KCl,MgO与NaCl晶胞结构相似,以图中体心白色球为Mg2+ , 则黑色球为O2﹣ , 1个Mg2+周围和它最邻近且等距离的O2﹣有6个,所以答案是:TiN>MgO>KCl;6;(5)V的价电子排布式是3d34s2 , 有3对孤对电子,Cr的价电子排布式是3d54s1 , 有5对孤对电子,Cr2O3含未成对电子多,则磁性大,磁记录性能越好,所以答案是:Cr2O3 .
=3,所带电荷为﹣3,根据电中性知K+应是0.5个,故化学式为:KFe2(CN)6 , 所以答案是:KFe2(CN)6;(4)对于离子晶体,晶格能越大,熔点越高,则熔沸点TiN>MgO>KCl,MgO与NaCl晶胞结构相似,以图中体心白色球为Mg2+ , 则黑色球为O2﹣ , 1个Mg2+周围和它最邻近且等距离的O2﹣有6个,所以答案是:TiN>MgO>KCl;6;(5)V的价电子排布式是3d34s2 , 有3对孤对电子,Cr的价电子排布式是3d54s1 , 有5对孤对电子,Cr2O3含未成对电子多,则磁性大,磁记录性能越好,所以答案是:Cr2O3 .


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】白铁皮在发生析氢腐蚀时有0.2mol电子转移,下列说法正确的是( )
A.有5.6 g金属被腐蚀
B.有6.5 g金属被氧化
C.有0.15 mol金属失去电子
D.标准状况下有4.48 L H2逸出
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列现象与胶体的性质无关的是 ( )
A. 夏日的傍晚常常看到万丈霞光穿云而过美不胜收
B. 过滤除去氯化钠溶液中的泥沙
C. 食品加工厂利用豆浆中加入盐卤做豆腐
D. 化工厂利用静电除尘技术去除废气中的固体悬浮物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有关如图所示装置的叙述不正确的是( ) 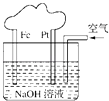
A.这是一个原电池装置
B.该装置中Pt为正极,电极反应为:O2+2H2O+4e﹣═4OH﹣
C.该装置中Fe为负极,电极反应为:Fe﹣2e﹣+2OH﹣═Fe(OH)2
D.这是电解NaOH溶液的装置
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】文房四宝即笔、墨、纸、砚,其中以湖笔、徽墨、宣纸和端砚最为称著。下列说法正确的是
A.徽墨中墨的主要成分是黑色的油脂B.湖笔中笔头的羊毫的主要成分是蛋白质
C.宣纸的主要成分是无机碳和少量的纤维素D.含较多氧化铁的端砚呈黑色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列溶液中有关物质的浓度关系正确的是( )
A.c(NH ![]() )相等的(NH4)2SO4、NH4HSO4、NH4Cl溶液中:c(NH4HSO4)>c[(NH4)2SO4]>c(NH4Cl)
)相等的(NH4)2SO4、NH4HSO4、NH4Cl溶液中:c(NH4HSO4)>c[(NH4)2SO4]>c(NH4Cl)
B.向醋酸钠溶液中加入适量醋酸,得到的酸性混合溶液:c(Na+)>c(CH3COO﹣)>c(H+)>c(OH﹣)
C.1.0 mol/L Na2CO3溶液:c(OH﹣)=c(HCO ![]() )+c(H+)+2c(H2CO3)
)+c(H+)+2c(H2CO3)
D.某二元弱酸的酸式盐NaHA溶液中:c(H+)+c(Na+)=c(OH﹣)+c(HA﹣)+c(A2﹣)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究小组为探究元素周期表中元素性质的递变规律,设计了如下实验。
Ⅰ.(1)将钠、钾、镁、铝各1mol分别投入到足量的同浓度的盐酸中,试预测实验结果:________与盐酸反应最剧烈,________与盐酸反应的速度最慢;________与盐酸反应产生的气体最多。
向Na2S溶液中通入氯气出现黄色浑浊,可证明Cl的非金属性比S强,反应的离子方程式为_______________。
(3)资料显示:钠、镁、铝都可以用于制备储氢的金属氢化物。
① NaH是离子化合物,能与水发生氧化还原反应生成H2,该反应的还原剂是________________。
② NaAlH4是一种良好的储氢材料。NaAlH4与水反应产生氢气的化学方程式为____________________。
Ⅱ.为验证氯、溴、碘三种元素的非金属性强弱,用下图所示装置进行试验(夹持仪器已略去,气密性已检验)。

实验过程:
①打开弹簧夹,打开活塞a,滴加浓盐酸。
②当B和C中的溶液都变为黄色时,夹紧弹簧夹。
③当B中溶液由黄色变为棕红色时,关闭活塞a。
④……
(1)A中发生反应生成氯气,请写出该反应的离子方程式:___________________。
(2)验证氯气的氧化性强于碘的实验现象是________________________。
(3)B、C管口“浸有NaOH溶液的棉花”的作用是__________________________。
(4)为验证溴的氧化性强于碘,过程④的操作和现象是______________________。
(5)过程③实验的目的是____________________。
(6)请运用原子结构理论解释氯、溴、碘非金属性逐渐减弱的原因:_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】简答题:
(1)NH4Cl溶液呈 , 用离子方程式表示原因 .
(2)普通泡沫灭火器的钢铁容器里装着一只小玻璃筒,其中玻璃筒内盛装溶液,使用时,倒置灭火器,两种药液相混合就会喷出含二氧化碳的白色泡沫.产生此现象的离子方程式是 .
(3)NaHSO3溶液呈性,原因 .
(4)在25℃下,向浓度均为0.1molL﹣1的MgCl2和CuCl2混合溶液中逐滴加入氨水,先生成沉淀(填化学式),生成该沉淀的离子方程式为 . 已知25℃时Ksp[Mg(OH)2]=1.8×10﹣11 , Ksp[Cu(OH)2]=2.2×10﹣20 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与生产、生活密切相关。下列说法错误的是
A.生活中“卤水点豆腐”的原理是Mg2+、Ca2+等离子使蛋白质胶体发生聚沉
B.有机玻璃和高温结构陶瓷都属于新型无机非金属材料
C.新能源汽车的推广与使用有利于减少光化学烟雾的产生
D.茶叶中含有的茶多酚可用于制备食品防腐剂
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com