
【题目】A是一种重要的化工原料,A的产量可以用来衡量一个国家的石油化工水平,D是具有果香气味的烃的衍生物.A、B、C、D在一定条件下存在如下转化关系![]() 部分反应条件、产物被省略
部分反应条件、产物被省略![]() .
.
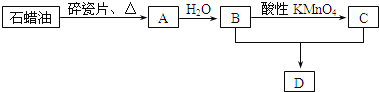
(1)工业上,由石油获得石蜡油的方法是______,由石蜡油获得A是______![]() 填“物理”或“化学”
填“物理”或“化学”![]() 变化.
变化.
(2)![]() 的化学式是______;
的化学式是______;![]() 的反应类型是______反应;写出反应
的反应类型是______反应;写出反应![]() 的化学方程式:______
的化学方程式:______
(3)丁烷是由石蜡油获得A的过程中的中间产物之一,写出它的两种同分异构体的结构简式:______、______.
【答案】分馏 化学 ![]() 加成 CH3CH2OH+CH3COOH
加成 CH3CH2OH+CH3COOH![]() CH3COOCH2CH3+H2O
CH3COOCH2CH3+H2O ![]()
![]()
【解析】
A的产量通常衡量一个国家的石油化工水平,则A应为![]() ,与水在一定条件下发生加成反应生成B为
,与水在一定条件下发生加成反应生成B为![]() ,乙醇被酸性高锰酸钾氧化生成C为
,乙醇被酸性高锰酸钾氧化生成C为![]() ,
,![]() 和
和![]() 在浓硫酸作用下反应生成D为
在浓硫酸作用下反应生成D为![]() 。
。
⑴工业上,由石油分馏获得石蜡油,石蜡油经裂解可得到乙烯,为化学变化;故答案为:分馏;化学。
⑵由上述分析可知,A的化学式为![]() ,
,![]() 是
是![]() 与水在一定条件下发生加成反应生成
与水在一定条件下发生加成反应生成![]() ,反应
,反应![]() 是乙醇与乙酸在浓硫酸、加热条件下生成乙酸乙酯,反应方程式是:CH3CH2OH+CH3COOH
是乙醇与乙酸在浓硫酸、加热条件下生成乙酸乙酯,反应方程式是:CH3CH2OH+CH3COOH![]() CH3COOCH2CH3+H2O;故答案为:
CH3COOCH2CH3+H2O;故答案为:![]() ;加成;CH3CH2OH+CH3COOH
;加成;CH3CH2OH+CH3COOH![]() CH3COOCH2CH3+H2O。
CH3COOCH2CH3+H2O。
⑶丁烷有正丁烷和异丁烷两种同分异构体,结构简式分别为:![]() 、
、![]() ;故答案为:
;故答案为:![]() 、
、![]() 。
。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】第四周期中的18种元素具有重要的用途,在现代工业中备受青睐。
(1)钛原子的价电子排布式为______________________,TiCl4沸点136℃,熔点-25℃,晶体类型为___________晶体。
(2)铜的第二电离能(I2)却大于锌的第二电离能,其主要原因是______________________。
(3)与As同主族的短周期元素是N、P。AsH3中心原子轨道杂化的类型_________________;一定压强下将AsH3、NH3和PH3的混合气体降温时液化顺序是______________________,理由是______________________。
(4)铬是一种硬而脆抗腐蚀性强的金属,常用于电镀和制造特种钢。下图1为铬的晶胞结构图,则铬晶胞属于___________堆积;该晶胞中原子的体积占晶胞体积的百分率为___________。

(5)钴晶体的一种晶胞(如图2所示)的边长为anm,密度为ρg·cm-3,NA表示阿伏加德罗常数的值,则钴原子半径为___________mm,钴的相对原子质量可表示为___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二氧化氯(ClO2,黄绿色易溶于水的气体)是高效、低毒的消毒剂,答下列问題:
(1)工业上可用KC1O3与Na2SO3在H2SO4存在下制得ClO2该反应氧化剂与还原剂物质的量之比为_______________。
(2)实验室用NH4Cl、盐酸、NaClO2(亚氯酸钠)为原料,通过以下过程制备ClO2:
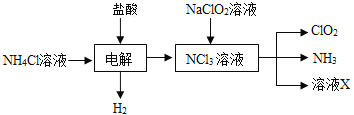
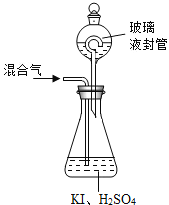
图1 图2
①电解时发生反应的化学方程式为_______________________________________________ 。
②溶液X中大量存在的阴离子有________________________________________________ 。
③除去ClO2中的NH3可选用的试剂是 ___________________(填标号)。
a.水 b.碱石灰 c.浓硫酸 d.饱和食盐水
(3)用上图2装置可以测定混合气中ClO2的含量:
Ⅰ.在锥形瓶中加入足量的碘化钾,用50 mL水溶解后,再加入 3 mL 稀硫酸:
Ⅱ.在玻璃液封装置中加入水.使液面没过玻璃液封管的管口;
Ⅲ.将一定量的混合气体通入锥形瓶中吸收;
Ⅳ.将玻璃液封装置中的水倒入锥形瓶中:
Ⅴ.用0.1000 mol·L-1硫代硫酸钠标准溶液滴定锥形瓶中的溶液(I2+2S2O32-=2I-+S4O62-),指示剂显示终点时共用去20.00 mL硫代硫酸钠溶液。在此过程中:
①锥形瓶内ClO2与碘化钾反应的离子方程式为_______________________________。
②玻璃液封装置的作用是________________________________________________。
③V中加入的指示剂通常为___________,滴定至终点的现象是_________________________。
④测得混合气中ClO2的质量为____________________________ g.。
(4)O2处理过的饮用水会含有一定最的亚氯酸盐。若要除去超标的亚氯酸盐,下列物庾最适宜的是________(填标号)。
a.明矾 b.碘化钾 c.盐酸 d.硫酸亚铁
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】石油是一种重要的资源。A~F是常见有机物,它们之间的转化关系如图1所示(部分产物和反应条件已略去),其中A的产量可以用来衡量一个国家的石油化工发展水平,E是最简单的芳香烃。回答下列问题:

(1)步骤②所用试剂X为___________(写化学式),D的官能团名称是_______;
(2)F的结构简式为________________,步骤①的反应类型:___________;
(3)写出下列步骤中的化学方程式(注明反应条件):
步骤③_____________________________________;
步骤④_______________________________________;
(4)用图2所示实验装置制取乙酸乙酯。请回答:试管b中所装溶液应为_____,乙酸乙酯生成后,分离出产品时的操作方法是______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】绿色化学对化学反应提出了“原子经济性”(原子节约) 新概念及要求。理想的原子经济性反应是原料分子中的原子全部转变成所需产物,不产生副产物,实现零排放。下列反应符合“原子经济性”要求的是( )
A.乙醇与氧气在银的催化作用下反应制备乙醛
B.乙烷与氯气反应制备氯乙烷
C.以苯和乙烯为原料,在一定条件下反应生产乙苯
D.乙醇与浓硫酸共热制备乙烯
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下面是几种有机化合物的转换关系:
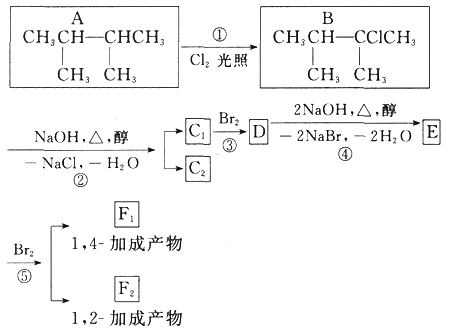
请回答下列问题:
(1)根据系统命名法,化合物A的名称是_____。
(2)上图反应中(填反应类型),①是_____反应,③是_____反应。
(3)E是重要的化工原料,写出由D生成E的化学方程式:_____。
(4)C1的结构简式是_____。
(5)写出符合下列条件的A的同分异构体的结构简式_____。
①含支链 ②核磁共振氢谱有3个峰
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A是天然气的主要成分,以A为原料在一定条件下可获得有机物B、C、D、E、F,其相互转化关系如图。已知烃B在标准状况下的密度为1.06g·L-1,C能发生银镜反应,F为有浓郁香味,不易溶于水的油状液体。
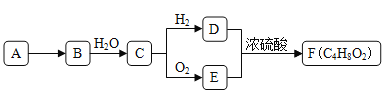
请回答:
(1)有机物D中含有的官能团名称是__________________。
(2) D+E→F的反应类型是_________________________。
(3)有机物A在高温下转化为B的化学方程式是_________________。
(4)下列说法正确的是___。
A.有机物E与金属钠反应比水与金属钠反应要剧烈
B.有机物D、E、F可用饱和Na2CO3溶液鉴别
C.实验室制备F时,浓硫酸主要起氧化作用
D.有机物C能被新制碱性氢氧化铜悬浊液、酸性KMnO4溶液氧化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.已知一氧化碳与水蒸气反应过程的能量变化如图所示:
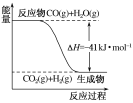
(1)反应的热化学方程式为___________________________。
(2)已知:Ti(s) +2Cl2(g) = TiCl4(l) △H = -804.2kJ/mol;
2Na(s) +Cl2(g) = 2NaCl(s) △H = -882.0kJ/mol
Na(s) = Na(l) △H =+2.6 kJ/mol
请写出用液态钠与四氯化钛置换出钛的热化学方程式_____________________________________
II.在某一容积为2 L的密闭容器内,加入0.8 mol的H2和0.6 mol的I2,在一定条件下发生如下反应:H2(g)+I2(g)![]() 2HI(g) ΔH<0,反应中各物质的浓度随时间变化情况如下图甲所示:
2HI(g) ΔH<0,反应中各物质的浓度随时间变化情况如下图甲所示:

(3)该反应的化学平衡常数表达式为________。
(4)根据图甲数据,反应开始至达到平衡时,平均速率v(HI)为________。
(5)反应达到平衡后,第8分钟时:
①若升高温度,化学平衡常数K________(填“增大”“减小”或“不变”),HI浓度的变化正确的是________(用图乙中a~c的编号回答)。
②若加入I2,H2浓度的变化正确的是________(用图乙中d~f的编号回答)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于阿伏加德罗常数NA的说法正确的是( )
A.标况下11.2LHCl气体溶于0.5L水中,所得溶液中含Cl- 数目为NA
B.NA个Fe(OH)3胶体粒子的质量为107g
C.20gD2O和H218O中含有的质子数为10NA
D.在电解精炼铜过程中转移了NA 个电子,阳极溶解了32g铜
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com