
”¾ĢāÄæ”æÄ³Ń§ÉśÓĆČēÓŅĶ¼ĖłŹ¾µÄ×°ÖĆ½ųŠŠ»Æѧ·“Ó¦X+2Y”ś2ZÄÜĮæ±ä»ÆĒéæöµÄŃŠ¾æ£®µ±ĶłŹŌ¹ÜÖŠµĪ¼ÓŹŌ¼ĮYŹ±£¬æ“µ½ŹŌ¹ÜÖŠ¼×“¦ŅŗĆęĻĀ½µ£¬ŅŅ“¦ŅŗĆęÉĻÉż£®¹ŲÓŚøĆ·“Ó¦µÄĻĀĮŠŠšŹöÕżČ·µÄŹĒ£Ø £©
¢ŁøĆ·“Ó¦ĪŖ·ÅČČ·“Ó¦
¢Ś·“Ó¦ĪļµÄ×ÜÄÜĮæ±ČÉś³ÉĪļµÄ×ÜÄÜĮæøß
¢ŪøĆ·“Ó¦¹ż³ĢæÉŅŌæ“³ÉŹĒ”°Öü“ę”±ÓŚX,YÄŚ²æµÄÄÜĮæ×Ŗ»ÆĪŖČČĮæ¶ųŹĶ·Å³öĄ“£®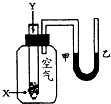
A.¢Ł¢Ś¢Ū
B.¢Ł¢Ū
C.¢Ś¢Ū
D.¢Ū
”¾“š°ø”æA
”¾½āĪö”æ½ā£ŗµ±ĶłŹŌ¹ÜÖŠ¼ÓČėŹŌ¼ĮYŹ±£¬æ“µ½UŠĶ¹ÜÖŠŅŗĆę¼×“¦ĻĀ½µ£¬ŅŅ“¦ÉĻÉż£¬ĖµĆ÷øĆ·“Ó¦ŹĒ·ÅČČ·“Ó¦£¬·Å³öµÄČČŹ¹µĆ¼ÆĘųĘæÖŠĘųŃ¹Éżø߶ų³öĻÖøĆĻÖĻ󣬹Ź¢ŁÕżČ·£¬
ŌŚ·ÅČČ·“Ó¦ÖŠ£¬·“Ó¦ĪļµÄÄÜĮæøßÓŚÉś³ÉĪļµÄÄÜĮ棬¹Ź¢ŚÕżČ·£»
øĆ·“Ó¦¹ż³ĢæÉŅŌæ“³ÉŹĒ”°Öü“ę”±ÓŚX”¢YÄŚ²æµÄÄÜĮæ×Ŗ»ÆĪŖČČĮæ¶ųŹĶ·Å³öĄ“£¬¹Ź¢ŪÕżČ·£®
¹ŹŃ”A£®


 Ņ»æĪŅ»Į·æĪŹ±“ļ±źĻµĮŠ“š°ø
Ņ»æĪŅ»Į·æĪŹ±“ļ±źĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŌŚČēĶ¼µÄŹµŃé×°ÖĆÖŠ£¬ŹµŃéæŖŹ¼Ņ»¶ĪŹ±¼äŗ󣬶Ō擵½µÄĻÖĻ󊚏ö²»ÕżČ·µÄŹĒ£Ø £©
A.
Ę»¹ūæé»įøɱń
B.
µØ·Æ¾§Ģå±ķĆęÓŠ”°°×°ß”±
C.
Š”ŹŌ¹ÜÄŚÓŠ¾§ĢåĪö³ö
D.
pHŹŌÖ½±äŗģ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æÉčNAĪŖ°¢·ü¼ÓµĀĀŽ³£ŹżµÄÖµ”£ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ £Ø £©
A. 10g46£„µÄŅŅ“¼Ė®ČÜŅŗÖŠĖłŗ¬ĒāŌ×ÓŹżÄæĪŖ1.2NA
B. 1L1mol/L Na2CO3ČÜŅŗÖŠŗ¬ÓŠNAøöCO32-
C. µē½ā¾«Į¶ĶµÄ¹ż³ĢÖŠ£¬Ćæ×ŖŅĘNAøöµē×ÓŹ±£¬Ńō¼«ČܽāĶµÄÖŹĮæĪŖ32g
D. ³£ĪĀĻĀpH=1µÄH2SO4ČÜŅŗÖŠ£¬H+µÄÅضČĪŖ0.20mol/L
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ³£ĪĀĻĀ£¬½«³żČ„±ķĆęŃõ»ÆĤµÄA1”¢Cuʬ²åČėÅØHNO3ÖŠ×é³ÉŌµē³Ų(Ķ¼1)£¬²āµĆŌµē³ŲµÄµēĮ÷Ēæ¶Č(I)Ėꏱ¼ä(t)µÄ±ä»ÆČēĶ¼2ĖłŹ¾”£·“Ó¦¹ż³ĢÖŠÓŠŗģ×ŲÉ«ĘųĢå²śÉś”£ĻĀĮŠĖµ·Ø“ķĪóµÄŹĒ £Ø £©

A. t1Ź±æĢĒ°£¬A1ʬµÄµē¼«·“Ó¦ĪŖ£ŗ2A1+3H2O - 6e- ØT A12O3+6H+
B. t1Ź±£¬ŅņA1ŌŚÅØĻõĖįÖŠ¶Ū»Æ£¬Ńõ»ÆĤ×č°ĮĖA1¼ĢŠų·“Ó¦
C. t1Ö®ŗó£¬øŗ¼«CuŹ§µē×Ó£¬µēĮ÷·½Ļņ·¢Éśøıä
D. ÉÕ±ÖŠ·¢ÉśµÄĄė×Ó·“Ó¦ĪŖ£ŗ2NO2+2OH- ØT 2NO3-+H2O
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠ»ÆŗĻĪļÖŠŃōĄė×Ó°ė¾¶ÓėŅõĄė×Ó°ė¾¶±ČÖµ×īŠ”µÄŹĒ
A. NaF B. MgI2 C. BaI2 D. KBr
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĪŅĆĒ“©µÄŅĀ·žĶس£ŹĒÓÉĻĖĪ¬ÖƳɵģ¬³£¼ūµÄĻĖĪ¬ÓŠĆŽ»Ø”¢ŃņĆ«”¢µÓĀŚµČ”£ÓĆ×ĘÉÕ·Øæɳõ²½¼ų±šČżÖÖĻĖĪ¬£¬øųČżÖÖĻĖĪ¬±ąŗÅŗ󣬷ֱš×ĘÉÕ²śÉśµÄĘųĪ¶ČēĻĀ£ŗ
ĻĖĪ¬±ąŗÅ | ¢Ł | ¢Ś | ¢Ū |
×ĘÉÕŹ±µÄĘųĪ¶ | ĢŲŹāĘųĪ¶ | ÉÕÖ½ĘųĪ¶ | ÉÕ½¹ÓšĆ«ĘųĪ¶ |
ŌņŃņĆ«µÄ±ąŗÅĪŖ_________£¬ĆŽ»ØµÄ±ąŗÅĪŖ_________£¬µÓĀŚµÄ±ąŗÅĪŖ_________”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æÓŅĶ¼ŹĒÓ¦ÓƵē»Æѧ·½·Ø¼ģ²āæÕĘųÖŠSO2µÄŌĄķŹ¾ŅāĶ¼”£ĻĀĮŠÓŠ¹ŲĖµ·Ø²»ÕżČ·µÄŹĒ

A. øĆ×°ÖĆ¹¤×÷Ź±Äܽ«»ÆѧÄÜ×Ŗ±äĪŖµēÄÜ£¬²¢ÓŠH2SO4Éś³É
B. µē¼«b±ķĆęO2·¢Éś»¹Ō·“Ó¦£¬µē¼«ø½½üČÜŅŗµÄpHÉżøß
C. µē¼«a±ķĆęµÄµē¼«·“Ó¦Ź½ĪŖ£ŗSO2£«2H2O£2e£===SO![]() £«4H£«
£«4H£«
D. ĘųĢåѳʷӦ“Óµē¼«aĒųÓņĶØČė£¬ŃłĘ·ÖŠµÄSO2ŌŚµē¼«a±ķĆęµĆµ½µē×Ó
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ¢ń£®¼×“¼Č¼ĮĻµē³Ų±»ČĻĪŖŹĒ21ŹĄ¼Ķµē¶ÆĘū³µ×ī¼ŃŗņŃ”¶ÆĮ¦Ō“”£
£Ø1£©101 kPaŹ±£¬1 mol CH3OHŅŗĢåĶźČ«Č¼ÉÕÉś³ÉCO2ŗĶŅŗĢ¬Ė®Ź±·Å³öČČĮæ726.51 kJ£¬Ōņ±ķŹ¾¼×“¼Č¼ÉÕµÄČČ»Æѧ·½³ĢŹ½ĪŖ_______________________________”£
£Ø2£©¼×“¼ÖŹ×Ó½»»»Ä¤Č¼ĮĻµē³ŲÖŠ½«¼×“¼ÕōĘū×Ŗ»ÆĪŖĒāĘųµÄĮ½ÖÖ·“Ó¦ŌĄķŹĒ£ŗ
¢ŁCH3OH(g)+H2O(g)=CO2(g)+3H2(g) ”÷H1=+49.0 kJ”¤mol-1 ¢ŚCH3OH(g)+ ![]() O2(g)= CO2(g)+2H2(g) ”÷H2
O2(g)= CO2(g)+2H2(g) ”÷H2
ŅŃÖŖH2(g)+ ![]() O2(g)===H2O(g) ”÷H = ”Ŗ241.8kJ”¤mol-1£¬Ōņ·“Ó¦¢ŚµÄ”÷H2=_____________”£
O2(g)===H2O(g) ”÷H = ”Ŗ241.8kJ”¤mol-1£¬Ōņ·“Ó¦¢ŚµÄ”÷H2=_____________”£
£Ø3£©¹¤ŅµÉĻŅ»°ćæɲÉÓĆČēĻĀ·“Ó¦Ą“ŗĻ³É¼×“¼£ŗCO(g)+2H2(g)![]() CH3OH(g)£¬ĻÖŌŚŹµŃéŹŅÄ£ÄāøĆ·“Ó¦²¢½ųŠŠ·ÖĪö”£ĻĀĶ¼ŹĒøĆ·“Ó¦ŌŚ²»Ķ¬ĪĀ¶ČĻĀCOµÄ×Ŗ»ÆĀŹĖꏱ¼ä±ä»ÆµÄĒśĻßČēÓŅĶ¼”£
CH3OH(g)£¬ĻÖŌŚŹµŃéŹŅÄ£ÄāøĆ·“Ó¦²¢½ųŠŠ·ÖĪö”£ĻĀĶ¼ŹĒøĆ·“Ó¦ŌŚ²»Ķ¬ĪĀ¶ČĻĀCOµÄ×Ŗ»ÆĀŹĖꏱ¼ä±ä»ÆµÄĒśĻßČēÓŅĶ¼”£

¢ŁøĆ·“Ó¦µÄģŹ±ä¦¤H______0(Ģī”°£¾”±”¢”°£¼”±»ņ”°£½”±)”£
¢ŚT1ŗĶT2ĪĀ¶ČĻĀµÄĘ½ŗā³£Źż“󊔹ŲĻµŹĒK1_______K2(Ģī”°£¾”±”¢”°£¼”±»ņ”°£½”±)”£
£Ø4£©H2 ŗĶCOŗĻ³É¼×“¼·“Ó¦ĪŖ£ŗCO£Øg£©+2H2£Øg£©![]() CH3OH£Øg£©£ØÕż·“Ó¦ŹĒ·ÅČČ·“Ó¦£©”£ŌŚŗćĪĀ£¬Ģå»żĪŖ2LµÄĆܱÕČŻĘ÷ÖŠ·Ö±š³äČė1.2mol COŗĶ1mol H2£¬10minŗó“ļµ½Ę½ŗā£¬²āµĆŗ¬ÓŠ0.4mol CH3OH£Øg£©”£Ōņ“ļµ½Ę½ŗāŹ±COµÄÅضČĪŖ_______£»10minÄŚÓĆH2±ķŹ¾µÄ»Æѧ·“Ó¦ĖŁĀŹĪŖ_______£»ČōŅŖ¼ÓæģCH3OHµÄÉś³ÉĖŁĀŹ²¢ĢįøßCOµÄ×Ŗ»ÆĀŹ£¬æɲÉČ”µÄ“ėŹ©ÓŠ________________£ØĢīŅ»ÖÖŗĻĄķµÄ“ėŹ©£©”£
CH3OH£Øg£©£ØÕż·“Ó¦ŹĒ·ÅČČ·“Ó¦£©”£ŌŚŗćĪĀ£¬Ģå»żĪŖ2LµÄĆܱÕČŻĘ÷ÖŠ·Ö±š³äČė1.2mol COŗĶ1mol H2£¬10minŗó“ļµ½Ę½ŗā£¬²āµĆŗ¬ÓŠ0.4mol CH3OH£Øg£©”£Ōņ“ļµ½Ę½ŗāŹ±COµÄÅضČĪŖ_______£»10minÄŚÓĆH2±ķŹ¾µÄ»Æѧ·“Ó¦ĖŁĀŹĪŖ_______£»ČōŅŖ¼ÓæģCH3OHµÄÉś³ÉĖŁĀŹ²¢ĢįøßCOµÄ×Ŗ»ÆĀŹ£¬æɲÉČ”µÄ“ėŹ©ÓŠ________________£ØĢīŅ»ÖÖŗĻĄķµÄ“ėŹ©£©”£
£Ø5£© ¶žŃõ»ÆĢ¼ŗĻ³É¼×“¼ŹĒĢ¼¼õÅŵĊĀ·½Ļņ£¬½«CO2×Ŗ»ÆĪŖ¼×“¼µÄČČ»Æѧ·½³ĢŹ½ĪŖ£ŗ CO2(g) +3H2(g) ![]() CH3OH(g) +H2O(g) ”÷H ”£
CH3OH(g) +H2O(g) ”÷H ”£
¢ŁøĆ·“Ó¦µÄĘ½ŗā³£Źż±ķ“ļŹ½ĪŖK=___________”£
¢ŚŌŚŗćČŻĆܱÕČŻĘ÷ÖŠŹ¹CO2ŗĶH2£ØĪļÖŹµÄĮæÖ®±ČĪŖ1”Ć3£©·¢ÉśÉĻŹö·“Ó¦£¬·“Ó¦¹ż³ĢÖŠ²āµĆ¼×“¼µÄĢå»ż·ÖŹż¦Õ(CH3OH)Óė·“Ó¦ĪĀ¶ČTµÄ¹ŲĻµČēĻĀĶ¼ĖłŹ¾£¬Ōņ”÷H _________0£ØĢī”°“óÓŚ”±»ņ”°Š”ÓŚ”±£©

²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠŹĀŹµÖŠ£¬²»ÄÜÓĆĄÕĻÄĢŲĮŠŌĄķ½āŹĶµÄŹĒ £Ø £©
A. ĻņK2Cr2O4ČÜŅŗÖŠµĪČėÅصÄNaOHČÜŅŗŗó£¬ČÜŅŗ»ĘÉ«¼ÓÉī
B. ŹµŃéŹŅÓĆÅű„ŗĶŹ³ŃĪĖ®·ØŹÕ¼ÆĀČĘų
C. ·“Ó¦2SO2£«O2![]() 2SO3””¦¤H<0£¬¹¤ŅµÉĻ²ÉČ”øßĪĀµÄ“ėŹ©ÓŠĄūÓŚĢįøßSO2µÄ×Ŗ»ÆĀŹ
2SO3””¦¤H<0£¬¹¤ŅµÉĻ²ÉČ”øßĪĀµÄ“ėŹ©ÓŠĄūÓŚĢįøßSO2µÄ×Ŗ»ÆĀŹ
D. ŗĻ³É°±·“Ó¦£ŗN2£«3H2![]() 2NH3””¦¤H<0£¬ĪŖŹ¹°±µÄ²śĀŹĢįøߣ¬ĄķĀŪÉĻÓ¦²ÉČ”µĶĪĀøßŃ¹µÄ“ėŹ©
2NH3””¦¤H<0£¬ĪŖŹ¹°±µÄ²śĀŹĢįøߣ¬ĄķĀŪÉĻÓ¦²ÉČ”µĶĪĀøßŃ¹µÄ“ėŹ©
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com