
如图所示的甲、乙两个装置中(常温),胶头滴管中吸入某种液体,圆底烧瓶中充入(或放入)另一种物质,挤压胶头滴管中液体,一段时间后两装置中的气球都有明显地胀大(忽略液体体积对气球的影响).则所用试剂分别可能依次是
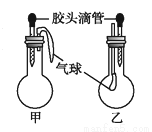
甲 | 乙 | |||
滴管中 | 烧瓶中 | 滴管中 | 烧瓶中 | |
A | 水 | 过氧化钠 | 饱和碳酸氢钠溶液 | CO2 |
B | 水 | 钠 | 饱和碳酸钠溶液 | CO2 |
C | NaOH溶液 | 碳酸氢钠 | 澄清石灰水 | 碳酸氢钠 |
D | 稀盐酸 | 碳酸氢钠 | 饱和食盐水 | Cl2 |
 名校通行证有效作业系列答案
名校通行证有效作业系列答案科目:高中化学 来源:2015-2016学年陕西省高二上10月月考化学试卷(解析版) 题型:选择题
SF6是一种优良的绝缘气体,分子结构中只存在S—F键。已知:1 mol S(s)转化为气态硫原子吸收能量280 kJ,断裂1 mol F—F、S—F键需要吸收的能量分别为160 kJ、330 kJ,则S(s)+3F2(g)=SF6(g)的反应热ΔH为
A.-1528.6 kJ·mol-1 B.+1220 kJ·mol-1
C.-1220 kJ·mol-1 D.+1528.6 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源:2016届江西省高三上学期期中测试化学试卷(解析版) 题型:选择题
二氯化二硫(S2Cl2)是广泛用于橡胶工业的硫化剂,其分子结构如图所示,常温下,S2Cl2是种橙黄色液体,遇水易水解,并产生能使品红褪色的气体,化学方程式为:2S2Cl2+2H2O=SO2↑+3S↓+4HCl下列说法中错误的是
A.S2Cl2的结构式为Cl-S-S-Cl
B.反应中SO2是还原产物,S是氧化产物
C.S2Cl2为含有极性键和非极性键的分子
D.反应中,生成1molSO2,转移电子为3mol
查看答案和解析>>
科目:高中化学 来源:2015-2016学年山西省高二上11月月考化学试卷(解析版) 题型:填空题
在如图所示的装置中,若通直流电5min时,铜电极质量增加2.16 g。试回答下列问题。
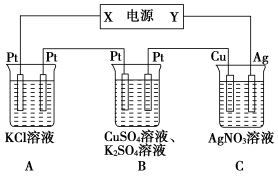
(1)电源中X电极为直流电源的________极。
(2)pH变化:A:________,B:________,C:________。(填“增大”、“减小”或“不变”)
(3)通电5 min时,B中共收集224 mL (标准状况下) 气体,溶液体积为200 mL,则通电前CuSO4溶液的物质的量浓度为________(假设电解前后溶液体积无变化)。
(4)若A中KCl足量且溶液的体积也是200 mL,电解后,溶液的pH为________(假设电解前后溶液体积无变化)。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年山西省高二上11月月考化学试卷(解析版) 题型:选择题
为增强铝的耐腐蚀性,现以铅蓄电池为外电源,以A1作阳极、Pb作阴极,电解稀硫酸,使铝表面的氧化膜增厚。反应原理如下:
电池:Pb(s)+PbO2(s)+2H2SO4(aq)=2PbSO4(s)+2H2O(l)
电解池:2Al+3H2O Al2O3+3H2↑ 电解过程中,以下判断正确的是( )
Al2O3+3H2↑ 电解过程中,以下判断正确的是( )
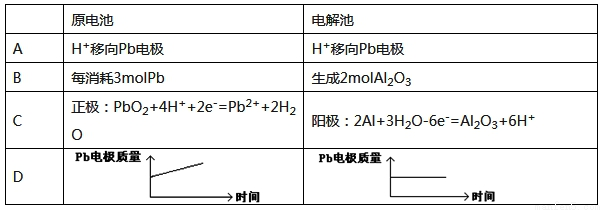
查看答案和解析>>
科目:高中化学 来源:2015-2016学年浙江省高一上期中测试化学试卷(解析版) 题型:选择题
下列物质在水中的电离方程式书写正确的是
A.NaHSO4===Na++HSO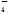 B.NaHCO3===Na++H++CO32-
B.NaHCO3===Na++H++CO32-
C.KClO3===K++Cl-+3O2- D.Al2(SO4)3===2Al3++3SO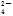
查看答案和解析>>
科目:高中化学 来源:2016届云南省高三上第四次月考理综化学试卷(解析版) 题型:填空题
2015年8月12日晚,天津滨海新区某公司仓库发生爆炸,事发仓库里存放了大量的硝酸铵、氰化钠(NaCN)、金属钠等危险化学品。回答下列问题:
(1)NaCN的电子式为: 。
(2)金属钠属于危化品中的易燃固体,其着火时不能用水灭火,请用化学方程式解释其原因:_____________________________。
(3)氰化钠是一种重要的化工原料,也是剧毒危险品,皮肤伤口接触、吸入、吞食微量可中毒死亡。氰化钠易溶于水,水溶液呈强碱性。氰化钠泄露可用双氧水或硫代硫酸钠中和。
①用离子方程式表示氰化钠水溶液呈强碱性的原因: 。
②用双氧水处理产生一种酸式盐和一种能使湿润的红色石蕊试纸变蓝的气体,请写出该反应的化学方程式_____________________________;
③用硫代硫酸钠中和的离子方程式为CN—+S2O32—→A+SO32—(已配平),A为 (填化学式)。
(4)CN— 中C元素显+2价,N元素显﹣3价,则非金属性N_______C(填<、=或>),请用简单的实验方法证明(要求说明简单操作、现象和结论): 。
(5)0.4mol/L 的NaCN和0.2mol/L的HCl等体积混合,溶液显碱性,其溶液中离子浓度大小排列顺序是
查看答案和解析>>
科目:高中化学 来源:2015-2016学年贵州省高一上半期测试化学试卷(解析版) 题型:选择题
下列说法正确的是
A.直径介于1 nm~100 nm之间的微粒称为胶体
B.制备Fe(OH)3胶体的方法是将饱和FeCl3溶液加热煮沸
C.胶体与浊液的本质区别是其稳定性,胶体属于介稳体系
D.利用丁达尔效应可以区分溶液和胶体溶液
查看答案和解析>>
科目:高中化学 来源:2015-2016学年西藏山南第二高级中学高一上期末化学试卷(解析版) 题型:实验题
实验室中欲配制225mL6 mol•L-1的H2SO4溶液,现有足量的18mol•L-1的浓硫酸。现有三种规格容量瓶:100mL、250 mL、500 mL,试回答:
(1)此时最少需要________ mL 浓H2SO4.
(2)可供选择的仪器除容量瓶外,还有 ①玻璃棒 ②烧瓶 ③烧杯 ④量筒 ⑤药匙 ⑥托盘天平.
上述仪器中,在配制6mol/L 的H2SO4时用不到的仪器是(填代号)________,缺少的仪器是________,你选择的容量瓶的规格是________ mL。使用容量瓶(已经洗涤干净)时的第一步操作是________;
(3)用量筒量取浓硫酸后,应如何混合稀释浓硫酸________;
(4)在配制过程中,下列操作中错误________,能导致结果偏低的操作是________,(填代号,其他操作都正确)。
A.洗涤量取浓H2SO4后的量筒2-3次,并将洗涤液转移到容量瓶中
B.先将浓H2SO4沿着烧杯壁慢慢到入烧杯中,再向烧杯中加入蒸馏水来稀释
C.未等稀释后的H2SO4溶液冷却至室温就转移到容量瓶中
D.定容时,加蒸馏水超过容量瓶刻度,又用胶头滴管吸出
E.转移溶液前,容量瓶中含有少量蒸馏水
F.定容摇匀后,发现液面低于刻度,又用胶头滴管加蒸馏水至刻度
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com