
 按要求完成下列问题:
按要求完成下列问题: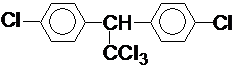 ;
;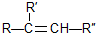 在一定条件下氧化可得产物
在一定条件下氧化可得产物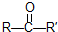 和
和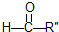 .某烃1mol在一定条件下氧化得到产物
.某烃1mol在一定条件下氧化得到产物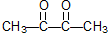 和OHCCH2CH2CHO各1mol.这种烃的结构简式是
和OHCCH2CH2CHO各1mol.这种烃的结构简式是 .
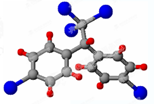
. 分析 (1)DDT人类合成的第一种有机氯农药,可知其分子中含有Cl原子,然后结合球棍模型判断其结构简式;
(2)根据信息中反应原理及反应产物判断该有机物的结构简式.
解答 解:(1)DDT人类合成的第一种有机氯农药,其分子中含有Cl原子,根据DDT的球棍模型可知,其结构简式为: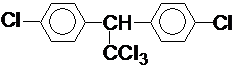
故答案为: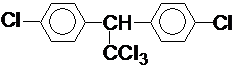
(2)某烃1mol在一定条件下氧化得到产物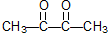 和OHCCH2CH2CHO各1mol,根据信息反应原理可知,将C=O双键的O去掉,然后剩余部分结合形成碳碳双键即可得到反应物,则该烃的结构简式为:
和OHCCH2CH2CHO各1mol,根据信息反应原理可知,将C=O双键的O去掉,然后剩余部分结合形成碳碳双键即可得到反应物,则该烃的结构简式为:
故答案为:
点评 本题考查了有机物结构简式的书写,题目难度中等,注意掌握球棍模型的表示意义、常见有机物结构与性质,(2)为难点,明确信息反应原理为解答关键.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:选择题
| A. | pH=0的溶液中:ClO-、Cu2+、SO42-、K+ | |
| B. | 使pH试纸变红色的溶液中:Fe2+、I-、NO3-、Cl- | |
| C. | 能够和金属镁反应放出气体的溶液中:Na+、H+、SO42-、Cl- | |
| D. | 常温下,水电离出的c(H+)与c(OH-)乘积为10-28的溶液中:K+、Na+、HS-、Ca2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
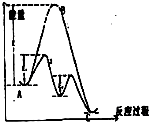
| A. | 使用正催化剂能够加快反应的速率,根本上是由于催化剂参与反应,并且同等程度地降低了正逆反应的活化能 | |
| B. | 2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑△H>0,该反应过程可用该图象表示 | |
| C. | 使用催化剂不仅能加快反应速率,而且可以让不可能发生的反应发生,如利用催化技术处理汽车尾气:2CO+2NO═2CO2+N2 | |
| D. | 化学反应的本质是旧键断裂,新键形成,如图可知反应的能量变化由旧键断裂释放的能量和新键形成吸收的能量大小决定 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1 mol甲与足量的乙完全反应共转移了1 mol电子 | |
| B. | Y元素在周期表中的位置为第三周期第ⅣA族 | |
| C. | 原子半径:W>Z>Y>X | |
| D. | 1.0 L 0.1 mol•L-1戊溶液中阴离子总的物质的量小于0.1 mol |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 只有①② | B. | 只有①③ | C. | 只有②③ | D. | 只有①④ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
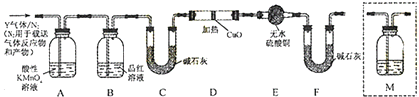
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com