
| A. | 在蔗糖中加入浓硫酸后出现发黑现象,说明浓硫酸具有脱水性 | |
| B. | 浓硫酸和浓盐酸混合可制氯化氢 | |
| C. | 常温下,浓硫酸可以用铝罐贮存,说明铝与浓硫酸不反应 | |
| D. | 反应CuSO4+H2S→CuS↓+H2SO4能进行,说明硫化铜既不溶于水,也不溶于稀硫酸 |
分析 浓硫酸具有强氧化性,可用铝发生钝化反应,与硫化氢、碳等发生氧化还原反应,具有吸水性,可用于干燥气体,浓硫酸具有脱水性,可使蔗糖碳化,以此解答该题.
解答 解:A.在蔗糖中加入浓硫酸后出现发黑现象,说明浓硫酸具有脱水性,故A正确;
B.浓硫酸溶于水放热,且盐酸易挥发,可用于制备少量氯化氢,故B正确;
C.常温下,铝于浓硫酸发生钝化反应,在表面生成一层致密的氧化膜而阻碍反应的继续进行,故C错误;
D.反应符合复分解的条件,说明硫化铜不溶于稀硫酸和水,故D正确.
故选C.
点评 本题综合考查硫酸的性质,为高频考点,侧重考查学生的双基以及元素化合物知识的综合理解和运用,注意浓硫酸的脱水性、吸水性的区别,难度不大.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:选择题
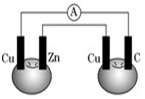 重庆市璧山中学校在化学兴趣活动中,曾老师利用番茄做成电池(如图所示),铜片和锌片用导线连接后插入番茄里,则碳是( )
重庆市璧山中学校在化学兴趣活动中,曾老师利用番茄做成电池(如图所示),铜片和锌片用导线连接后插入番茄里,则碳是( )| A. | 阳极 | B. | 正极 | C. | 阴极 | D. | 负极 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Ba(OH)2 | B. | BaCl2 | C. | Ba(NO3)2 | D. | NaOH |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
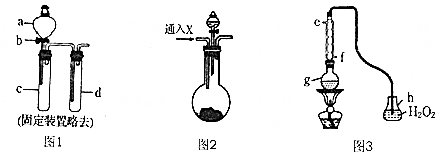
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氢氧化钡溶液与稀硫酸混合:Ba2++SO42-→BaSO4↓ | |
| B. | 铁粉溶于稀硫酸中:2Fe+6H+→2Fe3++3H2↑ | |
| C. | 氨水与盐酸混合:OH-+H+→H2O | |
| D. | 硫化钠溶液中滴加硝酸银:S2-+2Ag+→Ag2S↓ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 化学性质 | 实际应用 |
| A | Na、K均是活泼金属 | 钠钾合金用作原子反应堆导热剂 |
| B | H2O2能使蛋白质变性 | 医疗上用于伤口消毒 |
| C | CH2=CH2能与H2O发生加成反应 | 乙烯用作果实的催熟剂 |
| D | NH3具有还原性 | 作食品加工的制冷剂 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com