
| A. | ②③⑥ | B. | ①③⑥ | C. | ②④ | D. | ③⑤ |
分析 ①碳酸钠和盐酸的加入量和顺序不同,离子反应不同分析;
②依据氢氧化铝不溶于弱酸弱碱分析判断;
③酸性H2CO3>C6H5OH>HCO3-;
④硝酸银和氨水的量不同加入顺序不同现象不同,离子反应不同进行分析;
⑤从亚铁离子和碘离子的还原性不同,加入氯水量的多少不同,产物不同分析;
⑥酸式盐和对应碱的反应与量无关分析.
解答 解:①碳酸钠少量时发生的反应为CO32-+2H+=CO2↑+H2O;碳酸钠过量的反应离子方程式为CO32-+H+=HCO3-,所以量不同反应不同,故①不符合;
②硫酸铝溶液与氨水的反应只有,Al3++3NH3•H2O=Al(OH)3↓+3NH4+与量无关,故②符合;
③苯酚钠中通入二氧化碳反应生成碳酸氢钠和苯酚,与量无关,C6H5O-+CO2+H2O→C6H5OH+HCO3-,故③符合;
④硝酸银溶液与氨水反应,氨水多时生成银氨溶液,氨水少时生成氢氧化银沉淀,所以量不同产物不同,反应不同,故④不符合;
⑤Fe2+<I-的还原性,氯水的量的多少不同,反应进行的程度不同,少量氯水时只氧化亚铁离子,氯水过量氧化亚铁离子后继续氧化碘离子,故⑤不符合;
⑥碳酸氢钙溶液与澄清石灰水的反应Ca2++HCO3-+OH-=CaCO3↓+H2O,与量无关,故⑥符合;
综上所述②③⑥符合;
故选A.
点评 本题考查了离子方程式的书写原则,难度中等,主要是量不同会发生不同的离子反应的离子方程式的书写,关键是熟练掌握离子的性质和产物与过量试剂的后续反应的性质掌握.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:多选题
| A. | MgCl2 | B. | FeCl2 | C. | AlCl3 | D. | CuCl2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
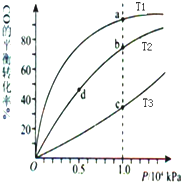
| A. | 温度:T1>T2>T3 | B. | 平衡常数:K(a)>K(c) K(b)=K(d) | ||
| C. | 正反应速率:v(a)>v(c) v(b)>v(d) | D. | 平均摩尔质量:M(a)<M(c) M(b)>M(d) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用胶头滴管加液时,不能伸入试管中 | |
| B. | 蒸馏盛在烧瓶中含水的酒精,需在瓶内放一些碎瓷片 | |
| C. | 萃取实验中涉及气体压强原理 | |
| D. | 用容积为100 mL的量筒量取80 mL无水乙醇,使液面最低点至刻度80 mL处 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | X>Z>Y | B. | Z>Y>X | C. | X>Y>Z | D. | Z>X>Y |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用过滤的方法分离溶液和胶体 | |
| B. | 用四氯化碳萃取碘水中的碘 | |
| C. | 用蒸馏的方法将自来水制成蒸馏水 | |
| D. | 用加热的方法分离氯化钠和单质碘固体 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | △H<0、△S>0的反应在任何温度下都能自发进行 | |
| B. | NH4HCO3(s)═NH3 (g)+H2O(g)+CO2(g)△H=+185.57 kJ•mol-1能自发进行,原因是体系有自发地向混乱度增加的方向转变的倾向 | |
| C. | 硝酸铵固体的溶解过程与焓变有关 | |
| D. | 在其他外界条件不变的情况下,使用催化剂,可以改变化学反应进行的速率 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com