
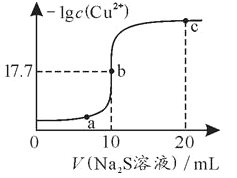
【题目】某温度下,向10 mL 0.1 mol·L-1 CuCl2溶液中滴加0.1 mol·L-1的Na2S溶液,滴加过程中溶液中-lgc(Cu2+)与Na2S溶液体积(V)的关系如图所示,下列有关说法正确的是( )(已知:Ksp(ZnS)=3×10-25)
A.a、b、c三点中,水的电离程度最大的为b点
B.Na2S溶液呈碱性的原因: S2-+2H2O![]() H2S+ 2OH-
H2S+ 2OH-
C.a、b、c三点中, b点溶液中S2-度最小
D.向100 mL Zn2+、Cu2+浓度均为10-5mol·L-1的混合溶液中逐滴加入10-4 mol·L-1的Na2S溶液,Cu2+先沉淀
【答案】D
【解析】
从图中可以看出,在b点,Cu2+与S2-刚好完全反应,生成CuS沉淀;在a点,Cu2+有剩余;在c点,S2-过量,据此分析解答。
A. a、b、c三点中,a、c分别为Cu2+和S2-水解,都能促进水的电离,而b点水发生电离没有获得帮助,所以电离程度最小,A错误;
B. 多元弱酸的阴离子应分步电离,而不能一步完成,B错误;
C. a、b、c三点中, a点溶液中Cu2+有剩余,S2-浓度最小,C错误;
D. Ksp(ZnS)=3×10-25,Ksp(CuS)=10-17.7×10-17.7=10-35,CuS的溶度积小,先生成沉淀,
向100 mL Zn2+、Cu2+浓度均为10-5mol·L-1的混合溶液中逐滴加入10-4 mol·L-1的Na2S溶液,Cu2+先沉淀,D正确。
故选D。


 小学生10分钟口算测试100分系列答案
小学生10分钟口算测试100分系列答案科目:高中化学 来源: 题型:
【题目】下列过程或现象与盐类水解无关的是
A.向Na2CO3溶液中滴加酚酞试液变红色B.实验室保存硫酸亚铁溶液时加入少量铁粉
C.加热FeCl3溶液颜色会变深D.KAl(SO4)2·12 H2O可用于净水
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列图象与对应的说法正确的是![]()
A.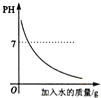 向NaOH溶液中加水稀释
向NaOH溶液中加水稀释
B. 等质量的Al、Zn与足量的稀硫酸反应
等质量的Al、Zn与足量的稀硫酸反应
C. 向稀硫酸中加入
向稀硫酸中加入![]() 溶液
溶液
D. 恒温下,适量蒸发饱和NaCl溶液的水分
恒温下,适量蒸发饱和NaCl溶液的水分
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,用0.1000 mol·L-1 NaOH溶液滴定20.00 mL 0.1000 mol·L-1 CH3COOH溶液所得滴定曲线如图。下列说法不正确的是( )
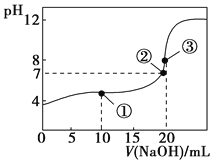
A. 在曲线上任一点均存在:c(Na+)c(OH-) = c(CH3COO-)c(H+)
B. 点①所示溶液中:c(CH3COO-)+2c(OH-) = c(CH3COOH)+2c(H+)
C. 点②所示溶液中:c(Na+) = c(CH3COO-)
D. 点③所示溶液中:c(Na+) > c(OH-) > c(CH3COO-) > c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】取等物质的量浓度的NaOH溶液两份A和B,每份10mL,分别向A、B中通入不等量的CO2,再继续向两溶液中逐滴加入0.2mol/L的盐酸,标准状况下产生的CO2气体体积与所加的盐酸溶液体积之间的关系如图所示,下列叙述正确的是( )

A. A曲线表明原NaOH溶液中通入CO2后,所得溶液中的溶质成分是Na2CO3和NaHCO3
B. B曲线中消耗盐酸0<v(HCl)<25mL时发生的离子反应为:OH-+H+=H2O H++CO32-=HCO3-
C. B曲线表明原NaOH溶液中通入CO2后,所得溶液加盐酸后产生CO2气体体积(标准状况)的最大值为224mL
D. 原NaOH溶液的物质的量浓度为1.0mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,求下列溶液的pH(已知lg2=0.3)。
(1)0.1mol·L-1的CH3COOH溶液(已知CH3COOH的电离常数Ka=1.8×10-5)。
(2)0.1mol·L-1NH3·H2O溶液(NH3·H2O的电离度为α=1%,电离度=![]() ×100%)。
×100%)。
(3)将pH=8的NaOH与pH=10的NaOH溶液等体积混合。
(4)将pH=5的盐酸与pH=9的NaOH溶液以体积比11∶9混合。
则(1)pH=___;(2)pH=___;(3)pH=___;(4)pH=___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应的离子方程式书写正确的是( )
A.H2SO4溶液与氢氧化钠反应:OH-+H+=H2O
B.铝与NaOH溶液反应:Al+2OH-= ![]() +H2↑
+H2↑
C.AlCl3溶液与氨水反应:AlCl3+3OH-=Al(OH)3↓+3Cl-
D.Cl2与氢氧化钠溶液反应:Cl2+2OH-=2ClO-+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】人们对苯的认识有一个不断深化的过程。已知分子式为 C6H6的结构有多种,其中的两种为:
Ⅰ.![]() Ⅱ.
Ⅱ.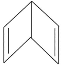
(1)这两种结构的化学性质区别表现在:Ⅰ不能____(填字母,下同),而Ⅱ能____。
A.被酸性KMnO4溶液氧化
B.与溴水发生加成反应
C.与氢气发生加成反应
(2)已知Ⅰ结构下,该物质能在一定条件下与液溴反应,其反应方程式为________________。
(3)今发现C6H6还可能有另一种如下图所示的立体结构,该结构的四氯代物有______种。
![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯化亚铜(CuCl)广泛应用于化工、印染、电镀等行业。CuCl微溶于水,不溶于稀酸,可溶于Cl-浓度较大的体系,在潮湿的空气中易水解氧化。以海绵铜(主要成分是Cu和少量CuO)为原料,采用硝酸铵氧化分解技术生产CuCl的工艺过程如下:
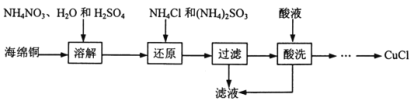
(1)基态铜原子核外电子排布式为:________。
(2)为了提高溶解速率,可以适当加热到60~70℃,还可以采用的措施为________。
(3)溶解步骤的温度控制在60~70℃,温度不宜过高的原因是________。该步骤中Cu 与NH4NO3反应的离子方程式为 (N元素被还原到最低价)_________________。
(4)还原步骤发生反应的离子方程式为______________________。
(5)滤液的主要成分为__________(写化学式)。
(6)酸洗时,可选用稀硫酸或稀盐酸,但不能用浓盐酸的原因是_________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com