
【题目】已知断裂1 mol H2(g)中的H—H键需要吸收436.4 kJ的能量,断裂1 mol O2(g)中的共价键需要吸收498 kJ的能量,生成H2O(g)中的1 mol H—O键能放出462.8 kJ的能量。下列说法正确的是( )
A. 断裂1 mol H2O中的化学键需要吸收925.6 kJ的能量
B. 2H2(g)+O2(g)===2H2O(g) ΔH=-480.4 kJ·mol-1
C. 2H2O(l)===2H2(g)+O2(g) ΔH=471.6 kJ·mol-1
D. H2(g)+![]() O2(g)===H2O(l) ΔH=-240.2 kJ·mol-1
O2(g)===H2O(l) ΔH=-240.2 kJ·mol-1
【答案】B
【解析】A.生成H2O(g)中的1molH-O键能放出462.8KJ的能量,则断裂1molH2O(g)中的化学键需要吸收热量462.8KJ×2=925.6KJ,但并未说明水的状态,故A错误;B.2H2(g)+O2(g)═2H2O(g)△H=(436.4KJ/mol)×2+(498KJ/mol)-2×2×(462.8KJ/mol)=-480.4KJmol-1,故B正确;C.2H2O(g)=2H2O(l)△H=-88KJ/mol,则2H2(g)+O2(g)═2H2O(l)△H=-568.4KJ/mol,可知2H2O(l)═2H2(g)+O2(g)△H=+568.4KJmol-1,故C错误;D.2H2(g)+O2(g)═2H2O(l)△H=-568.4KJ/mol,则H2(g)+![]() O2(g)═H2O(l)△H=-284.2KJmol-1,故D错误;故选B。
O2(g)═H2O(l)△H=-284.2KJmol-1,故D错误;故选B。


科目:高中化学 来源: 题型:
【题目】下图是以苯酚为主要原料制取冬青油和阿司匹林的过程:

(1)写出第①步反应的离子方程式:__________________________,
(2)B溶于冬青油致使产品不纯,可用下列哪种试剂即可除去________,
A. Na B. NaOH 溶液 C. Na2CO3溶液 D. NaHCO3溶液
(3)冬青油含有的官能团名称为________________,
(4)写出阿司匹林在加热条件下与足量NaOH 溶液反应的化学方程式_____________________,
(5)下列有关描述不正确的是________。
A.第②步反应中的酸A可以是稀H2SO4
B.第③步反应的类型为取代反应
C.1 mol冬青油与浓溴水反应最多可消耗3 mol Br2
D.可以利用FeCl3溶液鉴别冬青油和阿司匹林
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】苯环上原有取代基对新导入取代基所占的位置有一定影响,其规律是:(1)苯环上新导入的取代基所占的位置主要取决于原有取代基的性质。(2)把原有取代基分成两类:一类取代基主要使新导入的取代基进入苯环的邻位和对位,如—CH3(或烃基)、—Br等;另类取代基主要使新导入的取代基进入苯环的间位,如—NO2、—CHO等。(假设一个反应只能引入一个取代基)
已知:苯在FeBr3粉存在的条件下与液溴发生取代反应:
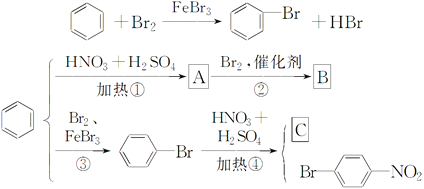
请回答下列问题:
(1)写出A、B、C的结构简式:
A____________,B____________,C____________。
(2)写出下列转化的化学方程式,并指明反应类型。
①______________________________,____________________;
②______________________________,____________________;
③______________________________,____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列检验离子的方法及现象描述正确的是 ( )
A. 检验Na+:将干净的铂丝蘸取少量溶液在酒精灯上灼烧,观察火焰呈浅紫色
B. 检验NH![]() :滴入NaOH溶液后,加热,用湿润红色石蕊试纸检验发现变蓝
:滴入NaOH溶液后,加热,用湿润红色石蕊试纸检验发现变蓝
C. 检验SO![]() :加入BaCl2溶液出现白色沉淀,再加足量稀盐酸沉淀不溶解
:加入BaCl2溶液出现白色沉淀,再加足量稀盐酸沉淀不溶解
D. 检验Cl-:确定溶液中无SO![]() 后,加入AgNO3溶液出现白色沉淀
后,加入AgNO3溶液出现白色沉淀
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. 元素周期表中有8个主族
B. 稀有气体元素原子的最外层电子数均为8
C. 氢是原子半径最小的元素
D. 氮元素位于第二周期VIIA族
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关性质的比较,不能用元素周期律解释的是
A. 金属性:Na > Mg B. 酸性:H2SO4 > HClO
C. 碱性:KOH > NaOH D. 热稳定性:HC1 > HBr
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上生产钾是用钠和熔化的KCl反应制取,反应方程式为KCl+Na![]() NaCl+K。
NaCl+K。
有关数据见下表:
熔点/℃ | 沸点/℃ | 密度/(g·cm-3) | |
Na | 97.8 | 883 | 0.97 |
K | 63.7 | 774 | 0.86 |
KCl | 770 | 1 500 | 1.984 |
NaCl | 801 | 1 413 | 2.165 |
(1)上述反应是_____反应;是否符合金属活动性顺序?________。
(2)上述反应是在_____(填“气态”“液态”或“固态”)下进行,生成的金属钾是_____(填“气态”“液态”或“固态”)。
(3)反应温度确定在850 ℃,如果反应温度确定在900 ℃行不行?_____,其原因是______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com