
| … | ① | ② | ③ | |
| … | ④ | ⑤ |
 .
.分析 由元素在短周期中的位置可知,①为C、②为N、③为O、④为P、⑤为S,
(1)电子层数=周期数,最外层电子数=族序数;
(2)①~⑤元素均为非金属元素;
(3)②的气态氢化物为氨气;
(4)非金属性越强,元素最高价氧化物对应水化物的酸性越强.
解答 解:由元素在短周期中的位置可知,①为C、②为N、③为O、④为P、⑤为S,
(1)电子层数=周期数,最外层电子数=族序数,则从原子结构角度分析,①、②、③三种元素的电子层数相同,②、④位于元素周期表的第ⅤA族,
故答案为:电子层数;ⅤA;
(2)①~⑤元素均为非金属元素,可寻找高效农药的元素,而催化剂、耐高温、耐腐蚀的合金材料均为金属元素,半导体材料在金属与非金属的交界处,
故答案为:a;
(3)②的气态氢化物为氨气,其电子式为 ,故答案为:
,故答案为: ;
;
(4)非金属性S>P,元素最高价氧化物对应水化物的酸性较强的物质的化学式为H2SO4,故答案为:H2SO4.
点评 本题考查位置、结构、性质,为高频考点,把握元素的位置、性质、原子结构为解答的关键,侧重分析与应用能力的考查,注意原子结构与元素位置的关系,题目难度不大.


科目:高中化学 来源: 题型:推断题
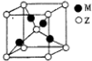 X、Y、Z、R、M是原子序数依次增大的五种元素,基态X原子的s电子数比p电子数多3个,
X、Y、Z、R、M是原子序数依次增大的五种元素,基态X原子的s电子数比p电子数多3个,查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 时间/min | 0 | 5 | 10 | 15 | 20 | 25 | 30 |
| c(X)/mol/L | 0.2 | c | 0.6 | 0.6 | 1.0 | c1 | c1 |
| c(Y)/mol/L | 0.6 | c | 0.4 | 0.4 | 0.4 | c2 | c2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
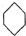 (g)?3H2(g)+
(g)?3H2(g)+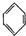 (g)△H1
(g)△H1 (g)+H2(g)→
(g)+H2(g)→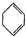 (g)△H2=+28.6KJ/mol
(g)△H2=+28.6KJ/mol (g)+2H2(g)→
(g)+2H2(g)→ (g)△H3=-237KJ•mol-1
(g)△H3=-237KJ•mol-1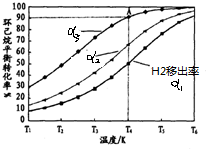
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
| 周期 族 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | O |
| 2 | ⑥ | ⑦ | ⑧ | |||||
| 3 | ① | ③ | ⑤ | ⑨ | ⑩ | |||
| 4 | ② | ④ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
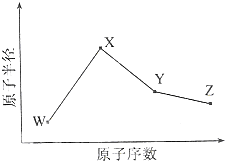 W、X、Y、Z是四种常见的短周期元素,其原子半径随原子序数变化如图所示.已知W的一种核素的质量数为18,中子数为10;X和Ne原子的核外电子数相差1;Y的单质是一种常见的半导体材料;Z的电负性在同周期主族元素中最大.
W、X、Y、Z是四种常见的短周期元素,其原子半径随原子序数变化如图所示.已知W的一种核素的质量数为18,中子数为10;X和Ne原子的核外电子数相差1;Y的单质是一种常见的半导体材料;Z的电负性在同周期主族元素中最大.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ax/100bmol/L | B. | ax/500bmol/L | C. | ax/2000bmol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com